איזומריות ציס-טראנס


בכימיה, איזומריות ציס-טראנס או איזומריות גאומטרית היא סוג של סטריאו-איזומריות המתארת את האוריינטציה של קבוצות פונקציונליות במולקולה. איזומרים כאלה כוללים בדרך כלל קשרים כפולים, כיוון שהאטומים המקושרים אינם יכולים להסתובב סביב ציר הקשר. תיתכן גם איזומריות מסוג זה במבנים טבעתיים, בהם יכולת הסיבוב סביב הקשרים מוגבלת מאוד, וכן בקומפלקסים מתכתיים בעלי סימטריה מרובעת כגון ציספלאטין.
המושג "איזומריות גאומטרית" נחשב לשם נרדף מיושן של "איזומריות ציס-טראנס", לפי ארגון IUPAC. לעיתים הוא משמש לתיאור סטריאו-איזומריות כללית (כלומר, משמש גם לציון איזומרים אופטיים); המונח הנכון לציון סטריאו-איזומריות לא-אופטיות הוא דיאסטריאואיזומריות.
לחומר בעלת איזומריות ציס-טרנס שתי צורות - צורת ציס, וצורת טראנס. במקרה בו המתמירים מצביעים בכיוונים דומים, הדיאסטראומר מכונה "ציס", וכאשר הם מצביעים בכיוונים מנוגדים הדיאסטריאומר מכונה "טראנס". 2-בוטן מהווה דוגמה לפחמימה קטנה המציגה איזומריות ציס-טראנס (ראו משמאל).
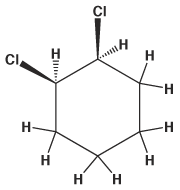
גם לתרכובות אליציקליות ייתכנו איזומרי ציס וטרנס. דוגמה טובה לכך היא 1,2-דיכלורוציקלוהקסאן:
 |
|
| trans-1,2-dichlorocyclohexane | cis-1,2-dichlorocyclohexane |
תכונות פיזיקליות של איזומרי ציס וטראנס[עריכת קוד מקור | עריכה]
לעיתים קרובות לאיזומרי ציס וטראנס תכונות פיזיקליות שונות. ההבדלים בין האיזומרים נובעים בדרך כלל מצורת המולקולה, או ממומנט הדיפול הכולל שלה. הבדלים אלה יכולים להיות קטנים מאוד, כמו במקרה של נקודת הרתיחה של אלקנים לא מסועפים - לציס-2-פנטן טמפרטורת רתיחה של 36°C, ולטרנס-2-פנטן - 37°C. לעומתם, במקרה כמו ציקלואוקטן, לאיזומר הציס טמפ' רתיחה של 145°C, ולטראנס - 75°C בלבד. ההבדל הגדול בין האיזומרים נובע מהמתח הטבעתי הגדול בטראנס-ציקלואוקטן, שגם מפחית מאוד את יציבותו לעומת איזומר הציס. במקרה אחר, 2-butenedioic acid, ההבדלים הגדולים בתכונות הפיזיקליות ובריאקטיביות הביאו למתן שני שמות שונים לגמרי - אזור הציס קרוי חומצה מלאית, והטראנס - חומצה פומרית.
ניתן לזהות מגמות כלליות במקרה של איזומרים גאומטריים הנובעים מנוכחות קשרים כפולים, ובמיוחד כאשר שני המתמירים זהים. מגמות אלה נובעות מהעובדה שהדיפולים של המתמירים באיזומר הטראנס מתקזזים (עקב הפנייה לכיוונים מנוגדים), בעוד שבאיזומר הציס נוצר דיפול שקול חזק בכיוון המשותף. כתוצאה מכך, לאיזומרי טראנס יש בדרך כלל צפיפות נמוכה יותר מאשר לאיזומרי ציס.
לפי March,[1] באופן כללי לטראנס-אלקנים סימטריה גבוהה מאיזומרי הציס, ויש להם נקודת רתיחה גבוהה יותר, ומסיסות נמוכה יותר בממסים אינרטיים. קבועי הפיצול האופייניים בספקטרוסקופיית NMR גבוהים יותר עבור איזומר הטראנס (בין 12 ל-18 הרץ, ערך טיפוסי: 15Hz), לעומת איזומר הציס (בין 0 ל-12 הרץ, ערך טיפוסי: 8Hz).
סימוני E/Z[עריכת קוד מקור | עריכה]

שיטת ציס/טרנס למתן שמות אינה מתאימה למקרים בהם יש יותר משני מתמירים שונים על אטומי הקשר הכפול. למקרים אלה פותחה שיטת סימון E/Z - האות Z מגיעה מהמילה הגרמנית zusammen ("ביחד"), המחליפה את הסימון ציס, והאות E - מהמילה entgegen ("נגד"), המחליפה את הסימון טראנס.
ההבחנה בין איזומר E ל-Z נעשית בעזרת כללי הדירוג של קהאן-אינגולד-פרלוג. באופן כללי - לאטומים בעלי מספר אטומי גבוה יותר - דירוג גבוה יותר ועבור אטומים זהים, קבוצות גדולות יותר (אתיל לעומת מתיל, לדוגמה) מקבלות דירוג גבוה יותר. אם שני המתמירים בעלי הדירוג הגבוה ביותר (אחד מכל צד של הקשר הכפול) פונים לאותו כיוון - האיזומר יכונה Z, ואם הם פונים לכיוונים מנוגדים - יכונה E.
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- הגדרת סטריאואיזומריות לפי IUPAC
- הגדרת איזומריות גאומטרית לפי IUPAC
- הגדרת איזומריות ציס-טראנס לפי IUPAC
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ Advanced organic Chemistry, Reactions, mechanisms and structure 3ed. page 111 Jerry March ISBN 0-471-85472-7
