אנהידריד אצטי
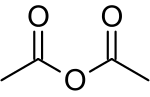 | |
| מולקולת אנהידריד אצטי | |
 | |
| שם סיסטמטי |
acetic anhydride |
|---|---|
| שמות נוספים | ethanoic anhydride, Acetic acid anhydride, Acetyl acetate |
| כתיב כימי |
C₄H₆O₃ |
| מסה מולרית | 102.09 גרם/מול |
| מראה | נוזל שקוף |
| מספר CAS | 108-24-7 |
| צפיפות | 1.082 גרם/סמ"ק |
| מצב צבירה | נוזל |
| טמפרטורת היתוך |
−73.1 °C 200.05 K |
| טמפרטורת רתיחה |
139.8 °C 412.95 K |
| מקדם שבירה | 1.3901 |
| אנתלפיית התהוות סטנדרטית | 628.4 - קילוג'ול למול |
| LD50 | 1,000 חלקים למיליון, 1,780 מיליגרם לקילוגרם, 4 מיליליטר |
| NFPA 704 | |
אנהידריד אצטי (ACETIC ANHYDRIDE) הוא תרכובת אורגנית שנוסחתה CH3CO)2O) מסומן גם כ Ac2O. החומר הוא אנהידריד (אלמימה) של חומצה אצטית וזהו האנהידריד הפשוט ביותר שניתן לבודד[1]. אנהידריד אצטי הוא נוזל שקוף שריחו כשל חומצת חומץ בשל התגובה עם אדי מים שבאוויר. לחומר יישומים בסינטיזה אורגנית.
ייצור[עריכת קוד מקור | עריכה]
אנהידריד אצטי מופק מתגובת דה-הידרציה של חומצה אצטית ב-800°C. נדרשת הפרדת התוצרים כדי למנוע תגובה מחודשת עם המים לפרוק התוצר.

החומר מופק גם בתגובת פחמן חד-חמצני CO עם מתיל אצטט (אסתר של מתנול וחומצה אצטית) בתגובה:
בתהליך הופך המתיל אצטט למתיל יודיד ומלח אצטט. הCO מגיב עם מתיל יודיד לקבלת אצטיל יודיד CH3C(O)I שמגיב עם מלח האצטט או עם חומצה אמטית לקבלת התוצר. הקטליזטורים הוא רודיום יודיד RhI3 וליתיום יודיד LiI. כיוון שהאנהידריד אינו יציב במים התגובה מבוצעת בממס אל מיימי.
תגובות[עריכת קוד מקור | עריכה]
אנהידריד אצטי הוא ריאגנט למגוון תגובות אצטיליציה (acetylation) כלומר הוספת קבוצת אצטיל CH3CO למולקולות, בעיקר של כהלים ואמינים. ניתן לראות באנהידריד מקור ל+CH3CO, בתגובות אלו כך למשל בתגובה בין אנהידריד אצטי לאתנול להפקת אתיל אצטט
לפעמים בסיס כפירידין משמש כקטליזטור לתגובות אלו.
שימושים[עריכת קוד מקור | עריכה]
- אנהידריד אצטי שימש לייצור צלולוז-אצטט (פולימר ששימש לייצור סרטי צילום וסיבים) מצלולוז.
- החומר משמש לייצור אספירין מחומצה סליצילית

- שימור עץ על ידי החדרת האנהידריד לעץ הגולמי באוטוקלב
- ייצור עמילן מעובד לתעשיית המזון
- משמש ליצירת הרואין
בטיחות[עריכת קוד מקור | עריכה]
אנהידריד אצטי הוא חומר מגרה ודליק. נשימת אדי החומר מסוכנת. בנוכחות מי חמצן נוצר החומר הנפיץ דיאצטיל פראוקסיד.
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- MSDS (גיליון בטיחות חומרים) של אנהידריד אצטי (אנגלית)
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ אנהידריד פורמי פשוט שיותר אלא שהוא מתפרק ספונטנית מחוץ לתמיסה



