אלפא-סינוקלאין
ערך ללא מקורות
| ||
| ערך ללא מקורות | |
יש לערוך ערך זה. ייתכן שהערך סובל מבעיות ניסוח, סגנון טעון שיפור או צורך בהגהה, או שיש לעצב אותו, או מפגמים טכניים כגון מיעוט קישורים פנימיים.
| ||
| יש לערוך ערך זה. ייתכן שהערך סובל מבעיות ניסוח, סגנון טעון שיפור או צורך בהגהה, או שיש לעצב אותו, או מפגמים טכניים כגון מיעוט קישורים פנימיים. | |
אלפא-סינוקלאין (באנגלית: alpha-synuclein או α-synuclein) הוא חלבון ממשפחת הסינוקלאינים[5], הנמצא בכמות גדולה במוח האדם. כמויות קטנות יותר נמצאות בלב, בשרירים וברקמות אחרות. במוח, אלפא-סינוקלאין נמצא בעיקר בקצות תאי העצב, בתוך מבנים הנקראים "קצוות טרום-סינפטיים". שם הוא נכנס לאינטראקציה עם פוספוליפידים ועם חלבונים.
במסגרת תהליך של העברה סינפטית, הקצוות הטרום-סינפטיים משחררים חומרים הקרויים מוליכים עצביים מתוך שלפוחיות סינפטיות. תהליך זה משמש להעברת איתותים בין תאי העצב והוא חיוני לתפקוד התקין של המוח. על אף שתפקיד האלפא-סינוקלאין אינו מובן כהלכה, ישנם מחקרים לפיהם הוא ממלא תפקיד בשמירה על אספקת השלפוחיות הסינפטיות בקצוות הטרום-סינפטיים באמצעות היווצרותן של אשכולות (clustering) של שלפוחיות סינפטיות. הוא עשוי גם לסייע בבקרת השחרור של דופמין, סוג של מוליך עצבי שהוא חיוני, בין השאר, לבקרת התחלתן ועצירתן של תנועות בלתי רצוניות[6]. האלפא-סינוקלאין הוא גם המרכיב העיקרי של גופי לוי האופייניים למחלת פרקינסון[7].
חלבון האלפא-סינוקליאין האנושי מורכב מ-140 חומצות אמינו והוא מקוּדד על ידי הגן SNCA. נמצא כי אלפא-סינוקלאין הוא גם קודמן של המרכיב נון-א-בטא (NACP) (non- A-beta- component precursor) של העמילואיד האופייני למחלת אלצהיימר.
התבטאות ברקמות[עריכת קוד מקור | עריכה]
אלפא-סינוקלאין הוא חלבון מסוג סינוקלאין בעל תפקיד לא ידוע היטב הנמצא בעיקר ברקמת עצב והמהווה כ-1% מכלל החלבונים שבציטוזול של תאי המוח. נמצא בייחוד בנאוקורטקס, היפוקמפוס, החומר השחור, תלמוס ובמוחון. אלפא-סינוקלאין הוא בראש ובראשונה חלבון נוירונלי אך נמצא גם בתאי גלייה.[8] במלנוציטים התבטאות החלבון מווסתת על ידי הגורם MITF - Microphthalmia-associated transcription factor. הימצאות האלפא-סינוקלאין בגרעיני הנוירונים שבמוחות היונקים רומז על תפקיד האלפא-סינוקלאין בגרעין של התא. עם זאת הוא נמצא בעיקר בקצוות הטרום-סינפטיים, גם כשהוא חופשי וגם כשהוא קשור לקרום התאי. בכל רגע נתון 15% מאלפא-סינוקלאין שבנוירונים קשור לקרום התא. מאוחר יותר נמצא כי אלפא סינוקלאין ממוקם במיטוכונדריות הנוירונליות. הוא מתבטא בצורה מוגברת במיטוכונדריה של פקעת ההרחה (Olfactory bulb), ההיפוקמפוס, הסטריאטום ובתלמוס, אזורים שהם עתירים גם באלפא-סינוקלאין ציטוזולי. אולם קליפת המוח והמוחון מהווים יוצאים מן הכלל, בכך שמכילים הרבה מאוד אלפא-סינוקלאין ציטוזולי ורמות נמוכות מאוד של אלפא-סינוקלאין מיטוכונדרי. הוכח כי אלפא סינוקלאין מתמקם בקרום הפנימי של המיטוכונדריות ושההשפעה המעכבת של אלפא-סינוקלאין על הפעילות I המורכבת בשרשרת הנשימה היא תלוית מנה. כמו כן הועלתה הסברה שהאלפא-סינוקלאין במיטוכונדריות מתבטא באופן שונה באזורים מוחיים שונים ושרמות הרקע של האלפא- סינוקלאין עלולות להפריע לתפקוד המיטוכונדריה ולהביא נוירונים מסוימים לניוון.
לפחות שלושה איזופורמים של סינוקלאין נוצרים דרך שחבור חלופי. הצורה הנפוצה ביותר של החלבון והנחקרת ביותר, היא החלבון בעל אורך מלא של 140 חומצות אמינו. איזופורמים אמרים הם אלפא-סינוקלאין-126 החבר שאריות 41–54 עקב חוסר האקסון 3 (exon 3); ואלפא=סינוקלאין 112 החסר שארית 103–130 שנוצר עקב חוסר אקסון 5.
פעילות אוטופורטאוליטית[עריכת קוד מקור | עריכה]
בעזרת ספקטרומטריית מסה המבוססת על ניידות יונים (IMS-MS) בעלת רזולוציה גבוהה על אלפא-סינוקלאין מטוהר בעזרת HPLC in vitro נמצא כי אלפא -סינוקלאין יכול להיות אוטופרוטאוליטי, כלומר לפרק את עצמו תוך היווצרות מגוון של קטעים קטנים. ייתכן כי תוצרים אוטופרוטאוליטים כאלה ממלאים תפקיד כחומרי ביניים או קואנזימים בצבירת האלפא-סינוקלאין in vivo.
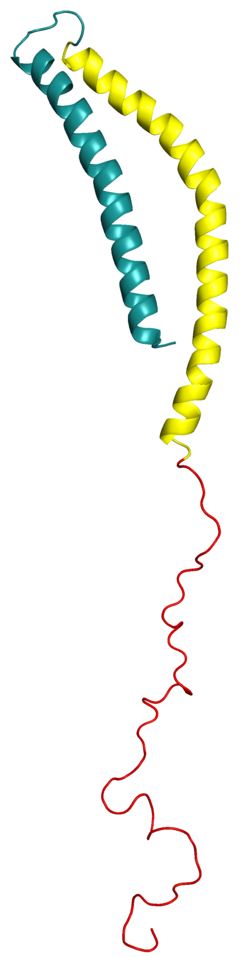
מבנה[עריכת קוד מקור | עריכה]
אלפא-סינוקלאין נחשב לחלבון בעל מבנה פנימי משובש, כלומר חסר מבנה תלת-ממדי יחיד ויציב. נכון לשנת 2014 דיווחים רבים רמזו על קיומם של מבנים חלקיים או של מצבים אוליגומריים מובנים בתוך מבנה התמיסה של אלפא-סינוקאלין, אפילו בהיעדרם של ליפידים. מגמה זו נתמכת גם על ידי מספר רב של מדידות של מולקולות בודדות באמצעות מלקחיים אופטיים על עותקים בודדים של אלפא-סינוקלאין מונומרי ועל דימרים או טטרמרים חלבוניים מחוזקים קוולנטית.
רצף[עריכת קוד מקור | עריכה]
המבנה הראשוני של אלפא-סינוקלאין מחולק בדרך כלל לשלושה מתחמים שונים:
- שיירי 1–60 - עם זיקה חזקה לקרום התא:
קצה אמיני אמפיפאתי שבו בולטים ארבעה שיירי-11 חוזרים, הכוללים רצף הסכמה KTKEGV. לרצף זה נטייה מבנית לסליל אלפא, הדומה לזו של מתחמים המקשרים אפוליפיופרוטאינים.
- שיירי 61–95: אזור מרכזי הידרופובי, הכולל את "המרכיב הלא-אמילואידדי בטא" (non-amyloid-β component (NAC, המעורב בצבירת חלבונים.
- שיירי 96–140: אזור בעל חומציות גבוהה ועתיר-פרולין - ללא נטייה מבנית ייחודית
תפקיד[עריכת קוד מקור | עריכה]
באוכלוסייה בדידה של קצוות טרום- סינאפטיים במוח בעת תקופה של סידור סינפטי מחדש נמצא ויסות-מעלה של אלפא-סינוקלאין. מחקרים הצביעו על אינטראקציה משמעותית בין אלפא סינוקלאין לטובולין ואלפא-סינוקלאין מסוגל לפעול לפעמים כחלבון העשוי להלוות למיקרוטובולים, כמו חלבון טאו.
לפי מחקרים נוספים ייתכן כי אלפא-סינוקלאין יכול לפעול כחלבון סוכך ("שפרון" מולקולרי) ביצירת קומפלקסים SNARE. הוא נקשר בעיקר לפוספוליפידים של קרום התא דרך תחום הקצה האמיני ולסינפטוברווין-2 דרך הקצה הקרבוקסילי, ומעורבותו חשובה בפעילות הסינפטית. הצטברו עדויות כי אלפא-סינוקלאין מעורב בתפקוד מערכת גולג'י של הנוירון ובמעברי הבועיות. לכאורה אלפא-סינוקלאין הוא חיוני להתפתחות הנורמלית של התפקודים הקוגניטיביים. עכברי נוקאאוט עם אינאקטיבציה ממוקדת של התבטאות האלפא-סינוקלאין סובלים מפגיעה בלמידה המרחבית ובזיכרון העבודה.
אינטראקציות עם ליפידים[עריכת קוד מקור | עריכה]
מחד קיימים נתונים על האינטראקציה של אלפא-סינוקלאין עם קרום התא ועל מעורבותו בהרכב הקרום ומחזור שלו. מסריקת גנום השמרים נמצא כי מספר גנים המעורבים בחילופי החומרים הליפידים ממלאים תפקיד ברעילות של האלפא-סינוקלאין. מאידך, רמת ההתבטאות של אלפא-סינוקלאין משפיעה על צמיגות ועל הכמות היחסית של חומצות השומן בדו-השכבה הליפידית.
אלפא-סינוקלאין נקשר במישרין עם קרומי הליפידים, תוך התחברות לשטחים הטעונים שלילית של פוספוליפידים. הוא יוצר מבנה מורחב הליקלי על בועיות קטנות. חד-למלריות אלפא-סינוקלאין נראה יוצר חלקיקים דמויי-דיסקה ליפידיים הדומים לאפוליפופרוטאינים. היו מחקרים שתמכו באפשרות של פעילות נוגדת חימצון של האלפא-סינוקלאין בקרום.
אינטראקציות עם חלבונים[עריכת קוד מקור | עריכה]
הוכח שאלפא-סינוקלאין נכנס לאינטראקציה עם:
משמעות קלינית[עריכת קוד מקור | עריכה]


בזמנו נחשב אלפא-סינוקלאין לחלבון מסיס בלתי מובנה. עם זאת צורות שלו שלא עברו מוטציה יוצרות טטרמר מקופל יציב עמיד בפני צבירה. אף על פי שנתון זה שוחזר והורחב בכמה מעבדות, הוא עדיין שנוי במחלוקת. עם זאת אלפא-סינוקלאין מצטבר כדי ליצור פיברילים (סיבונים) בלתי מסיסים במצבים פתולוגיים המתאפיינים בקיומם של גופי לוי, כדוגמת מחלת פרקינסון, הקהיון עם גופי לוי והאטרופיה המערכתית הנפוצה. הפרעות אלה נקראות סינוקלאינופאתיות. האלפא-סינוקלאין הוא המרכיב המבני הראשוני של סיבוני גופי לוי. לעיתים מכילים גופי לוי חלבון טאו. אולם אלפא-סינוקלאין והחלבון טאו מהווים קבוצות משנה שונות של פילמנטים (חוטונים) בתוך אותם גופי הסגר. ניתן למצוא פתולוגיה של אלפא-סינוקלאין גם במקרים ספורדיים ומשפחתיים של מחלת אלצהיימר.
מנגנון הצבירה של אלפא-סינוקלאין אינו ברור. קיימות הוכחות לצורת ביניים עתירת משטחי בטא היכולה לבשר את הצבירה ובסופו של דבר קודמן של גופי לוי. מחקר יחיד משנת 2008 רמז כי אלפא סינוקלאין קיים כתערובת באיזון של קונפורמר בלתי מובנים, של מבני סליל אלפא ועתירי משטח בטא. מוטציות או של בופר הידועים כמשפרים את הצבירה מגבירים בצורה ניכרת את כמות הקופנורמרים בטא. ממצא זה מצביע כי זו קונפורמציה הקשורה לצבירה פתולוגית. בין האסטרטגיות בטיפול הסינוקלאינופאתיות נשקל השימוש במעכבים של צבירת אלפא-סינוקלאין. הוכח למשל כי מולקולה קטנה של קומינאלדהיד מעכב פיברילציה של אלפא-סינוקלאין. במחלות אלה יש חשד במעורבות הנגיף אפשטיין בר.
במקרים נדירים של צורות משפחתיות של מחלת פרקינסון, קיימת מוטציה בגן המקודד את אלפא סינוקאלין. זוהו חמש מוטציות נקודתיות. דווח על השפעה של מוטציות מסוימות בשלבי ההתחלה וההגברה של תהליך הצבירה. דופליקציה וטריפליקציה של הגן נראות כסיבה נדירה של מחלת פרקינסון במשפחות אחרות, אך יותר שכיחה מהמוטציות הנקודתיות. מכאן ההשערה כי מוטציות מסוימות של אלפא סינוקלאין עלולות לגרום לפיברילים דמויי-אמילואיד התורמים להיווצרות מחלת פרקינסון.
ייתכן כי צורת פריונית של החלבון אלפא-סינוקלאין היא הסוכן הפתוגני של מחלת האטרופיה המערכתית הנפוצה.
ראו גם[עריכת קוד מקור | עריכה]
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- האתר Genetics Home Reference של SNCA gene- NIH
- באתר Uniprot
- *[Uéda K, Fukushima H, Masliah E, Xia Y, Iwai A, Yoshimoto M, Otero DA, Kondo J, Ihara Y, Saitoh T (Dec 1993). Molecular cloning of cDNA encoding an unrecognized component of amyloid in Alzheimer disease. Proceedings of the National Academy of Sciences of the United States of America 90 (23). с. 11282–6
- [Xia Y1, Saitoh T, Uéda K, Tanaka S, Chen X, Hashimoto M, Hsu L, Conrad C, Sundsmo M, Yoshimoto M, Thal L, Katzman R, Masliah J Alzheimers Dis. 2001 Oct;3(5):485-494. E.https://www.ncbi.nlm.nih.gov/pubmed/12214035]
Characterization of the human alpha-synuclein gene: Genomic structure, transcription start site, promoter region and polymorphisms
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ 1 2 3 GRCh38: Ensembl גרסה 89: ENSG00000145335 - Ensembl, מאי 2017
- ^ 1 2 3 GRCm38: Ensembl גרסה 89: ENSMUSG00000025889 - Ensembl, מאי 2017
- ^ "Human PubMed Reference:".
- ^ "Mouse PubMed Reference:".
- ^ קיימים גם סינוקאלין בטא וגאמא
- ^ על הגן SNCA באתר NIH והספרייה הלאומית לרפואה של ארצות הברית
- ^ Leonidas Stefanis, α-Synuclein in Parkinson’s Disease, Cold Spring Harbor – Perspectives in Medicine, 13 December 2011
- ^ Alice Filippini, Massimo Gennarelli, Isabella Russo, α-Synuclein and Glia in Parkinson’s Disease: A Beneficial or a Detrimental Duet for the Endo-Lysosomal System?, ResearchGate, March 201
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.