תסמונת קרצינואידית
| הסבר בסרטון | |
| תחום | אנדוקרינולוגיה, אונקולוגיה |
|---|---|
| שכיחות | 5 אנשים פר מיליון תושבים[1] |
| גורם | גידול אנדוקריני[1] |
| תסמינים | הסמקה, שלשול, עייפות,[1] |
| אבחון | בדיקת שתן וסריקת דימות[1] |
| טיפול | ניתוח, כימותרפיה[1] |
| סיבוכים | תת לחץ דם, מחסור בניאצין, מחלת לב מסתמית[1] |
| קישורים ומאגרי מידע | |
| eMedicine |
276837 |
| MeSH | D008303 |
| סיווגים | |
| ICD-10 |
E34.0 |
| ICD-11 |
5B10 |
תסמונת קרצינואידית היא קבוצה של תסמינים המתרחשים כתוצאה מחומרים המשתחררים על ידי גידולים נוירואנדוקריניים (גידולים קרצינואידים).[1] התסמינים עשויים לכלול הסמקה, שלשול, צפצופים, גירוד, דלדול שרירים ועייפות.[1] סיבוכים עשויים לכלול לחץ דם נמוך, מחסור בניאצין ומחלת לב מסתמיים והסיבוך הנפוץ ביותר, אי ספיקת תלת-צדדית .[1]
התסמונת מופיעה אצל כ-10% מהאנשים עם גידולים נוירואנדוקריניים.[1] לרוב מדובר בגידולים המערבים את המעי ומתפשטים לכבד.[1] התקפות עלולות להיגרם על ידי אכילה, אלכוהול או מתח.[1] התקפות עלולות להיות מגורות על ידי חומרים כגון סרוטונין, היסטמין, ופרוסטגלנדינים .[1] התסמונת מסווגת כתסמונת פאראנופלסטית .[2] אבחון התסמונת הוא בדרך כלל על ידי בדיקת שתן של 24 שעות ולאחר מכן הדמיה רפואית לאיתור הגידול.[1]
הטיפול עשוי לכלול אוקטריאוטיד, לנראוטיד, ניתוח וכימותרפיה .[1] תסמונת קרצינואיד היא נדירה.[1] כ-5 מיליון אנשים מאובחנים בה בשנה.[1] הימצאות התסמונת נפוצה לרוב החל מגיל 55 עד 60 שנים.[1] גברים ונשים מושפעים מהתסמונת כמעט באופן שווה.[1] התסמונת תוארה לראשונה בשנת 1953.[3]
סימנים וסימפטומים[עריכת קוד מקור | עריכה]

התסמונת הקרצינואידית מתרחשת בכ-5% מהגידולים הקרצינואידים ומתבטאת כאשר חומרים מכלי דם מהגידולים נכנסים למחזור הדם המערכתי ונמלטים מהסינון בכבד.
- הסמקה: הממצא הקליני החשוב ביותר הוא הסמקה של העור, בדרך כלל של הראש והחלק העליון של בית החזה.[4]
- שלשול : כאשר השלשול אינטנסיבי ונפיץ, הוא עלול להוביל להפרעות אלקטרוליטים והתייבשות .
- כאבי בטן : עקב תגובה דמופלסטית של המזנטריה או גרורות בכבד.[5]
- כיווץ ברנוכוסים: שעלול להיות מושרה על ידי היסטמין, משפיע על מספר קטן יותר של חולים ולעיתים מלווה את ההסמקה.
- קרדיומיופתיה מגבילה משנית: לכ 50% מהחולים יש אבנורמליות לבבית קלאסית מהסוג המגביל, הנגרמת על ידי סרוטונין הגורם לעיבוי וצילוק הרקמה האנדוקרמיומית של מסתם הלב, הנקרא פיברוזיס לבבי. התוצאה היא לב עם קצב וכיווץ תקינים, אך עם הפחתת המתיחה הראשונית של שרירי התאים והפחתת נפח הדם בחדרים בחלק הדיאסטולי.
פתופיזיולוגיה[עריכת קוד מקור | עריכה]
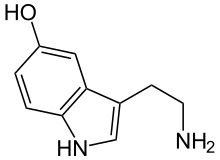
גידולים קרצינואידים מייצרים מספר חומרים מכלי דם פעילים, ובראשם סרוטונין. נהוג לחשוב שסרוטונין הוא הגורם להסמקה, אבל זה נכון רק חלקית.[6] ההסמקה נובעת גם מהפרשת קליקריין, האנזים המזרז את ההמרה של קינינוגן לליזיל-ברדיקינין. האחרון מומר עוד יותר לברדיקינין, אחד ממרחבי כלי הדם החזקים ביותר הידועים.
תסמינים נוספים של התסמונת הקרצינואידית הם שלשול (נראה שנגרם מהעלייה בסרוטונין, המגביר מאוד את הפריסטלטיקה, ומשאיר פחות זמן לספיגת נוזלים), תסמונת דמוית פלגרה (כנראה נגרמת מהסטה של כמויות גדולות של טריפטופן מסינתזה של ויטמין B 3 ניאצין, הדרוש לייצור NAD, לסינתזה של סרוטונין וחומרים אחרים), נגעים פיברוטיים של האנדוקרדיום, במיוחד בצד ימין של הלב וכתוצאה מכך אי ספיקה של המסתם התלת-צדדי, ובתדירות נמוכה יותר, גם של השסתום הריאתי, ובאופן נדיר, גם כיווץ סימפונות.
הביולוגיה של גידולים אלו שונה מסוגי גידול רבים אחרים. מחקר מתמשך על הביולוגיה של גידולים אלו עשוי לחשוף מנגנונים חדשים להתפתחות הגידול.[7]
אבחנה[עריכת קוד מקור | עריכה]

כאשר יש מידה מסוימת של חשד קליני, הבדיקה הראשונית השימושית ביותר היא בדיקת רמות השתן של 5-HIAA, התוצר הסופי של חילוף החומרים של סרוטונין, במשך 24 שעות.[5] חולים עם תסמונת קרצינואידית מפרישים בדרך כלל יותר מ-25 מ"ג של 5-HIAA ליום.
הדמיה[עריכת קוד מקור | עריכה]
עבור מציאת של נגעים ראשוניים וגרורות כאחד, ההדמיה הראשונית היא בבדיקות הדמיה מיוחדות המשתמשות בתכונה נוספת של התאים הנוירואנדוקריניים - ביטוי קולטנים לסומטוסטטין. שיעורי הזיהוי החציוניים עם בדיקה זו הם כ-89%, בניגוד לטכניקות הדמיה אחרות כמו סריקת CT ו-MRI עם שיעורי זיהוי של כ-80%.
בדרך כלל, בבדיקת CT נראה שינוי דמוי עכביש/סרטן במזנטריה עקב הפיברוזיס משחרור הסרוטונין. בדיקת F-FDG PET/CT אשר מעריכה את חילוף החומרים המוגבר של גלוקוז, עשוי גם לסייע באיתור הנגע הקרצינואידי או בהערכת גרורות.
מיקום הגידול[עריכת קוד מקור | עריכה]
מציאת מיקום הגידול עשויה להיות קשה ביותר. [דרוש מקור] בליעת בריום ובדיקת מעקב של המעי עשויות להראות לעיתים את הגידול. צורה נוספת של לוקליזציה של גידול היא האוקטרוסקן. חומר מעקב של אינדיום 111 מוזרק לווריד ואז הגידולים סופגים החומר ונראים בסורק. רק הגידולים סופגים את חומר הסומטוסטטין אינדיום 111 מה שהופך את הסריקה ליעילה ביותר.
אפשרויות טיפול[עריכת קוד מקור | עריכה]
להקלה סימפטומטית של תסמונת קרצינואיד: [דרוש מקור]
- נוגדי הורמני גדילה (אוקטראוטיד) -אנלוג לסומטוסטטין שמפחית את הפרשת הסרוטונין על ידי הגידול, ובאופן משני, מקטין את תוצר הפירוק של סרוטונין (5-HIAA)
- טלוטריסטאט אתיל יחד עם אנלוגי סומטוסטטין בחולים שאינם מגיבים למונותרפיה אנלוגית סומטוסטטין.[8] זהו מעכב טריפטופן הידרוקסילאז ומפחית את ייצור הסרוטונין.[9]
- טיפול ברדיונוקלידים לקולטן פפטיד (PRRT) עם לוטטיום-177, איטריום-90 או אינדיום-111 המסומן כאוקטרוטאט יעיל ביותר
- Cyproheptadine (תרופה אנטי-היסטמינית עם השפעות אנטי- סרטונרגיות)
טיפול חלופי למטפולים מתאימים:
- כריתה כירורגית של גידול וכימותרפיה
- כימותרפיה אנדווסקולרית, כימואמבוליזית, ממוקדת המועברת ישירות לכבד באמצעות צנתרים מיוחדים המעורבים עם חרוזים תסחיפים (חלקיקים החוסמים כלי דם), המשמשים לחולים עם גרורות בכבד .
אי ודאות[עריכת קוד מקור | עריכה]
קשה לקבוע את התקדמות המחלה מכיוון שהמחלה יכולה לשלוח גרורות בכל מקום בגוף ויכולה להיות קטנה מכדי להזדהות עם כל טכנולוגיה עדכנית.
פרוגנוזה[עריכת קוד מקור | עריכה]
הפרוגנוזה משתנה מאדם לאדם. הפרוגנוזה נעה בין 95% הישרדות של 5 שנים למחלה מקומית ל-80% הישרדות של 5 שנים עבור אלו עם גרורות בכבד. זמן ההישרדות הממוצע מתחילת הטיפול באוקטריאוטיד עלה לכ-12 שנים.[10]
ראו גם[עריכת קוד מקור | עריכה]
לקריאה נוספת[עריכת קוד מקור | עריכה]
- Kvols, L. K., Moertel, C. G., O'Connell, M. J., Schutt, A. J., Rubin, J., & Hahn, R. G. (1986). Treatment of the malignant carcinoid syndrome. New England Journal of Medicine, 315(11), 663-666.
- Mabvuure, N., Cumberworth, A., & Hindocha, S. (2012). In patients with carcinoid syndrome undergoing valve replacement: will a biological valve have acceptable durability?. Interactive cardiovascular and thoracic surgery, 15(3), 467-471.
קישורים חיצוניים[עריכת קוד מקור | עריכה]
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 Pandit, S; Annamaraju, P; Bhusal, K (בינואר 2020). Carcinoid Syndrome. PMID 28846309.
{{cite book}}: (עזרה) - ^ Shields, Thomas W.; LoCicero, Joseph; Reed, Carolyn E.; Feins, Richard H. (2009). General Thoracic Surgery (באנגלית). Lippincott Williams & Wilkins. p. 1540. ISBN 978-0-7817-7982-1.
- ^ Norton, Jeffrey; Bollinger, R. Randall; Chang, Alfred E.; Lowry, Stephen F. (2012). Surgery: Basic Science and Clinical Evidence (באנגלית). Springer. p. 852. ISBN 978-3-642-57282-1.
- ^ "Carcinoid syndrome: a statistical evaluation of 748 reported cases". Journal of Experimental & Clinical Cancer Research. 18 (2): 133–41. 1999. PMID 10464698.
- ^ 1 2 Anezka C. Rubin de Celis Ferrari, João Glasberg, Rachel P. Riechelmann, Carcinoid syndrome: update on the pathophysiology and treatment, Clinics 73, 2018-08-20 doi: 10.6061/clinics/2018/e490s
- ^ Papaliodis, Dean, et al.
- ^ "The biological hallmarks of ileal carcinoids". European Journal of Clinical Investigation. 41 (12): 1353–60. 2011. doi:10.1111/j.1365-2362.2011.02537.x. PMID 21605115.
- ^ "FDA Approves Xermelo for Carcinoid Syndrome Diarrhea" (באנגלית). U.S. Food and Drug Administration. 28 בפברואר 2017. נבדק ב-1 במרץ 2017.
{{cite news}}: (עזרה) - ^ "Xermelo (telotristat ethyl) Tablets, for Oral Use. Full Prescribing Information" (PDF). Lexicon Pharmaceuticals, Inc. 8800 Technology Forest Place. The Woodlands, TX 77381. נבדק ב-1 במרץ 2017.
{{cite web}}: (עזרה) - ^ S.-M. Sjöblom, Clinical Presentation and Prognosis of Gastrointestinal Carcinoid Tumours, Scandinavian Journal of Gastroenterology 23, 1988-01-01, עמ' 779–787 doi: 10.3109/00365528809090760
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.
