גליובלסטומה מולטיפורמה – הבדלי גרסאות
| שורה 5: | שורה 5: | ||
[[קובץ:Glioblastoma_-_MR_sagittal_with_contrast.jpg|ממוזער| [[דימות תהודה מגנטית|MRI]]<nowiki/>עם חומר ניגוד שמדגים GBM בנער בן 15.]] |
[[קובץ:Glioblastoma_-_MR_sagittal_with_contrast.jpg|ממוזער| [[דימות תהודה מגנטית|MRI]]<nowiki/>עם חומר ניגוד שמדגים GBM בנער בן 15.]] |
||
[[קובץ:Glioblastoma_(1).jpg|ממוזער|גליובלסטומה ]] |
[[קובץ:Glioblastoma_(1).jpg|ממוזער|גליובלסטומה ]] |
||
הסימנים והסימפטומים של המחלה רבים ושונים, ותלויים במיקום הגידול, ויכולים לנבוע הן מהגידול עצמו והן מהטיפולים שכן אלו וגם אלו משפיעים ישירות על המוח עצמו. התסמינים יהיו נוירולוגים, קוגנטיביים ולעתים אף פסיכיאטרים. ביניהם פירכוסים, בחילות והקאות, כאבי ראש, אובדון זיכרון והמיפרזיס (חולשה בחלק אחד של הגוף). סימפטומים פסיכיאטרים עלולים לכלול פסיכוזות הלוצינציות, שינויי מצב רוח ושינויי אישיות, שיידרשו, כתלות בחומרתם, טיפול פסיכיאטרי או תרופתי. כיוון שחלקים שונים של המוח אחראים על תפקודים שונים, הסימפטומים יהיו במקרים רבים תלויי גידול. למשל, חולים עם גידול באונה הקדמית דיווחו יותר על חוסר עכבות וקשיי שיפוט מחולים אחרים. {{הערה|{{צ-מאמר |
|||
| ⚫ | |||
|מחבר=Florien W Boele, Alasdair G Rooney, Robin Grant, and Martin Klein1 |
|||
|שם=Psychiatric symptoms in glioma patients: from diagnosis to management |
|||
|כתב עת=Neuropsychiatr Dis Treat |
|||
|כרך= |
|||
|עמ= |
|||
|מו"ל= |
|||
|שנת הוצאה=2015 |
|||
|קישור=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4467748/ |
|||
|doi=10.2147/NDT.S65874}}}} |
|||
| ⚫ | התסמינים יכולים להופיע מיד, אך לעתים הגידול יגיע למימדים גדולים מאד טרם יופיע תסמינים כלשהם. ככל שהמחלה מתקדמת, מחמירים התסמינים. רוב המטופלים יסבלו בשלב כלשהו בקשיי תנועה והמיפרזיס, כמו גם קשיי תקשורת כאלו או אחרים ובלבול. התסמינים השכיחים ביותר בחודש האחרון לחיים היו הפרעות בליעה (85%), ישנוניות (85%), כאבי ראש (36%), פרכוסים (30%) ובלבול/דילריום (15%).{{הערה|{{צ-מאמר|מחבר=Esther Lin, Mark A. Rosenthal, Brian H. Le, and Peter Eastman|שם=Neuro-oncology and palliative care: a challenging interface|כתב עת=Neuro Oncol|כרך=|עמ=2012 Sep; 14|מו"ל=|שנת הוצאה=|קישור=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3480249/}}}} קשיי התקשורת ושינויי האישיות המופיעים במקרים רבים במטופלים אלו מהווים אתגר קשה למטופלים, למטפלים ולבני משפחותיהם. |
||
== גורמי סיכון == |
== גורמי סיכון == |
||
גרסה מ־00:12, 25 באוקטובר 2016
 |
דף זה אינו ערך אנציקלופדי
| |
| דף זה אינו ערך אנציקלופדי | |
גליובלסטומה מולטיפורמה, נקראת גם אסטרוציטומה שלב 4, ידוע גם בקיצור GBM, הוא סרטן המוח הנפוץ והאגרסיבי ביותר. הסמינים והסימפטומים תחילה אינם ספציפים. הם עשויים לכלול כאבי ראש, שינויים באישיות, בחילות וסימפטומים הדומים לאלו של שבץ. לעתים ההחמרה בסימפטומים היא מהירה, והם יכולים להתקדם עד לחוסר הכרה. גליובלסטומה מהווה 15.4% מכלל גידולי המוח הראשוניים בכלל ו-45.6% מכלל גידולי המוח הממאירים הראשוניים. ברוב המקרים הגורם אינו יודע. הפרוגנוזה של גידול זה גרועה: שיעורי ההישרדות הם בערך כ-12-15 חודשים לאחר האבחנה, כשפחות מ-3%-5% שורדים יותר מחמש שנים. ללא טיפול, ההישרדות היא בדרך כלל 3 חודשים. f-3 אנשים מתוך 100,000 מפתחים את המחלה בשנה. במקרים נדירים יכול להופיע סוג סרטן זה גם בחוט השדרה.
סימנים וסימפטומים
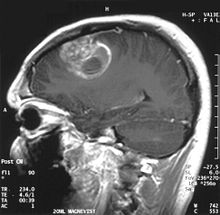

הסימנים והסימפטומים של המחלה רבים ושונים, ותלויים במיקום הגידול, ויכולים לנבוע הן מהגידול עצמו והן מהטיפולים שכן אלו וגם אלו משפיעים ישירות על המוח עצמו. התסמינים יהיו נוירולוגים, קוגנטיביים ולעתים אף פסיכיאטרים. ביניהם פירכוסים, בחילות והקאות, כאבי ראש, אובדון זיכרון והמיפרזיס (חולשה בחלק אחד של הגוף). סימפטומים פסיכיאטרים עלולים לכלול פסיכוזות הלוצינציות, שינויי מצב רוח ושינויי אישיות, שיידרשו, כתלות בחומרתם, טיפול פסיכיאטרי או תרופתי. כיוון שחלקים שונים של המוח אחראים על תפקודים שונים, הסימפטומים יהיו במקרים רבים תלויי גידול. למשל, חולים עם גידול באונה הקדמית דיווחו יותר על חוסר עכבות וקשיי שיפוט מחולים אחרים. [1]
התסמינים יכולים להופיע מיד, אך לעתים הגידול יגיע למימדים גדולים מאד טרם יופיע תסמינים כלשהם. ככל שהמחלה מתקדמת, מחמירים התסמינים. רוב המטופלים יסבלו בשלב כלשהו בקשיי תנועה והמיפרזיס, כמו גם קשיי תקשורת כאלו או אחרים ובלבול. התסמינים השכיחים ביותר בחודש האחרון לחיים היו הפרעות בליעה (85%), ישנוניות (85%), כאבי ראש (36%), פרכוסים (30%) ובלבול/דילריום (15%).[2] קשיי התקשורת ושינויי האישיות המופיעים במקרים רבים במטופלים אלו מהווים אתגר קשה למטופלים, למטפלים ולבני משפחותיהם.
גורמי סיכון
מסיבות לא ידועות, הגליובלסטומה מתרחשת יותר בקרב גברים.רוב מקרי הגליובלסטומה מופיעים ללא כל נטייה גנטית. לא נמצא קשר בין גליובלסטומה לעישון, צריכת בשר מעובד או חשיפה לשדות אלקטרו-מגנטיים. ייתכן שיש קשר בין הגידול לבין צריכת אלכוהול (מקור). ייתכן שיש קשר נמוך בין קרינה מניינת וגליובלסטומה. אנליזה מ-2006 הראתה קשר בין סרטן המוח לחשיפה לעופרת במקום עבודה.
גורמי סיכון נוספים:
- מין: גברים.
- גיל: מעל גיל 50.
- מוצא: לבנים, היספנים ואסיאתים.
- אסטרוציטומה מדרגה נמוכה אשר עשויה, לעתים קרובות, להתפתח לגידול בדרגה גבוהה יותר.
- המחלות הגנטיות הבאות קשורות עם שכיחות גבוהה יותר של גליומות: נוירופיברומטוזיס, תסמונת לי פרומני, תסמונת טורקוט, טרשת גבשושית ותסמונת ון-היפל לינדאו.
אפדימיולוגיה
השכיחות של סרטן זה עולה עם הגיל, כשהשיא הוא בין הגילאים 75-84.
פתוגנזה
אבחון

ברוב המקרים הגורם אינו יודע. גורמי סיכון נדירים הם הפרעות גנטיות כמו נוירופיברומטוזיס, תסמונת לי פראומני וכן טיפולים רדיותרפים (הקרנות). הגידול יכול להתפתח מתא נורמלי במוח, או מתאי אסטרוציטומה בשלב נמוך יותר שעברו מוטציה. האבחון נעשה בדרך כלל על ידי שילוב בדיקת CT, MRTI וביופסיה.
שיעורי ההישרדות הם בערך כ12-15 חודשים לאחר האבחנה, כשפחות מ-3%-5% שורדים יותר מחמש שנים. ללא טיפול, ההישרדות היא בדרך כלל 3 חודשים. 3 אנשים מתוך 100,000 מפתחים את המחלה בשנה. .
סימנים וסימפטומים
הסימנים והסימפטומים של המחלה רבים ושונים, ותלויים במיקום הגידול. ביניהם פירכוסים, בחילות והקאות, כאבי ראש, אובדון זיכון והמיפרזיס (חולשה בחלק אחד של הגוף). כמו כן, עלולים להופיע שינויי אישיות, בעיות זיכרון וחסרים נוירולוגים בעקבות מעורבות של האונה הטמפורלית והאונה הקדמית. התסמינים יכולים להופיע מיד, אך לעתים הגידול יגיע למימדים גדולים מאד טרם יופיע תסמינים כלשהם.
חשוב להבחין בין גליובלסטומה ראשונית לגליובלסטומה משנית, גידולים המתפתחים באופן ספונטני או גידולים המתפתחים מגליומות בדרגה נמוכה, בהתאמה. לגליובלסטומה ראשונית יש את הפרגנוזה הגרועה ביותר, וההבחנה ביניהם חשובה לקביעת סוג הטיפול. מעל 80% מגליובלסטומות משניות נושאות מוטציה בגן IDH1, מוטציה שנדירה בגליובלסטומות ראשוניות (5%-10%). כך שמוטציה זו מהווה כלי שימושי לאבחון סוג הגידול משום שמבחינה היסטולוגית הגידולים דומים מאד, ואבחנה ללא סמנים ביולוגים מולוקולריים לא אמינה.
טיפול
הטיפול בגידול קשה בשל כמה סיבות: תאי הגידול עמידים מאד בפני הטיפולים הקונבנציונליים, המוח רגיש מאד לטיפולים, ועלול להינזק מהם, המוח מוגבל מאד ביכולת שלו לטפל בעצמו, תרופות רבות אינן מסוגלות לחצות את מחסום דם-מוח. טיפולים בגידול הראשוני ובגרורות מוחיות כוללים הן טיפול בסימפטומים והן טיפול פליאטיבי.
טיפול סימפטומטי
טיפול זה מתמקד בהקלה על התסמינים ושיפור איכות חייו של המטופל על ידי תרופות אנטי-אפלפטיות וכקורטיקוסטרואידים.
- היסטורית, כ-90% מהמטופלים עם גליובלסטומה קיבלו טיפול אנטי-אפילפטי, למרות שההערכה היא שרק 40% מהמטופלים נדרשו באמת לטיפול זה. תופעת יתר של הקרנות יחד עם קבלת פניטואין הם תגובות קשות בעור כמו אריתמה מולטיפורמה ותסמונת סטיבן-ג'ונסון.
- הסטרואידים שיתנו יהיו בדרך כלל דקסמתזון, במטרה להפחית בצקת, הפחתת לחץ תוך-גולגולתי מה שיכול להפחית את כאבי הראש או נטייה לנמנום. .
טיפול פליאטיבי
מטרת הטיפול הפליאטיבי הוא שיפור איכות החיים והארכתם. טיפול זה יכול לכלול ניתוח (עם שוליים נקיים ככל הניתן), הקרנות וכימותרפיה. כריתה מלאה של הגידול מזוהה עם פרוגנוזה טובה יותר.
ניתוח
הניתוח הוא השלב הראשון של הטיפול של גליובלסטומה. יתרונות הניתוח כוללים כריתה עבור אבחנה פתולוגית, הקלה של התסמינים וכן הסרת המחלה טרם פיתוח עמידות להקרנות וכימותרפיה.
ככל שהיקף הגידול המוסר גדול יותר, כך הפרוגנוזה טובה יותר. הסרה של 98% או יותר מהגידול קשורה באופן משמעותי עם איכות חיים טובים יותר. הסיכויים של הסרה כמעט מוחלטת של הגידול גדלים אם הניתוח מונחה על ידי צבע פלואורסצנטי בשם חומצה אמינולבולינית-5. תאי הגידול בעת האבחנה מפוזרים באופן נרחב במוח, כך שגם במקרים של כריתה מוחלטת של הגידול הוא בדרך כלל יחזור ויופיע ליד האתר המקורי או במקומות רחוקים יותר במוח. המטופל יקבל הקרנות וכימותרפיה במאמץ לדכא ולהאט חזרה של המחלה. עם ניתוח בלבד, שיעור ההישרדות החציוני עומד על שישה חודשים.
הקרנות
טיפול רדיותרפי לאחר ניתוח הפך לטיפול הסטנדרטי בגליובלסטומה מאז שנות השבעים. טיפול זה ניתן בדרך כלל עם טמודל. מחקר משמעותי שנערך בשנות השבעים הראה שבקרב 303 מטופלים עם GBM שחולקו באופן רנדומלי, אורך החיים החציוני בקרב אלו שקיבלו טיפול רדיותרפי היה כפול מאלה שלו. נחיצותו ויעילותו של טיפול זה הוכחו במחקרים רבים נוספים אחרים. בממוצע, מוריד הטיפול הרדיותרפי את גודל הגידול ל-107 תאים. הטיפול המקובל הוא טיפול במינון של עד 60 Gy.
אף כי התאים הסרטניים רגישים יותר לקרינה, גם תאי המוח הרגילים עלולים להינזק במהלך טיפול. נזק כזה, אם קורה, יהיה בדרך כלל קל, וישפיע על החדות הקוגנטיבית והיכולת לחשוב ולבצע משימות מורכבות. תופעות לוואי מהסוג הזה עלולות להחמיר ככל ששדה הקרינה גדול יותר וממושך יותר ונוטה להחמיר עם הזמן. תופעות לוואי אלו נוגעות יותר לאנשים ששורדים כמה שנים לאחר ההקרנות, מה שאינו קורה בדרך כלל בגליובלסטומה. נוסף לכך, קרינה יכולה להשפיע גם על מאזן ההורמונים בגוף ותופעות הלוואי הכרוכות בשינוי מאזן זה.
כימותרפיה
הטיפול הסטנדרטי בגידול זה הוא טיפול רדיותרפי יחד עם טמוזולומיד, המוכרת בשם המסחרי שלה - טמודל. זוהי תרופה ציטוטוקסית שמשתייכת לתכשירי אלקילציה שנכנסה לשימוש בשנת 2000. ייחודה של תרופה זו בניגוד לתרופות כימותרפיות אחרות היא יכולתה לחדור לרקמת המוח ולגידול. הטיפול נעשה דרך הפה וסבילותו בדרך כלל טובה.
מחקר גדול של 575 משתתפים הראה כי מטופלים שקיבלו טיפול רדיותרפי יחד עם טמודל שרדו 14.6 חודשים, לעומת 12.1 חודשים במטופלים שקיבלו הקרנות בלבד. בקרב אותם מטופלים, שיעורי ההישרדות לאחר 24 חודשים היו 26.5% בטיפול המשולב לעומת 10.4% בטיפול הקרינתי בלבד. מחקר המשכי שנערך לאחר 5 שנים הראה שיתרון ההישרדות שהודגם לאחר שנתיים המשיך גם לאחר מכן: לאחר ארבע שנים שרדו 12.1% מהחולים שטופלו בטיפול המשולב לעומת 3% שקיבלו טיפול קרינתי בלבד.[3] בעבודה שניתחה באמצעות מטא-אנליזה את תוצאותיהם של 12 מחקרים שגייסו יותר מ-3,000 חולים לצורך השוואה פרוספקטיבית אקראית של זרועות הטיפול, הוכח שטיפול כימי שיפר את ההישרדות ב-6% בתום שנה מהאבחנה, נתון שהיה בעל משמעות סטטיסטית מובהקת.[4] הטיפול הכימי הביא להארכת חציון ההישרדות בחודשיים ימים כיום הטיפול הסטנדרטי בסוג סרטן זה הוא הקרנות יחד עם טמודל. נראה כי הטמודל מגביר את הרגישות של תאי הגידול לקרינה. מנות גבוהות של טמודל אינן מעלות משמעותית את הרעילות שלו, אך היעילות של מינונים גבוהים יותר אינה גבוהה יותר ממינון סטנדרטי.
טיפול אנטי-אנגיוגני
כמו בגידולים רבים אחרים, גם במקרה של גליובלסטומה מתמקד המחקר בתרופות ביולוגיות "חכמות". את התוצאות המבטיחות ביותר עבור סוג זה של סרטן השיגה בבקיזומב אווסטין, המוכרת יותר בשמה אווסטין. זוהי תרופה אנטי סרטנית הפוגעת ביכולתו של הגידול הסרטני ליצור כלי דם - אנגיוגנזה. במחקר שנערך על 167 חולים הודגמה תוצאה של 42.6% PFS-6 (שישה חודשים ללא התקדמות המחלה), זאת בהשוואה ל-9% המקובל בטיפולי קו שני ושלישי בגידול. מחקרים שנעשו על טיפול באווסטין בגליובלסטומה ראשונית הראו הארכה משמעותית ב-PFS, אך לא נמצא שינוי משמעותי בהישרדות כוללת (Overall Survival). הסבר אפשרי לשוני בין הנתונים הללו הוא שהגידול מפתח עמידות לתרופה או שכלי הדם גדלים במהירות לאחר סיום הטיפול. בנוסף, חלה במטופלים ירידה נוירו-קוגנטיבית, הוחמרו תסמינים נוירולוגיים ונצפתה ירידה באיכות החיים לאורך זמן. עם זאת, המחקר על התרופה זו עוד לא הגיע לידי מיצויו, ונכון ל-2016, מחקרים רבים עודם בעיצומם.[5] [6]
פרוגנוזה
קישורים חיצוניים
- גליובלסטומה - הווה ועתיד, פרופ' טלי סיגל, גב‘ עדנה שלום, באתר Medical Media.
מקורות
{{cite journal}}: (עזרה)*הערות שוליים
- ^ Florien W Boele, Alasdair G Rooney, Robin Grant, and Martin Klein1, Psychiatric symptoms in glioma patients: from diagnosis to management, Neuropsychiatr Dis Treat, 2015 doi: 10.2147/NDT.S65874
- ^ Esther Lin, Mark A. Rosenthal, Brian H. Le, and Peter Eastman, Neuro-oncology and palliative care: a challenging interface, Neuro Oncol, עמ' 2012 Sep; 14
- ^ Stupp, Roger; Mason, Warren P.; Van Den Bent, Martin J.; Weller, Michael; Fisher, Barbara; Taphoorn, Martin J.B.; Belanger, Karl; Brandes, Alba A.; et al. (2005). "Radiotherapy plus Concomitant and Adjuvant Temozolomide for Glioblastoma". New England Journal of Medicine. 352 (10): 987–96. doi:10.1056/NEJMoa043330. PMID 15758009.
- ^ Stewart LA. Chemotherapy in adult high-grade glioma: a systematic review and meta-analysis of individual patient data from 12 randomised trials. Lancet 2002;359:1011-1018
- ^ Peng Fu, Yun-Song he, Qin Huang, Tao Ding, Yong-cun Cun, Hong-Yang Zhao, and Xiang Wei, Bevacizumab treatment for newly diagnosed glioblastoma: Systematic review and meta-analysis of clinical trials, Mol Clin Oncol מיקום בסדרה doi: 10.3892/mco.2016.816
- ^ Mark R. Gilbert, M.D., James J. Dignam, Ph.D., Terri S. Armstrong, Ph.D., A.N.P.-B.C., Jeffrey S. Wefel, Ph.D., Deborah T. Blumenthal, M.D., Michael A. Vogelbaum, M.D., Ph.D., Howard Colman, M.D., Ph.D., Arnab Chakravarti, M.D., Stephanie Pugh, Ph.D., Minhee Won, M.A., Robert Jeraj, Ph.D., Paul D. Brown, M.D., Kurt A. Jaeckle, M.D., David Schiff, M.D., Volker W. Stieber, M.D., David G. Brachman, M.D., Maria Werner-Wasik, M.D., Ivo W. Tremont-Lukats, M.D., Erik P. Sulman, M.D., Kenneth D. Aldape, M.D., Walter J. Curran, Jr., M.D., and Minesh P. Mehta, M.D., A Randomized Trial of Bevacizumab for Newly Diagnosed Glioblastoma, The New England Journal Of Medicine, February 20, 2014 doi: 10.1056/NEJMoa1308573
