מולה (אנטומיה)
 | |
| תחום |
פתולוגיה |
|---|---|
| מיקום אנטומי |
רירית הרחם |
| טיפול |
dactinomycin |
| קישורים ומאגרי מידע | |
| eMedicine |
254657 |
| MeSH | D006828 |
| סיווגים | |
| ICD-11 |
JA02 |

מחלות טרופובלסטיות הריוניות (Gestational trophoblastic diseases) הן גידולים שמקורם בהפריה לא תקינה של ביצית וזרעונים, המתפתחים ברחם באופן אבנורמלי. מולה הידטידיפורמית (ידועה כ- "מולה") היא הצורה השכיחה ביותר של מחלות אלו, והיא מתרחשת יותר אצל נשים הצעירות יותר מגיל 20 או המבוגרות יותר מגיל 40. הסיבה להיווצרותה של מולה יכולה להיות הפריה של ביצית ושני זרעונים או זרעון שעבר הכפלה, באופן בו הביצית המופרית איננה מכילה עובר אלא חלקי עובר וחלקי שליה. התסמינים הקליניים כוללים במרבית המקרים דימום בטרימסטר ראשון, רחם הגדל במהירות וגדול יחסית לשבוע ההריון, רמות BetaHCG גבוהות מאוד ולעיתים תופעות מוקדמות של רעלת היריון המתחילות בטרימסטר הראשון. הטיפול במולה הוא שאיבה וריקון של תוכן הרחם ומעקב, היות שחלק מן המולות נוטות להיות פרסיסטנטיות ואף להפוך ממאירות- במקרים כאלו, הטיפול הוא מתן כימותרפיה. יצוין, כי גם כאשר הגידולים הללו שולחים גרורות, הרי שבטיפול נכון שיעור הריפוי עומד על כ־90%, ולכן קיימת חשיבות לערוך בדיקות BetaHCG לנשים שבעברן היריון מולרי, הפלה, או היריון רגיל, אשר מתלוננות על דימום ווגינלי או הימצאות של גידול במקום כלשהו בגוף, אשר עלול לרמז על גרורות.
אופן היווצרות גידולים טרופובלסטיים[עריכת קוד מקור | עריכה]
מולה מחולקת לשני סוגים- מולה שלמה ומולה חלקית.
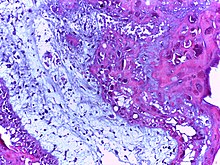
- מולה שלמה נובעת כתוצאה מהפריה בין ביצית ללא מטען גנטי (empty ovum) יחד עם זרעון שעבר דופליקציה או שני זרעונים, כאשר המטען הגנטי הנוצר הוא 46XY או 46XX (דיפלויד). במולה שלמה אין חלקי עובר או כדוריות דם עובריות, רמות ה- BetaHCG הן לרוב גבוהות מאוד (מעל 50,000), והסיכון למולה פרסיסטנטית נע בין 20% ל-30%. התלונות הקליניות נפוצות מאוד במקרים של מולה שלמה. המקרה באולטראסאונד של מולה שלמה כולל מראה של "סופת שלג" המבטא מספר מוקדים היפו-אקואיים, ללא יכולת להבחין בשק היריון או בעובר. כמו כן לעיתים ניתן להבחין בציסטות שחלתיות הקרויות theca lutein cysts, אשר נמצאות בשכיחות גבוהה יותר במקרים אלו. בפתולוגיה, המראה של מולה שלמה הוא כשל שלפוחיות דמויות ענבים הממלאות ומרחיבות את הרחם, בהיעדר של רקמה עוברית.
- מולה חלקית נובעת כתוצאה מהפריה בין ביצית עם מטען גנטי (הפלויד) יחד עם זרעון שעבר דופליקציה או שני זרעונים, כאשר המטען הגנטי הנוצר הוא 69XXY (ב־70% מהמקרים), 69XXX (ב־27% מן המקרים) וב-3% מהמקרים 69XYY (טריפלויד). מולה חלקית מכילה חלקי עובר וכדוריות דם עובריות, רמות BetaHCG נמוכות יותר מאשר במולה שלמה, וסיכוי של פחות מ- % 5 להפוך למולה פרסיסטנטית. המראה באולטראסאונד של מולה חלקית כולל אזורים מקומיים בהם יש שינויים טרופובלסטיים ולעיתים ניתן להבחין ברקמה עוברית.
סוגי גידולים טרופובלסטיים[עריכת קוד מקור | עריכה]
- מולה הידטידיפורמית (hydatidiform mole) כמפורט לעיל, אשר יכולה להיות שלמה או חלקית, היא הצורה השכיחה ביותר והשפירה של מחלות טרופובלסטיות. הסיכון למולה מוגבר אצל נשים בגילאי קיצון (מתחת ל-20, מעל 40), אצל נשים שטרם ילדו, נשים ממעמד סוציואקונומי נמוך, ונשים שהתזונה שלהם חסרה בקרוטן, חומצה פולית ופרוטאינים. קבוצת סיכון מעניינת שהראתה סיכוי של פי 10 לפתח את המחלה הן נשים מסוג דם A אשר הרו לגברים עם סוג דם O (בעיקר סיכון לפתח כוריוקרצינומה). יש לחשוד במולה בכל אישה המדממת במהלך המחצית הראשונה של ההריון, במצבים של פליטת שלפוחיות רחמיות מהנרתיק המהוות חלק מן המולה, במצבים של הקאות קשות במהלך ההריון או במצבים בהם החלה רעלת היריון טרם שבוע 24. חוסר אבחון לב עוברי באולטראסאונד, ורחם הגדול מדי לגיל ההריון המשוער, יכולים לתמוך באבחנה. רמות BetaHCG וביצוע אולטראסאונד הן הכרחיות לצורך האבחנה כי מדובר במולה.
- מולה חודרנית (או אינווסיבית) מדווחת בכ־10% עד 15% מן המקרים של היריון מולרי, והיא עלולה להביא להתפתחות של גרורות. מולה חודרנית מדווחת בכ־20% מן המקרים של מטופלות אשר עברו ריקון של הרחם לאחר היריון מולרי. זוהי למעשה מולה, אשר חדרה לשריר הרחם (מיומטריום) ולאיברים קרובים, והיא עלולה אף להביא לקרע של הרחם ולדימום תוך בטני. עם זאת, היא יכולה לעבור רגרסיה ספונטנית.
- כוריוקרצינומה- זהו גידול ממאיר ממשפחת המחלות הטרופובלסטיות, והוא נדיר יחסית (קיים בכ־2% עד 5% מסך המקרים של מחלות טרופובלסטיות). רבע מהמקרים הללו מתרחשים לאחר היריון במועד ורבע מתרחשים לאחר ביצוע הפלה. זהו גידול אפיתליאלי, אשר לרוב מתייצג כדימום ווגינלי מאוחר בתקופת משכב הלידה (לאחר הלידה).
- גידול שמקורו בשליה, או placental site trophoblastic tumor, ובראשי תיבות- PSTT, הוא גידול נדיר מאוד והוא לרוב מוגבל לרחם וגורם לגרורות יחסית מאוחר. גידול זה לא מפריש BetaHCG אלא HPL. גידול זה מקורו בשליה, והוא יכול להתרחש בכל סוג של היריון או להתייצג חודשים ואף שנים לאחר היריון. הטיפול בגידול זה הוא לרוב כריתת רחם, היות שהוא אינו מגיב לכימותרפיה באופן טוב.
סימנים קליניים[עריכת קוד מקור | עריכה]
- דימום רחמי, לרוב במהלך הסמסטר הראשון להריון, הוא התסמין העיקרי אשר אופייני לקיום של מולה, והוא מתרחש אצל יותר מ-90% מהנשים עם הריונות מולריים.
- בחילות והקאות מדווחות בכ־14% עד 32% מן המקרים, כאשר בחלק מן המקרים ההקאות הן תכופות עד כדי צורך באשפוז.
- אצל כמחצית מהמטופלות גודל הרחם יהיה גדול יותר ממה שמצופה יחסית לשבוע ההריון. יצוין כי בכשליש מהמקרים, הרחם דווקא יראה קטן יותר מהמצופה.
- ציסטות שחלתיות מסוג theca lutein cysts קיימות בכ־15% עד 30% מן המקרים של הריונות מולריים, ולרוב מקושרות יותר למצבים כגון כוריוקרצינומה.
- רעלת היריון המתרחשת בטרימסטר הראשון היא ממצא אבנורמלי שאינו מתרחש לרוב בהריונות רגילים, ומהווה פעמים רבות אינדיקציה לכך שמדובר בהריון מולרי. רעלת היריון כאמור מתרחשת בכ־10%- 12% מההריונות המולריים.
- יתר פעילות של בלוטת התריס מתרחש בכ־10% מן המקרים, ומקושר לרצפטורים לתיירוטרופין המשופעלים על ידי BetaHCG. לרוב, זהו ממצא ללא סימנים קליניים או סאב קליני.
בדיקות מעבדה[עריכת קוד מקור | עריכה]
בדיקת המעבדה העיקרית היא בדיקת ההורמון BetaHCG, המשמש הן לאבחנה, הן לטיפול והן למעקב אחר המחלה. רמת הירידה בהורמון עצמו לאחר הטיפול אמורה לרדת בתוך 14 שבועות ממועד סיום ההריון.
טיפול במולה[עריכת קוד מקור | עריכה]
ראשית יש לאבחן שאכן מדובר במולה, וכן לבצע בדיקות דם מלאות, בדיקות תפקוד כבד וכליה וכן צילום חזה.
הטיפול עצמו כולל ריקון של הרחם- suction curettage. יש לתת אוקסיטוצין תוך וורידי לאחר הוצאת חלק נכבד מהרקמה לצורך כיווץ הרחם. יש לשלוח את הרקמה לפתולוגיה. ניתן לעשות שאיבה וריקון של הרחם גם כאשר הרחם הוא בגודל של 28 שבועות, אולם בכל מקרה בו הרחם גדול מ-12 שבועות יש להכין מראש ציוד לפתיחת בטן לכל מקרה של דימום בלתי נשלט. עד לשימוש הנוכחי כיום בשאיבה וריקון, ביצוע כריתת רחם היה האופציה בה בחרו להשתמש במקרים בהם הרחם היה גדול מ-12-14 שבועות. כיום כריתת רחם מומלצת רק במקרים בהם האישה סיימה את תוכניות הילודה וכן נשים מבוגרות יותר, אשר אצלן הסיכוי לממאירות גבוה יותר. הסיבוכים הכרוכים בפעולות אלו כוללים מעבר של חלקי רקמה ותאים דרך מחזור הדם השלייתי לשאר חלקי הגוף ובעיקר לריאות, המהוות את המקום הראשוני לשאריות תאים של הריונות מולריים. במרבית המקרים תהיה רגרסיה ספונטנית של רקמה זו, אולם בחלק מן המקרים עלולה להתפתח אי ספיקה נשימתית, המאופיינת כקוצר נשימה וכיחלון תוך 4-6 שעות לאחר ביצוע הריקון והשאיבה.
ביצוע מעקב[עריכת קוד מקור | עריכה]
מאחר שקיים סיכון לממאירות לאחר היריון מולרי, יש לעקוב בקפדנות אחר רמות BetaHCG החל מיומיים לאחר ביצוע השאיבה, ולאחר מכן מדי שבוע עד שלא ניתן לאתר רמות אלו בדם במשך שלוש בדיקות רצופות. (להלן- "תקופת המעקב"). אם במהלך תקופה זו קיימת רמיסיה ספונטנית בתוך 14 שבועות, או ש- BetaHCG איננו יורד ונכנס לפלטו, יש להמשיך ולחזור בכל חודש על רמות BetaHCG לפחות שנה מלאה. התקופה הקריטית לצורך מעקב אחר רמות BetaHCG היא בין שבוע 4-6 לאחר הריקון.
יש לערוך בדיקה גניקולוגית תוך שבוע ממועד השאיבה והריקון וכן להעריך את גודל הרחם ואיברים גניטליים נוספים למקרים של גרורות. יש לחזור על הבדיקה מדי 4 שבועות עד לתום תקופת המעקב.
במידה ותצלום חזה שהתבצע טרום השאיבה של ההריון המולרי הראה נוכחות לגרורות, יש לערוך צילומי חזה כל 4 שבועות עד להיעלמות ספונטנית של נגעים אלו, ולאחר מכן כל שלושה חודשים עד לתום תקופת המעקב.
קיימים כמה ממצאים קליניים המקושרים לעליה בסיכון לממאירות. באופן כללי, ככל שרמות BetaHCG גבוהות יותר וככל שהרחם גדול יותר, כך הסיכון לממאירות גבוה יותר. שילוב של ציסטות תקה-לוטאניות בשחלה ורחם מוגדל, מגדיל מאוד את הסיכון לממאירות.
יש לתת אמצעי מניעה (למשל, גלולות למניעת היריון) למשך תקופת המעקב, כאשר אישה אשר נכנסה לרמיסיה ספונטנית, ואשר הבדיקות כולן שליליות למשך שנה, יכולה להיכנס להריון מתום שנה זו.
האינדיקציות למתן כימותרפיה במהלך תקופת המעקב כוללות:
- עליה ברמות BetaHCG למשך שבועיים עוקבים או פלטו של BetaHCG במשך 3 שבועות.
- רמות BetaHCG אשר עולות בשבוע ה-15 שלאחר הריקון.
- רמות BetaHCG אשר עולות לאחר הגעתן לערכים נורמליים.
- דימום אשר מתרחש לאחר הריקון ואשר מרמז לממאירות.
- תוצאות מהפתולוגיה המצביעות על כך שמדובר בכוריוקרצינומה.
טיפול בממאירות[עריכת קוד מקור | עריכה]
מחלות טרופובלסטיות ממאירות יכולות להיות מולה חודרנית, כוריוקרצינומה, PSTT, או מצב בו לאחר היריון מולרי אין ירידה בערכי BetaHCG או שקיים פלטו בערכים אלו.
לאחר האבחנה כי מדובר בגידול ממאיר, יש חשיבות קריטית ללקיחת היסטוריה רפואית ולבדיקה גופנית. למרבית המטופלות יהיה רחם מוגדל ושחלות מוגדלות. יש לבחון אזורים בהן עלולות להיווצר גרורות, בעיקר במערכת המין הנשית התחתונה. יש לערוך צילום חזה וכן CT בטן ומוח. כמו כן יש לקחת בדיקות כלליות- הכוללות בדיקות דם, תפקודי קרישה, ותפקודי כבד וכליות אשר קריטיים לצורך הערכת הסיכון שבמתן תרופות כימותרפיות העלולות לפגוע בתפקוד איברים אלו. לאחר נטילת המידע האמור, ובמידה והאישה מעוניינת לשמור על פוריות, יש לבחור בטיפול הספציפי בהתאם.
ממאירות ללא גרורות[עריכת קוד מקור | עריכה]
מחלה ממאירה המוגבלת לרחם בלבד היא השכיחה ביותר מבין המחלות הממאירות הטרופובלסטיות. הטיפול במצב כזה הוא מתן מתוטרקסט כטיפול כימותרפי יחידני, או מתן אקטינומיצין במקום. תגובה מלאה לטיפול נעה בין 60% ל-98%, כאשר במקרים של חוסר תגובה או תופעות לוואי לא נסבלות, ניתנת כימותרפיה אלטרנטיבית. יש להמשיך בקבלת קורס נוסף של כימותרפיה לאחר תוצאות שליליות של BetaHCG. אין לתת מתוטרקסט במקרים של מחלת כבד או כאשר תפקוד הכליות אינו תקין. חלון הזמן בין כל טיפול הוא מינימום של 7 ימים ויש לעקוב אחר ספירת דם וספירת תאי דם לבנים. לרוב, ניתנים בממוצע 3-4 קורסים של טיפול. לאחר הטיפול והשגת רמיסיה, יש לערוך בדיקות BetaHCG למשך שנה, מדי חודש.
ממאירות עם גרורות[עריכת קוד מקור | עריכה]
הטיפול במחלה מטסטטית יכול להיעשות או על ידי מתן מתוטרקסט, בדומה לטיפול במחלה שאינה גרורתית, או טיפול כימותרפי משולב בכמה תרופות. כדי להעריך איזו מטופלת תזדקק לטיפול משולב, פותחו מספר כלים להערכת רמת הסיכון הגלומה בגידול עצמו:
- ה- National cancer institute בארצות הברית הציע שתי קטגוריות: לנשים הצפויות להיות עם פרוגנוזה טובה ונשים עם פרוגנוזה צפויה שאינה טובה. נשים עם פרוגנוזה צפוי טובה הן נשים שאצלן רמות ה- BetaHCG נמוכות מ-40,000, נשים שמתן הטיפול הכימותרפי החל בתוך 4 חודשים מתחילת המחלה, ונשים שהגרורות אצלן מוגבלות לריאות או לאגן. נשים אלו יגיבו באופן טוב לטיפול כמותרפי יחידני- מתוטרקסט. נשים עם פרוגנוזה שאינה טובה הן נשים עם רמות BetaHCG גבוהות מ-40,000, שהחלו טיפולים כימותרפיים יותר מ-4 חודשים לאחר פרוץ המחלה, ושנמצאו אצלן גרורות בכבד או במוח. כמו כן, נשים שהגידול החל אצלן לאחר סיום היריון הן נשים הנמצאות תחת קבוצה זו. קבוצה זו של נשים מציגה אתגר טיפולי, ויש לשקול אשפוז ממושך וטיפול כימותרפי משולב ולעיתים גם הקרנות. הטיפול המשולב היום אשר מניב שיעורי תגובה של 80%, הוא טיפול הקרוי EMACO, אשר כולל אטופסיד, מתותרקסט, אקטינומיצין, ציקלופוספמיד ו- וינקריסטין. רמיסיה מוחלטת מוגדרת רק כאשר שלוש תוצאות עוקבות של BetaHCG הן שליליות.
- ארגון הבריאות העולמי (WHO) הגדיר שיטת ניקוד המבוססת על גורמי סיכון ספציפיים של המטופלת, לרבות גיל, רמות BetaHCG, גודל הגידול, מספר הגרורות ומיקומן וכישלון טיפול כימותרפי קודם. לדוגמה, גיל מעל 40 מקבל נקודה אחת. הימצאות גרורות בכבד ובמוח שוות ערך ל-4 נקודות. ככל שהגידול החל מאוחר יותר מההריון הקודם, כך הניקוד גבוה יותר. ככל שיש יותר גרורות כך הניקוד גדול יותר, כשמעל 8 גרורות הניקוד הוא 4 נקודות וכן הלאה. ניקוד שבין 0-6 שווה ערך להגדרת המטופלת כבעלת פרוגנוזה טובה, בעוד שניקוד 7 ומעלה מגדיר אותה כבעלת פרוגנוזה שאינה טובה.
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.
