אלוסטריה
אָלוֹסְטֶרְיָה (באנגלית: Allostery) היא תכונה של אנזימים וחלבונים. תופעה זו מתרחשת כשמולקולה מסוימת (המכונה בהקשר זה אפקטור) נקשרת לאנזים או לחלבון, ומשנה את נטייתו להיקשר לסובסטרט (במקרה של אנזים) או לליגנד (במקרה של חלבון).
המילה נטבעה על ידי ז'אק מונו על בסיס היוונית (ἄλλος, אחר, ו-στερεὀς, (גוף) מוצק, במובן של עצם תלת-ממדי), כדי להתייחס להבדל במיקום המרחבי בין מקום קשירת האפקטור לבין מקום קשירתו של הסובסטרט או הליגנד.[1]
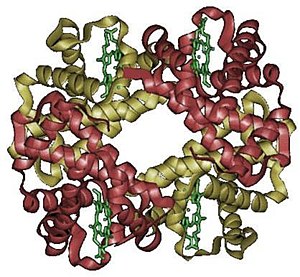
המוגלובין, אחד החלבונים הנפוצים והנחקרים ביותר בביוכימיה, הוא חלבון אלוסטרי. כל מולקולת המוגלובין מורכבת מארבע תת-יחידות; כל אחת מהן מסוגלת לקשור מולקולה דו-אטומית אחת של חמצן (O2). לאחר שנקשרת מולקולת חמצן אחת להמוגלובין, צורתו המרחבית של החלבון משתנה, ועל ידי כך נעשים שלושת אתרי הקישור האחרים בהמוגלובין חשופים יותר לסביבה החיצונית, דבר המגביר את נטייתם לקשור מולקולות חמצן.
במקרה של המוגלובין, הן האפקטור והן הסובסטרט הם אותה מולקולה (חמצן או פחמן דו-חמצני). במקרים רבים אחרים מדובר בשתי מולקולות שונות.
קישורים חיצוניים
[עריכת קוד מקור | עריכה]הערות שוליים
[עריכת קוד מקור | עריכה]- ^ Changeux J-P. 50th anniversary of the word “Allosteric.” Protein Science : A Publication of the Protein Society. 2011;20(7):1119-1124. doi:10.1002/pro.658.
