חמצון סוורן
חמצון סוורן, הקרוי על שם דניאל סוורן, הוא תגובה כימית לפיה אלכוהול ראשוני או שניוני מתחמצן לאלדהיד או קטון באמצעות אוקסליל כלוריד (אנ') (oxalyl chloride), דימתיל סולפוקסיד (DMSO) ובסיס אורגני, כגון טריאתילאמין (אנ')[1][2][3]. זוהי אחת מתגובות החמצון הרבות המכונות בדרך כלל חמצון 'DMSO משופעל'. התגובה ידועה באופי המתון שלה ובסיבולת הרחבה לקבוצות פונקציונליות[4][5][6][7].

תוצרי הלוואי הם דימתיל סולפיד (אנ'), פחמן חד-חמצני (CO), פחמן דו-חמצני (CO2), וכאשר טריאתילאמין משמש כבסיס - טריאתיל אמוניום כלוריד (אנ') (Et3NHCl). מבין תוצרי הלוואי הנדיפים, לדימתיל סולפיד ריח חזק שמתפשט ופחמן חד-חמצני רעיל בצורה חריפה, ולכן יש לבצע את התגובה והעבודה עליה במנדף. דימתיל סולפיד הוא נוזל נדיף (נקודת רתיחה 37°C) בעל ריח לא נעים אפילו בריכוזים נמוכים[8][9][10].
מנגנון[עריכת קוד מקור | עריכה]
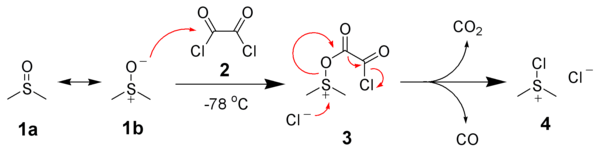
השלב הראשון בחמצון סוורן הוא תגובה בטמפרטורה נמוכה של DMSO, המסומן כ-1a, באופן רשמי בתור תורם רזוננס, המסומן כ-1b, עם אוקסליל כלוריד, 2. תוצר הביניים הראשון, 3, מתפרק במהירות תוך מתן פחמן דו-חמצני ופחמן חד-חמצני ומייצר כלורו (דימתיל)סולפוניום כלוריד, 4.
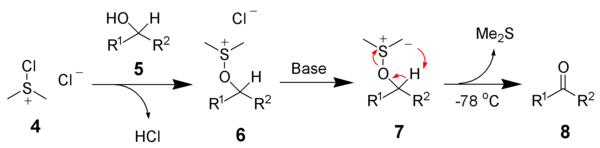
לאחר הוספת האלכוהול 5, הכלורו (דימתיל)סולפוניום כלוריד 4 מגיב עם האלכוהול כדי לתת את יון האלקוקסיסולפוניום, 6, תוצר הביניים העיקרי. תוספת של לפחות 2 אקוויוולנטים של בסיס - בדרך כלל טריאתילאמין - תגרום לדה-פרוטונציה של יון האלקוקסיסולפוניום כדי לתת את יליד (אנ') הגופרית, 7. במצב מעבר של טבעת בעלת חמישה איברים, יליד הגופרית 7 מתפרק ליצירת דימתיל סולפיד ואת תרכובת הקרבוניל הרצויה, 8.
וריאציות[עריכת קוד מקור | עריכה]
כאשר משתמשים באוקסליל כלוריד כחומר ההתייבשות, יש לשמור על התגובה בטמפרטורה נמוכה יותר ממינוס 60 מעלות צלזיוס בכדי להימנע מתגובות לוואי. באמצעות כלוריד ציאנורי (אנ') (Cyanuric chloride)[11] או אנהידריד טריפלואורואצטי (אנ')[12] במקום אוקסליל כלוריד, ניתן להעלות את טמפרטורת התגובה למינוס 30 מעלות צלזיוס ללא תגובות לוואי. שיטות אחרות לשפעול של DMSO כדי ליזום את היווצרותו של תוצר הביניים המרכזי 6 הן השימוש בקרבודיאימידים (אנ') (חמצון פיצנר-מופאת (אנ')), קומפלקס גופרית טריאוקסיד פירידין (חמצון פאריך-דורינג (אנ')) או אנהידריד אצטי (חמצון אולברייט-גולדמן). את תוצר הביניים 4 ניתן להכין גם מדימתיל סולפיד ו-N-Chlorosuccinimide (אנ') (חמצון קורי-קים (אנ')).
במקרים מסוימים, השימוש בטריאתילאמין כבסיס יכול להוביל לאפימריזציה בפחמן אלפא לקרבוניל החדש שנוצר. שימוש בבסיס נפחי יותר, כגון דיאיזופרופילאתילאמין, יכול להפחית את תגובת הלוואי הזו.
שיקולים[עריכת קוד מקור | עריכה]
דימתיל סולפיד, תוצר לוואי של חמצון סוורן, הוא אחד הריחות הלא נעימים הידועים לשמצה בכימיה אורגנית. בני אדם יכולים להבחין בתרכובת זו בריכוזים נמוכים כמו 0.02 עד 0.1 חלקים למיליון[13]. פתרון פשוט לבעיה זו הוא שטיפת כלי זכוכית משומשים עם אקונומיקה או תמיסת אוקסון (אנ'), אשר תחמצן את הדימתיל סולפיד בחזרה לדימתיל סולפוקסיד או לדימתיל סולפון, שניהם חסרי ריח ואינם רעילים[14].
תנאי התגובה מאפשרים חמצון של תרכובות רגישות לחומצה, שעלולות להתפרק בתנאי חמצון חומציים כגון חמצון ג'ונס (אנ'). לדוגמה, בסינתזה של תומפסון והית'קוק של ססקויטרפן (אנ') isovelleral[15], השלב האחרון בו משתמשים בפרוטוקול סוורן, נמנע משחלוף של הציקלופרופאן מתאנול במולקולה, הרגיש לחומצה.

ראו גם[עריכת קוד מקור | עריכה]
לקריאה נוספת[עריכת קוד מקור | עריכה]
- P. Y. Bruice (2017). Organic Chemistry (Eighth ed.). Prentice Hall.
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- חמצון סוורן ב-"Organic Chemistry Portal"
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ Omura, K.; Swern, D. (1978). "Oxidation of alcohols by "activated" dimethyl sulfoxide. A preparative, steric and mechanistic study". Tetrahedron. 34 (11): 1651–1660. doi:10.1016/0040-4020(78)80197-5.
{{cite journal}}: תחזוקה - ציטוט: multiple names: authors list (link) - ^ Mancuso, A. J.; Brownfain, D. S.; Swern, D. (1979). "Structure of the dimethyl sulfoxide-oxalyl chloride reaction product. Oxidation of heteroaromatic and diverse alcohols to carbonyl compounds". J. Org. Chem. 44 (23): 4148–4150. doi:10.1021/jo01337a028.
{{cite journal}}: תחזוקה - ציטוט: multiple names: authors list (link) - ^ Mancuso, A. J.; Huang, S.-L.; Swern, D. (1978). "Oxidation of long-chain and related alcohols to carbonyls by dimethyl sulfoxide "activated" by oxalyl chloride". J. Org. Chem. 43 (12): 2480–2482. doi:10.1021/jo00406a041.
{{cite journal}}: תחזוקה - ציטוט: multiple names: authors list (link) - ^ Organic Syntheses Procedure, www.orgsyn.org (באנגלית)
- ^ Organic Syntheses Procedure, www.orgsyn.org (באנגלית)
- ^ Organic Syntheses Procedure, www.orgsyn.org (באנגלית)
- ^ Tojo, G.; Fernández, M. (2006). Oxidation of alcohols to aldehydes and ketones: A guide to current common practice. Springer. ISBN 0-387-23607-4.
- ^ Mancuso, A. J.; Swern, D. (1981). "Activated dimethyl sulfoxide: Useful reagents for synthesis". Synthesis (Review). 1981 (3): 165–185. doi:10.1055/s-1981-29377.
{{cite journal}}: תחזוקה - ציטוט: multiple names: authors list (link) - ^ Tidwell, T. T. (1990). "Oxidation of alcohols to carbonyl compounds via alkoxysulfonium ylides: The Moffatt, Swern, and related oxidations". Org. React. (Review). 39: 297–572. doi:10.1002/0471264180.or039.03. ISBN 0471264180.
- ^ Tidwell, T. T. (1990). "Oxidation of alcohols by activated dimethyl sulfoxide and related reactions: An update". Synthesis (Review). 1990 (10): 857–870. doi:10.1055/s-1990-27036.
- ^ De Luca Lidia (2001). "A Mild and Efficient Alternative to the Classical Swern Oxidation". The Journal of Organic Chemistry. 66 (23): 7907–7909. doi:10.1021/jo015935s. PMID 11701058.
- ^ Omura, Kanji; Sharma, Ashok K.; Swern, Daniel (1976). "Dimethyl Sulfoxide-Trifluoroacetic Anhydride. New Reagent for Oxidation of Alcohols to Carbonyls". J. Org. Chem. 41 (6): 957–962. doi:10.1021/jo00868a012.
- ^ Morton, T. H. (2000). "Archiving Odors". In Bhushan, N.; Rosenfeld, S. (eds.). Of Molecules and Mind. Oxford: Oxford University Press. pp. 205–216.
- ^ Atkins, William J. Jr.; Burkhardt, Elizabeth R.; Matos, Karl (2006). "Safe Handling of Boranes at Scale". Org. Process Res. Dev. 10 (6): 1292–1295. doi:10.1021/op068011l.
- ^ Thompson, S. K.; Heathcock, C. H. (1992). "Total synthesis of some marasmane and lactarane sesquiterpenes". J. Org. Chem. 57 (22): 5979–5989. doi:10.1021/jo00048a036.

