לחץ אוסמוטי
לחץ אוסמוטי הוא הלחץ שמפעילה תמיסה על ממברנה חדירה למחצה המפרידה בינה לבין תמיסה אחרת, עקב הפרש בריכוז המומס בין שתי התמיסות.
פוטנציאל אוסמוטי הוא פוטנציאל האנרגיה של האוסמולריות בתמיסה, המונעת מהממס (שהוא על פי רוב מים, בסביבה ביולוגית) לצאת ממנה דרך ממברנה חדירה למחצה. כאשר הממס הוא מים, זהו המונח ההפוך לפוטנציאל מים, שהוא פוטנציאל האנרגיה המשפיעה על המים לצאת מהתמיסה דרך הממברנה.
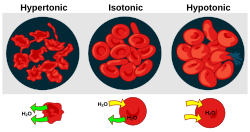
כאשר תא ביולוגי נמצא בסביבה היפוטונית (פנים התא מכיל ריכוז נמוך יותר של מים וגבוה יותר של מולקולות שאינן חודרות את הממברנה), מים חוצים את ממברנת התא לתוכו, ומפעילים עליו לחץ אוסמוטי להתרחב. בתאי צמח, דופן התא מגביל את ההתרחבות, ונוצר לחץ על הדופן כלפי חוץ, הקרוי לחץ טורגור. ניתן לחשב את הלחץ האוסמוטי π של תמיסה מהולה בעזרת הנוסחא:
כאשר
- i - פקטור ואן 'ט הוף
- M - מולריות
- R - קבוע הגזים, R = 0.08206 L · atm · mol-1 · K-1
- T הוא הטמפרטורה התרמודינמית (טמפרטורה מוחלטת)
ניתן לראות דמיון רב בין הנוסחא לעיל לחוק הגזים האידיאליים; כמו כן ניתן לראות כי הלחץ האוסמוטי אינו תלוי במטען החלקיקים.
אוסמולריות[עריכת קוד מקור | עריכה]
אוסמולריות היא יחידת מידה המשמשת לתיאור הפוטנציאל האוסמוטי של תמיסה. את הנוסחה אפשר להציג גם בדרך הבאה:
כאשר C הוא ריכוז המומס ביחידות אוסמול (osmole או בקיצור Osm) לליטר. אוסמול הוא יחידת מידה המוגדרת כמול חלקיקי מומס לליטר ממס. כאשר המומס מתחלק למספר יונים מוכפל האוסמול לפי מספר היונים. כך למשל מולר אחד של גלוקוז שווה לאוסמול אחד, אולם מולר אחד של נתרן כלורי מתפרק במים ליוני נתרן וליוני כלור ולכן מספר החלקיקים שלו כפול ושווה לשני אוסמולים.
בפיזיולוגיה נפוץ השימוש ביחידות מיליאוסמול לליטר [mOsm/liter].
יישומים[עריכת קוד מקור | עריכה]
לחץ אוסמוטי עומד בבסיס שיטת האוסמוזה ההפוכה, תהליך נפוץ לטיהור מים. המים לטיהור מושמים בכלי, ומופעל עליהם לחץ גדול מהלחץ האוסמוטי המופעל על ידי המים והמומסים בהם. בכלי יש פתח המכוסה בממברנה חדירה למחצה, המאפשרת מעבר מולקולות מים, אך לא חלקיקי מומס. ללא הפעלת לחץ חיצוני, מים מטוהרים יעברו את הממברנה לכיוון המים הלא-מטוהרים (כדי להגדיל בהם את ריכוז המים, כלומר, להקטין את ריכוז המומסים) - אוסמוזה. הפעלת הלחץ גורמת להיפוך כיוון התהליך - אוסמוזה הפוכה. הלחץ האוסמוטי של מי ים הוא כ-27 אטמוספירות. מתקני התפלת מים בשיטת אוסמוזה הפוכה משתמשים בלחצים של כ-70 אט' להתפלת מי ים.
לחץ אוסמוטי משמש למטרות רבות בצמחים. לחץ טורגור, הלחץ על דפנות התאים, מאפשר לצמחים עשבוניים לעמוד זקופים, ובעזרתו צמחים מווסתים את פתיחת הפיוניות שלהם. בתאי בעלי חיים, להם אין דפנות, לחץ אוסמוטי מופרז עלול לגרום לציטוליזה (תמס התא).
ראו גם[עריכת קוד מקור | עריכה]
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- לחץ ופוטנציאל אוסמוטי (באנגלית)


