נתרן פחמתי – הבדלי גרסאות
←פתיח: תיקון תעתוק |
הסרת קישור כפול |
||
| שורה 22: | שורה 22: | ||
|בסיסיות=3.67 |
|בסיסיות=3.67 |
||
}} |
}} |
||
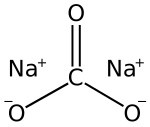
'''נתרן פחמתי''' (בלעז: '''סודיום קרבונט, Sodium Carbonate'''), הידוע גם כפחמת הנתרן, [[נתרן]] [[קרבונט]] או |
'''נתרן פחמתי''' (בלעז: '''סודיום קרבונט, Sodium Carbonate'''), הידוע גם כפחמת הנתרן, [[נתרן]] [[קרבונט]] או "סודה לכביסה", הוא [[מלח (כימיה)|מלח]] נתרני ש[[כתיב כימי|נוסחתו הכימית]] Na<sub>2</sub>CO<sub>3</sub>. פחמת הנתרן נפוץ בשימוש יומיומי בעיקר כ[[מים רכים|מרכך מים]]. ניתן להפיקו מאפר של צמחים מסוימים או, באופן מלאכותי, ממלח ו[[אבן גיר]], בתהליך הנקרא [[תהליך סולווה]]. |
||
==שימושים== |
==שימושים== |
||
גרסה מ־17:16, 11 בדצמבר 2015
שגיאות פרמטריות בתבנית:תרכובת
פרמטרים [ מסה מולקולרית, נוסחה כימית ] לא מופיעים בהגדרת התבנית
פרמטרים ריקים [ 1 ] לא מופיעים בהגדרת התבנית
 | |
| סודה לכביסה | |
 | |
| נתרן פחמתי | |
| שם סיסטמטי | נתרן פחמתי |
|---|---|
| שמות נוספים | סודה לכביסה |
| כתיב כימי |
CNa₂O₃ |
| מראה | מוצק גבישי לבן |
| מספר CAS | 497-19-8 |
| צפיפות | 2.54 גרם/סמ"ק |
| מצב צבירה | מוצק |
| מסיסות |
70 g/L (0 °C) 216 g/L (20 ºC) 450 g/L (100 °C) |
| טמפרטורת היתוך |
851 °C 1124.15 K |
| טמפרטורת רתיחה |
1600 °C 1873.15 K |
| חומציות | 10.33 |
| בסיסיות | 3.67 pKb |
נתרן פחמתי (בלעז: סודיום קרבונט, Sodium Carbonate), הידוע גם כפחמת הנתרן, נתרן קרבונט או "סודה לכביסה", הוא מלח נתרני שנוסחתו הכימית Na2CO3. פחמת הנתרן נפוץ בשימוש יומיומי בעיקר כמרכך מים. ניתן להפיקו מאפר של צמחים מסוימים או, באופן מלאכותי, ממלח ואבן גיר, בתהליך הנקרא תהליך סולווה.
שימושים
הנתרן הפחמתי משמש בעיקר כמרכך מים בתהליך הכביסה, ולכן מכונה לעתים סודה לכביסה. כאשר לא משתמשים בנתרן הפחמתי, נדרשים דטרגנטים נוספים על מנת לספוג את יוני המגנזיום והסידן החופשיים במי הכביסה. כמו כן, סודה לכביסה משמשת כמסיר יעיל לכתמי שומן ואלכוהול. בנוסף, הסודה לכביסה משמשת כמונעת אבנית בכלים המשמשים להרתחת מים.
שימוש נוסף וחשוב לנתרן הפחמתי הוא בייצור זכוכית: כאשר מחממים נתרן פחמתי עם סיליקה וסידן פחמתי לטמפרטורות גבוהות, ולאחר מכן מקררים במהירות, נוצרת הזכוכית הנפוצה ביותר, הידועה בשם זכוכית סודה (Soda-lime glass).
בזכות בסיסותו של הנתרן הפחמתי הוא משמש לעתים כבסיס בתהליכים הדורשים ויסות. לדוגמה, הוא משמש כווסת pH בתהליך פיתוח תמונות. באופן דומה, פעמים רבות משתמשים בנתרן הפחמתי בברכות, כאשר יש צורך לבטל את החומציות של הכלור.
הנתרן הפחמתי משמש גם בתור אלקטרוליט בתהליכים כימיים, בזכות מוליכותו הטובה בתהליך האלקטרוליזה.
ראו גם
- סידן פחמתי
- נתרן ביקרבונט (סודה לשתייה)
