משאבת לב
מתקיים דיון בו מוצע לאחד את הערך משאבת לב מלאכותי LVAD עם ערך זה.
| ||
| מתקיים דיון בו מוצע לאחד את הערך משאבת לב מלאכותי LVAD עם ערך זה. | |
 | |
| שיוך |
mechanical circulatory support |
|---|---|
| מזהים | |
| קוד MeSH |
E04.050.430 |
| מזהה MeSH |
D006353 |
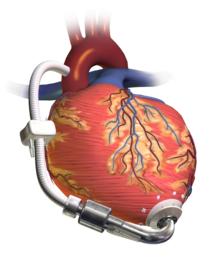
משאבת לב (באנגלית: ventricular assist device, בראשי תיבות: VAD) היא מכשיר מושתל אלקטרוני-מכני, המסייע בתפקוד הלב כאשר יש כישלון בתפקודו, בדרך כלל כאשר יש אי ספיקת לב.
ייתכנו מצבים בהם המשאבה תחליף חלקית את תפקוד הלב ומצבים בהם תחליף את תפקודו המלא.
ישנן משאבות המותאמות לסייע לחדר ימין בלב, חדר שמאל ואף לשני החדרים (באנגלית: RVAD, LVAD, BIVAD) והתאמתה תלויה בתפקוד הלב. למרות ההתאמה הוורסטילית, המשאבות לחדר השמאלי – LVAD הן הנפוצות ביותר, ולרוב הן היעילות ביותר לתפקוד לקוי.
המשאבה המיועדת לטיפול לחולי אי ספיקת לב עשויה להוות כ"גשר" בזמן שהמטופלים מחכים להשתלת לב, אך לעיתים תחשב כטיפול הסופי ולא כשלב המתנה בחולים שאינם מועמדים להשתלת לב.
תהליך השתלת המשאבה הוא במהלך ניתוח לב פתוח שעלול לכלול סיכונים רבים, אך המשאבה היא מכשיר מציל חיים במקרים רבים.[1]
תפקוד המשאבה ורכיביה[עריכת קוד מקור | עריכה]
משאבת הלב מורכב ממספר רכיבים, חיצוניים ופנימיים.[2]
המשאבה עצמה מחוברת ללב, והיא עוזרת לבצע את פעולותיו. במשאבת לב שמאלית, המשאבה שואבת דם מהחדר השמאלי בלב, מובילה אותו אל אבי העורקים (באנגלית: aorta) ומשם הדם ממשיך אל שארית הגוף רווי בחמצן. על מנת לאפשר את מעבר הדם מהלב אל העורק המשאבה מחוברת לחדר השמאלי של הלב ולה צינור המחובר אל אבי העורקים. אלו הם הרכיבים הפנימיים של המערכת המושתלת.
קיימים שני סוגי משאבות עיקריים - האחד מבצע את פעולת הלב בעזרת פולסטיליות, פעימות אשר מדמות את פעולת הלב, והשני על ידי זרם דם יציב מתמשך. מהמשאבה עצמה יוצא כבל (באנגלית: driveline) שיוצא אל מחוץ לעור ומתחבר למערכת שליטה ומקור חשמל חיצוני, עמם הולך המטופל באופן קבוע. המשאבה מופעלת על ידי מקור החשמל החיצוני בכל זמן נתון, וכן ניתן לבצע בקרה מתמדת בעזרת מכשיר השליטה. אלו הם הרכיבים החיצוניים של המערכת.
קיימים סוגים רבים של משאבות לב,[3] ותהליך פיתוחן מתמשך ומתעדכן בעולם הפיתוח הרפואי על מנת להקטין את גודל המשאבות, לייעל אותן ולצמצם את כמות הזיהומים.
בישראל, המשאבה העיקרית המושתלת כיום היא משאבת-לב שמאלית מסוג HM3.[4]
למי מיועדת משאבת הלב[עריכת קוד מקור | עריכה]
- מטופלים הממתינים להשתלת לב – ייתכן ותבוצע השתלת משאבת-לב במהלך המתנה להשתלת לב מתורם. המשאבה יכולה להמשיך את הזרמת הדם בלב למרות מחלת לב קיימת, והיא תוסר כאשר תבוצע השתלת הלב המיועדת. השתלת המשאבה עשויה לסייע בתפקוד שאר איברי הגוף שלא עובדים כראוי ובכך לשפר את המצב הרפואי. השתלה כזו נחשבת כ"גשר" עד להשתלה המיועדת.
- מטופלים ללא התאמה רגעית להשתלת לב – אם ישנו כשל בתפקוד הלב, ניתן לבצע השתלת משאבת לב כאשר המטופל אינו מתאים באותו הרגע להשתלת לב בגלל תנאים רפואיים אחרים. מדובר במעין שלב ביניים עד שתתקבל החלטה האם אינו כשיר לחלוטין להשתלת לב, ויישאר עם משאבת לב, או שייתכן ויהיה שיפור במצבו הרפואי ותהיה אופציה לבצע השתלת לב מתורם.
- מטופלים ללא התאמה להשתלת לב – כאשר אין התאמה כלל להשתלת לב, משאבות לב משמשות כטיפול לטווח ארוך לאנשים בעלי אי ספיקת לב שאינם מתאימים להשתלת לב. במקרה זה מדובר בטיפול סופי, שיכול לשפר באופן משמעותי את איכות החיים.
- מטופלים שתפקוד הלב עשוי לחזור למצב נורמלי – אם יש כישלון זמני בתפקוד הלב, הרופא עשוי להמליץ על השתלה כזו עד שהלב יוכל לחזור לתפקוד רגיל. פתרון זה נקרא כ"גשר" להחלמה.
סיכונים[עריכת קוד מקור | עריכה]
ניתוח השתלת משאבת-לב כולל סיכונים רבים, חלקם מעצם ביצוע ניתוח לב פתוח וחלקם ייחודיים למשאבה עצמה.
קרישי דם[עריכת קוד מקור | עריכה]
כאשר דם עובר דרם המשאבה, ייתכן וייווצרו קרישי דם. קריש דם יכול להאט או לחסום לחלוטין את זרימת הדם דרך הלב, ויכול להוביל לשבץ, התקף לב או לגרום למשאבה להפסיק לעבוד. ֿהרופא עשוי לתת למטופל מרשם לתרופות מדללות דם (לדוגמה: אספירין, קומדין) על מנת למנוע את היווצרות קשרי הדם לאחר השתלת המשאבה.
דימום[עריכת קוד מקור | עריכה]
השתלת משאבת-לב דורשת ניתוח לב פתוח. ניתוח כזה עשוי להגביר את הסיכון של דימום במהלך הניתוח או לאחריו. בנוסף, גם לקיחת מדללי הדם על מנת למנוע את קרישי הדם עלו להגביר את הסיכון לדימום.
זיהום[עריכת קוד מקור | עריכה]
משום שרכיבי ההפעלה של המערכת, מקור החשמל והשליטה נמצאים מחוץ לגוף, והם מחוברים למשאבה דרך העור, יש סיכון מוגבר לכניסה של חיידקים ולגרימת זיהום. כדאי לשים לב לסימנים של זיהום כגון כאב או אדמומיות באזור היציאה, יציאת נוזלים וחום.
כישלון המכשיר[עריכת קוד מקור | עריכה]
קיים סיכון לתפקוד לקוי של המשאבה לאחר ההשתלה. איכות השאיבה של המשאבה עלולה להיות לא מיטבית, אשר עלול לגרום לתופעת "שאיבה" של דפנות הלב ולמנוע מעבר של כמות דם מספקת. בנוסף, עלולה להיגרם בעיה למקור החשמל החיצוני ורכיבים אחרים במערכת האלקטרונית. כל בעיה כזו דורשת תגובה מיידית של המטופל והצוות הרפואי. המטופל יעבור הדרכה טרם ההשתלה על תפעול ופעולות שיש לנקוט במצבים כאלו.
מהלך הניתוח[עריכת קוד מקור | עריכה]
ניתוח להשתלת משאבת לב יבוצע על ידי צוות רפואי הרחב הכולל מנתח חזה ולב, רופא מסייע וצוות חדר ניתוח הכולל מרדים ועוזר מרדים, מפעיל מכונת לב ריאה, שתי אחיות חדר ניתוח, אחות VAD וקרדיולוג אקו. ניתוח להשתלת VAD נחשב "ניתוח לב פתוח", ובדרך כלל אורך בין 4 עד 6 שעות. אם בוצע ניתוח לב פתוח קודם, עשויות להיות הידבקויות והניתוח עלול להתארך. לאחר הרדמה, המרדים יכניס צינור הנשמה דרך הפה לתוך קנה הנשימה, ויחוברו עירויים לצורך טיפול תרופתי במהלך הניתוח ולאחריו. הניתוח יתחיל בחתף באמצע החזה. המנתח יפריד את הצלעות ויפתח את כלוב הצלעות על מנת לגשת אל הלב. בניתוחים רבים מסוג זה, הלב יחובר למכונת לב ריאה שתבצע את תפקיד הלב במהלך הניתוח, על מנת לאפשר תהליך ניתוח יציב ולשמור עם הזרם הדם והחמצן אל הגוף. לאחר מכן צוות הניתוח יחל בהשתלת המכשור הרפואי. בהשתלת משאבת לב שמאלית – חיבור משאבת הלב, חיבור הצינור לאבי העורקים, הולכת הכבלים אל מחוץ לעור אל יחידת השליטה. המשאבה תופעל והדם יחל לזרום בגוף תוך בקרה רציפה של הצוות הרפואי על תפקוד המשאבה, תתקיים הורדה ממכונת לב-ריאה באופן הדרגתי, והמשאבה תפעל לבדה. בסיום הניתוח, סוגרים את החתכים הפתוחים והמטופל יועבר ליחידה לטיפול נמרץ להתאוששות מהניתוח.
ראו גם[עריכת קוד מקור | עריכה]
לקריאה נוספת[עריכת קוד מקור | עריכה]
- Limael E. Rodriguez, M.D., Erik E. Suarez, M.D., Matthias Loebe, M.D., Ph.D., and Brian A. Bruckner, M.D, Ventricular Assist Devices (VAD) Therapy: New Technology, New Hope?
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- מידע על משאבת לב ותהליך הניתוח
- מאמר - השתלת משאבת לב לטווח הארוך
- ניתוח לב פתוח
- חוברת הדרכה - מרכז רפואי רבין
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ Ventricular assist device (VAD) - Mayo Clinic, www.mayoclinic.org
- ^ What is an LVAD? How does it work? | MyLVAD, www.mylvad.com
- ^ Types of VADs - Jefferson University Hospitals, hospitals.jefferson.edu
- ^ Abbott - HeartMate 3™ | MyLVAD, www.mylvad.com
