מיוגלובין
 | |
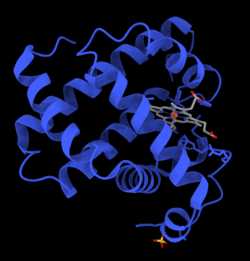
| המבנה התלת-ממדי של מיוגלובין | |
| שיוך |
myoglobin, pore-forming globin, globin/protoglobin, globin-like superfamily, גלובין |
|---|---|
מיוגלובין הוא חלבון גלובין קטן, המשמש לצד ההמוגלובין לנשיאת חמצן בגופם של בעלי חיים.
מיוגלובין מורכב מ-153 חומצות אמינו. במרכזו נמצאת קבוצת הם - מערכת טבעות חנקניות שבמרכזה אטום ברזל. קבוצת ההם היא זו המאפשרת את נשיאת החמצן, על ידי קשירת המולקולה הדו-אטומית של החמצן לאטום הברזל במרכזה.
מיוגלובין הוא נושא החמצן העיקרי בשרירים. האפיניות שלו לחמצן (זיקתו לקשירת חמצן) גדולה מזו של ההמוגלובין, המשמש לנשיאת חמצן בדם. ההבדל באפיניות בין שני החלבונים מאפשר את מעברו של החמצן מההמוגלובין למיוגלובין, וכך, את המשך זרימתו של החמצן לכיוון תאי הרקמות. בנוסף, ההבדל באפיניות מותאם למיקומם ותפקידם הפיזיולוגי: בריאות, בהן ריכוז החמצן גבוה, משמש ההמוגלובין לקשירת חמצן; ובשרירים, בהם ריכוז החמצן נמוך, משמש המיוגלובין לקשירת חמצן המשתחרר מההמוגלובין.
למיוגלובין יש רק תת-יחידה אחת ואילו ההמוגלובין מורכב מארבע תת-יחידות שכל אחת מהן דומה מאוד למיוגלובין. חלוקת המוגלובין לארבע תת-יחידות המאפשרת להמוגלובין להיות אלוסטרי (משנה זיקה לחמצן לפי מספר מולקולות החמצן שהוא כבר קשר). העובדה שכל אחת מתת היחידות דומה מאוד למיוגלובין מעידה על ההשתלשלות האבולוציונית של שני החלבונים; ההמוגלובין התפתח, ככל הנראה, מהמיוגלובין.
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- מיוגלובין, באתר אנציקלופדיה בריטניקה (באנגלית)
- ^ 1 2 3 GRCh38: Ensembl גרסה 89: ENSG00000198125 - Ensembl, מאי 2017
- ^ 1 2 3 GRCm38: Ensembl גרסה 89: ENSMUSG00000018893 - Ensembl, מאי 2017
- ^ "Human PubMed Reference:".
- ^ "Mouse PubMed Reference:".