תא שלוש אלקטרודות
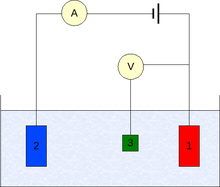
תא שלוש אלקטרודות באלקטרוכימיה הוא מתקן המשמש למדידות חשמליות. חשיבותו היא במגוון הטכניקות שאפשר ליישם בו, ובאיכות המדידות שניתן לבצע באמצעותו.
התא מורכב משלוש אלקטרודות: אחת היא העובדת ומפעילה מתח חשמלי וזרם חשמלי, אלקטרודת הייחוס משמשת למדידת המתח, והאלקטרודה העוזרת משמשת להזרמה ומדידה של הזרם. סידור זה הוא שיכלול של תא אלקטרוכימי, המאפשר מדידת רבות יותר ומדויקות יותר.
כללי[עריכת קוד מקור | עריכה]
שלוש האלקטרודות הן: אלקטרודה עובדת, אלקטרודת ייחוס ואלקטרודה עוזרת. הפרש המתחים בתא נופל בין האלקטרודה העובדת לאלקטרודת הייחוס, ואילו הזרם החשמלי זורם בין האלקטרודה העובדת לאלקטרודה העוזרת. תא מסוג זה ניתן היה לייצר רק אחרי המצאת המערכת האלקטרונית מגבר שרת המאפשרת הפרדה בין מדידת זרם למתח. חשיבותה של הפרדה זו רבה שכן מדידה של האחד משפיעה על תוצאות המדידה של האחר. זאת ועוד, הפרדה זאת מאפשרת מגוון טכניקות שבלתי ניתנת ליישום בתא אלקטרוכימי. שיטות המדידה המסורתיות נוהגות להפעיל מתח על התא ולמדוד את הזרם, (למשל וולטמטריה ציקלית), אם כי קיימת גם שיטות בהם הזרם מופעל על ידי המכשיר והמתח הוא הנמדד, או שיטת בהם מודדים מתח ללא הפעלת זרם.
מבנה התא[עריכת קוד מקור | עריכה]
מכיוון שתא זה משמש למדידות חשמליות עליו להיות מבודד. נהוגים תאים מזכוכית ותאים מטפלון. צורתם עשויה להיות גלילית, יתרון מסוים לצורה הגלילית היא הסימטריה הרבה שלהם, המקלה על חישובים הנוגעים למתרחש בתא. ישנם גם תאים בצורת חרוט קטום, או בצורות הייחודיות לכל ניסוי.
נהוג למלא את התא בנוזל המכיל מלח ממומס המשמש כאלקטרוליט. נוזל זה סוגר את המעגל החשמלי בין האלקטרודות, כלומר מאפשר לצורונים נושאי מטען לזרום בין אלקטרודה אחת לשנייה ובכך ליצור מתח או זרם. תפקיד שני של המלח המומס הוא מיסוך המתח הנובע מהאלקטרודות: היונים של המלח המומס מסתדרים בגבולות הנוזל ובכך מאפסים את השדה החשמלי בתוכו, תופעה המשותפת גם למוליכים אחרים בשדה חשמלי.
ניתוח חשמלי של התא[עריכת קוד מקור | עריכה]
כדי לחשב את הזרם בתא יש להביא בחשבון את קצב התרחשות תגובות החמצון-חיזור (וכמילת הלחם "חימזור") על פני האלקטרודות: אם המתח המסופק על ידי האלקטרודות הוא מסדר גודל של פוטנציאל החיזור של הצורון נושא המטען קצב החמצון-חיזור ייקבע על ידי הפרש המתחים, כלומר יציית למשוואת נרנסט. במקרה בו המתח המסופק על ידי האלקטרודה מספיק כדי ליצור פעילות חימזורית לצורון נושא המטען, קצב החימזור ייקבע על פי הסתברות הצורון להתנגש התנגשות פוריה באלקטרודה, כלומר על פי הקינטיקה של התגובה. במקרים בהם המתח המסופק על ידי האלקטרודה רב אף יותר, הגורם המשפיע היחיד הוא קצב הגעת הצורונים נושאי המטען אל האלקטרודה. לתנועת מטענים ייתכנו שלושה גורמים: תנועה בהשפעת הפרש פוטנציאלים חשמלי - זרם מיגרציה, תנועה בהשפעת ערבוב - קונבולוציה כימית, ותנועה בהשפעת דיפוזיה. כאמור תנועה בהשפעת הפרש פוטנציאלים אינה מתרחשת בגלל המיסוך. אם במהלך הניסוי התמיסה מעורבבת, הערבוב הוא הגורם הדומיננטי בקביעת קצב תנועת הצורונים, ולכן הערבוב יקבע גם את המתח והחשמל. בהיעדר ערבוב, הדיפוזיה היא הגורם הדומיננטי שיקבע את והמתח והזרם.
לקריאה נוספת (באנגלית)[עריכת קוד מקור | עריכה]
- Bard & Faulkner, Electrochemical Methods: Fundamentals and Applications, Second Edition, wiley, January 2001.

