זכוכית


זכוכית או חומר זכוכיתי הוא מוצק אמורפי אחיד, המיוצר על-פי רוב על ידי קירור[1] של חומרים מותכים. הקירור המהיר מונע היווצרות של שריג גבישי. לחומרים אלו יש טמפרטורה אופיינית למעברם ממצב צמיגי למצב זכוכיתי ומכונה "מעבר זכוכיתי" ומסומנת בספרות Tg.
בצורתה הטהורה הזכוכית היא חומר שקוף, בעל קשיות גבוהה באופן יחסי, עמיד לשחיקה ועמיד בדרך כלל מבחינה כימית וביולוגית. הזכוכית העתיקה, שהוכנה מקווארץ ונתרן פחמתי הייתה מסיסה באופן טבעי (בתהליך איטי). המסיסות מצטמצמת על ידי הוספת סידן פחמתי. ניתן ליצור זכוכית ממגוון רחב של חומרים, אולם רק מספר מצומצם של חומרים אכן נמצא בשימוש. העיקרי שבהם הוא קווארץ, המרכיב של חול נקי או בשמו הכימי צורן דו-חמצני SiO2.
ניתן לעצב את הזכוכית בקלות רבה לגופים בעלי שטח פנים חלק ובלתי חדיר. תכונות אלו הופכות את הזכוכית לחומר בעל מגוון רחב של שימושים. עם זאת, הזכוכית שבירה למדי ועלולה להתנפץ לרסיסים חדים. תכונותיה השונות של הזכוכית עשויות להשתנות על ידי הוספת מרכיבים שונים או טיפול בחום.
היסטוריה[עריכת קוד מקור | עריכה]

זכוכית נוצרה בטבע בעת התנגשות מטאורים בפני השטח של כדור הארץ, כבר לפני מיליוני שנים. מוכרים היטב שני סוגים של זכוכית טבעית - טקטיט וזכוכית מדבר לובית[2]. פגיעת ברק במשטח חול יוצר לפעמים צינוריות זכוכית דקות, הנקראות פולגוריט (אנ').[3] התפרצויות הרי געש פולטות לפעמים זכוכית געשית הנקראת אובסידיאן.[3] בני אדם השתמשו בזכוכית זו כבר בתקופת האבן. האובסידיאן סותת לסכינים וראשי חיצים חדים ביותר[4]. כבר בתקופה הפלאוליתית התיכונה נישאו כלי האובסידיאן או גושי אובסידיאן בלתי מעובד למרחק ניכר ממקום החציבה[5]. משערים שזכוכית יוצרה על ידי בני אדם בצורה אקראית, כ־4000 שנים לפני הספירה, בתהליך לוואי של הפקת מתכות. בהשפעת הטמפרטורה הגבוהה, האפר שנותר אחרי שריפה של זרעים התחבר עם החול ונוצרה זכוכית סיליקטית המכילה 60% SiO2. זכוכית זו שימשה ליצור תכשיטים.[6] לפי עדויות ארכאולוגיות, ייצור מכוון של כלי זכוכית נעשה כ-1500 שנה לפני הספירה, במצרים ובמסופוטמיה. לאחר זאת, במשך 300 שנה ייצור הזכוכית התפתח במהירות ואז חלה ירידה בעיסוק בזכוכית. במסופוטמיה חלה התאוששות כ-700 שנה לפנה"ס ואילו במצרים 500 שנה לפנה"ס. מאז, במשך 500 שנה, מצרים וארצות אחרות לאורך החוף המזרחי של הים התיכון הפכו למרכזים ליצור זכוכית.[7]
בשלב מאוחר יותר, יצור הזכוכית הגיע אף צפונית לאלפים. בכתב העת Antiquity פורסם ב-2023 כי נמצאו שרידים מסדנת הזכוכית מלפני 2000 שנים, באתר נמצ'יצה אשר בצ'כיה. המקום נחשב לאחד מאתרי ההתיישבות החשובים ביותר במאה ה-3-2 לפנה"ס, והיו בו מרכז ייצור של תכשיטי זכוכית ומסחר בהם. במקביל המקום שימש כמרכז פולחני ומושב לאליטות[8].
תחילת יצור הזכוכית הייתה מאתגרת משום שתנורי ההתכה היו קטנים והפקת החום שלהם הספיקה אך בקושי להתכת רכיבי הזכוכית. במאה הראשונה לפני הספירה הומצא צינור ניפוח הזכוכית. המצאה זו הקלה על יצור הכלים והוזילה אותם. יצור הזכוכית פרח באימפריה הרומית והתפשט מאיטליה לכל שאר האימפריה. בשנת 1000 לספירה, בעיר אלכסנדריה שבמצרים, היה המרכז החשוב ביותר ליצור זכוכית. במאות ה-13 וה14 אמנות הויטראז' הגיעה לשיאה באירופה, כפי שניתן לראות בקתדרלות קנטרברי ושארטר.
בתקופת מסעי הצלב מרכז תעשיית הזכוכית של אירופה עבר לוונציה. משום השימוש הרב בתנורים בתעשיית הזכוכית, שליטי ונציה חששו לשריפה בעיר, אשר רובה הייתה בנויה עץ, ובשנת1291 פרסמו צו אשר חייב את כל התעשייה לעבור לאי מוראנו[9]. חלק מאמני מוראנו נדדו לצפון אירופה ופיתחו שם את יצור הזכוכית.
בארצות הברית, בית החרושת הראשון לזכוכית הוקם בווירג'יניה, בשנת 1608. בשנת 1870 הומצאה המכונה החצי אוטומטית ליצור בקבוקים. החל בשנת 1890 הומצא מיכשור מדויק ויעיל ליצור מוצרי זכוכית שונים. בשנת 1959 הומצא תהליך חדיש ליצור זכוכית שטוחה ובתהליך זה מייצרים עד היום % 90 מהזכוכית השטוחה.[7]
בחצי השני של המאה העשרים התרחב השימוש בזכוכית גם כחומר ליצירת מעטפת של בניינים, ובפרט למעטפת של גורדי שחקים.
לדעת מחבר הספר "ספר היוחסין[10]", הומצא שימוש מודרני בזכוכית, לייצור מראות. "ובשנת ג' אלפים ותש"ע[11] היה איש שהמציא המראה של זכוכית", כנראה בידי חוקר יווני/רומאי.
הזכוכית במקרא ובתלמוד[עריכת קוד מקור | עריכה]

השם "זכוכית" מוזכר פעם אחת במקרא: ”לֹא יַעַרְכֶנָּה זָהָב וּזְכוֹכִית, וּתְמוּרָתָהּ כְּלִי פָז.” (ספר איוב, פרק כ"ח, פסוק י"ז), כתיאור לכלים יקרים.
מקור המילה[עריכת קוד מקור | עריכה]
מקור המילה הוא תכונת הזַכּוּת המאפיינת אותה. חוקר התלמוד הרב יהושע בראנד, בספרו כלי זכוכית בספרות התלמוד[12], מצביע על מונחים נוספים במקרא, שלדעתו פירושם זכוכית, כגון: "חול", "חלונות אטומות" ועוד.
בלשון חז"ל נקראה הזכוכית גם "סכוכית" (תוספתא מסכת שבת) או "זוגיתא" (תלמוד בבלי מסכת ברכות). בימי חז"ל הייתה הזכוכית יקרה מאוד מפני שהיה קשה מאוד לזככה ולייצר זכוכית שקופה או 'זכוכית לבנה' בלשון חז"ל. הגמרא[13] מספרת שכוס מזכוכית לבנה הייתה שווה 400 זוז.
סוגי זכוכית[עריכת קוד מקור | עריכה]


הזכוכית הנפוצה סודה ליים (Soda-lime)[עריכת קוד מקור | עריכה]
הזכוכית הנפוצה ביותר בשימוש נקראת Soda-Lime glass והיא משפחת ההרכבים הנפוצה ביותר ומשמשת בין היתר לשמשות, כלי אוכל, מוצרי נוי וכלי אחסון. כלי האחסון העיקריים עשויי הזכוכית הם הבקבוקים. התערובת להכנתם מכילה 8 סוגי תחמוצות, ביניהם - סיליקה (72.5%), אלומינה (1.5%), סידן חמצני (7.5%), נתרן חמצני (14.5%), מגנזיום חמצני (3.77%), תחמוצת ברזל (0.1%) ותחמוצת אשלגן (0.7%). הרכבה מ-81%−63%[14] צורן דו-חמצני (SiO2 - קוורץ, חומר הגלם - חול), נתרן פחמתי Soda (להורדת טמפרטורת ההתכה ומניעת גיבוש) וגיר (סידן פחמתי) Lime להעלאת היציבות הכימית.
הזכוכית העתיקה, אשר הוכנה מחול ונתרן פחמתי, הייתה מסיסה, אם כי , בקצב איטי. הסידן הפחמתי (אבן גיר) שמוסף היום מייצב את הזכוכית. בתקופה הרומית מקור הסידן הפחמתי היה בשברי הצדפות, אשר נמצאו באופן טבעי בחול, שהיה חומר הגלם ליצור הזכוכית.[6]
הרכב התוספים בזכוכית, וסוגי התוספים מאפשר קבלת זכוכיות שונות עם תכונות מכניות, אופטיות שונות המתאימות למגוון שימושים.
נקודת ההתכה של סיליקה טהורה (SiO2) היא בערך 2,000°C. הוספת חומרים כמו נתרן פחמתי ("סודה לכביסה" - סודיום קרבונט: Na2CO3) מורידים את טמפרטורת ההתכה ל-1,000°C בקירוב.
זכוכית בידודית[עריכת קוד מקור | עריכה]
זכוכית בידודית (double glazing) היא חלון המורכב משתי שכבות זכוכית או יותר המחוברות על ידי מסגרת (לרוב מאלומיניום), כאשר המסגרת מכילה סופחי לחות למניעת היווצרות אדים על חלקן הפנימי של השמשות. לעיתים בין השמשות יש גז מסוג ארגון להעצמת הבידוד התרמי והאקוסטי. מטרתה לבודד את חלל הבית הפנימי בידוד תרמי ואקוסטי.
זכוכית משוריינת[עריכת קוד מקור | עריכה]
 ערך מורחב – זכוכית משוריינת
ערך מורחב – זכוכית משוריינת
זכוכית בעלת מבנה המשלב זכוכית וחומרים פולימריים שונים בצורת שכבות מתחלפות, על מנת להפוך אותה לעמידה בפני פגיעת תחמושת של נשק קל (רובים וכדומה). התוצאה נקראת זגוגית[15] משוריינת ולא זכוכית משוריינת. בעת הפגיעה החלון מתרסק ונהרס, אך שומר על עמידותו בפני מספר מוגדר של פגיעות. בעולם נהוג דירוג של רמות לעמידותם של החלונות השונים לפגיעת קליעי נק"ל. חלונות משוריינים המשמשים כלי רכב צבאיים כבדים עמידים אף לאש מקלעים כבדים ורסיסים הנוצרים מפצצות ומטענים.

זכוכית מחוסמת[עריכת קוד מקור | עריכה]
זכוכית שעברה חימום מבוקר לטמפרטורה של כ-700 מעלות צלזיוס ולאחר מכן קירור מהיר מאוד באוויר. הקירור המהיר גורם לכך שהחלק החיצוני והחלק הפנימי של הזכוכית מתכווצים באופן שונה, מה שגורם להיווצרות מאמצים פנימיים. תהליך זה הופך את הזכוכית לבעלת חוזק גבוה פי 3–5 מאשר זכוכית רגילה. כאשר זכוכית מחוסמת נשברת, השבר גורם לשחרור המאמצים שנוצרו בתוך הזכוכית והיא מתנפצת לאלפי חלקים זעירים. ככל שהמאמצים הפנימיים בזכוכית גדולים יותר, כך היא קשה יותר, וכך גודל החלקיקים קטן יותר כאשר היא נשברת. זאת בניגוד לזכוכית לא-מחוסמת שיכולה להישבר גם למספר קטן של שברים גדולים[16].
פיברגלס (סיבי-זכוכית)[עריכת קוד מקור | עריכה]
סיבי זכוכית המיוצרים על ידי דחיסת זכוכית מותכת דרך חורים זעירים בבסיס הכבשן. כך נוצרים חוטים דקים מאוד שאפשר ליצור מהם אריגים קלים וחזקים. פיברגלס גם מגן מפני חום וחסין אש, ולכן בגדי הכבאים עשויים פיברגלס[17].
כלי זכוכית המיוצרים בניפוח[עריכת קוד מקור | עריכה]
 ערך מורחב – ניפוח זכוכית
ערך מורחב – ניפוח זכוכית
כלים אלה עשויים למעשה מזכוכית רגילה, אך טכניקת הייצור שלהם מאפשרת להם להיות דקים ועדינים והם משמשים בעיקר לקישוט. בישראל מוכרים כלים כאלה המיוצרים בחברון ומכונים "זכוכית חברון".
בעל המקצוע המכין כלים אלה מכונה "נפח זכוכית". זאת גם משום שהוא מנפח את הזכוכית המותכת באוויר.
ייצור זכוכית[עריכת קוד מקור | עריכה]

זכוכית גולמית מתקבלת כתוצאה מחימום רכיבי התערובת בכור היתוך. את הזכוכית הגולמית בדרך כלל מייצרים מחול SiO2, סודה Na2CO3, וסיד CaO. את כל הרכיבים מערבבים במכל ערבוב מיוחד ומחממים לטמפרטורה של 1,000°C ומתרחשת הריאקציה הבאה:
Na2CO3 + 2SiO2 + CaO → Na2SiO3 + CaSiO3 + CO2
מהזכוכית הגולמית ניתן להפיק מגוון רחב של זכוכיות שונות.
הרכב זכוכית[עריכת קוד מקור | עריכה]
ניתן למיין זכוכיות על פי הרכב היסודות המרכיבים את מבנה התחמוצת כלומר הקשורים לחמצנים מגשרים (יוצרי רשת Network formers או network intermediates). המשותף לכל הזכוכיות שהמרכיב העיקרי הוא סיליקה, בדרך כלל באחוז גבוה מ-50% מהרכב הזכוכית.
- זכוכית סיליקטית SiO2
- אלומוסיליקטית Al2O3;SiO2
- בורוסיליקטית B2O3;SiO2
- בורואלומוסיליקטית B2O3;Al2O3;SiO2
- אלומופוספטית P2O5;Al2O3;SiO2
- בורואלומופוספטית B2O3;Al2O3;P2O5
- אלומוסיליקופוספטית Al2O3;SiO2;P2O5
- פוספוונדית P2O5;V2O5
- סיליקוטיטנית SiO2;TiO2
- סיליקוצירקונית SiO2;ZrO
מבנה הזכוכית[עריכת קוד מקור | עריכה]
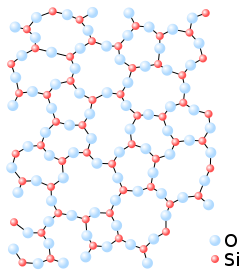
ממיינים את היסודות המשתתפים, לצד החמצן, בבניית הזכוכית ל-3 משפחות:
- יוצרי רשת (Network formers) הקשורים קוולנטית לחמצנים מגשרים
- משני רשת (Network modifiers) יוצרים קשרים יוניים עם חמצנים שאינם מגשרים (ב"קצוות פתוחים") לדוגמה מתכות אלקליות כנתרן ואשלגן או מתכות אלקליות עפרוריות כסידן או מגנזיום
- חומרי ביניים (Network intermediates),לדוגמה: BeO, Al2O3, Ga2O3, Fe2O3, TiO2, V2O5, Sb2O5, Nb2O5 שניתן לשלב ברשת החמצנים בריכוזים משתנים ויכולים להמצא גם כיונים בקצוות.
מודל רשת אקראית של זכריאסן (1932)[עריכת קוד מקור | עריכה]
זכריאסן חקר את המבנה של זכוכיות תחמוצת ועל סמך פיזור קרני X הוא גילה שיש להן סדר לטווח קצר, אך אין להם סדר לטווח הארוך. לכן לפי זכריאסן, זכוכית וגביש דומים רק בטווח קצר, אך לא בטווח ארוך כיון שמבנה הזכוכית לא שומר על מחזוריות כמו הגביש. על סמך התוצאות האלה הוא הגיע למסקנה שהזכוכית היא בעלת מבנה של רשת אקראית והציע את המודל שניתן לסכמו בכללים הבאים:
- כל אטום חמצן מחובר ללא יותר משני קטיונים.
- מספר אטומי חמצן מסביב לקטיון צריך להיות קטן (ארבעה או פחות)
- לפאוני חמצן יש יותר פינות משותפות מאשר צלעות או פאות
- לפחות שלוש פינות של כל פאוני חמצן הן משותפות
כללים האלה מנבאים נכון את יצירת זכוכית מתחמוצות כמו: SiO2, GeO2, B2O3, P2O5, כלומר מנבאים איזה יסוד יהיה "יוצר רשת" בזכוכית.
שימושים בתעשייה[עריכת קוד מקור | עריכה]

לזכוכיות העשויות מתרכובות יוצרות רשת, יש שימושים מוגבלים. למשל, תחמוצת של בור טהור (B2O3(Tg~4500C לא עמידה למים. זכוכית המכילה תחמוצת צורן SiO2 אשר שימושית בגלל עמידות כימית גם בטמפרטורות גבוהות במיוחד (עד 1,750°C), בעלת התנגדות לשינוי טמפרטורות (thermal shoc). זכוכית זאת חייבת להיות מעובדת בטמפרטורות שמעל 1,500°C. רוב סוגי הזכוכית השימושיים מכילים תוספים אשר מורידים את טמפרטורת העיבוד ומאפשרים קבלת תכונות רצויות ליישום. זכוכית לתעשייה מכילה לפחות חמש תחמוצות, לדוגמה זכוכית אופטית, מכילה יותר מעשר תחמוצות.
הוספת תרכובות יוניות ותחמוצות לזכוכית[עריכת קוד מקור | עריכה]

מוסיפים לזכוכית תרכובות יוניות (תחמוצות) ממספר סיבות:
- לקבלת זכוכית צבעונית. לדוגמה:
- CuO – תחמוצת נחושת – גוון כחול
- FeO – תחמוצת ברזל – גוון ירוק
- Fe2O3 – תחמוצת ברזל – גוון חום
- לזכוכית בה הוחלף חלק של סיליקה בתחמוצות בור, יש עמידות רבה לחום וכן עמידות כימית גבוהה. ניתן למצוא כמה סוגי תחמוצות בזכוכית. התחמוצת ממנה בנויה מטריצת הזכוכית (לדוגמה, סיליקה) נקראת:
- תוסף הנמצא בזכוכית כחלק מהרשת נקרא intermediate.
- תוסף השובר את רשת הזכוכית נקרא modifier.
קטיונים של נתרן ואשלגן הם network-modifier – אינם קשורים קוולנטית לרשת הטטראדרות היוצרת את הזכוכית אלא קשורים יונית לחמצנים בלתי מגשרים ויכולים לעבור דיפוזיה או לדלוף מהזכוכית (חילוף יונים) לתמיסות.
ישנם יוני חמצן אשר פועלים כגשרים בין יחידות הטטראדרים הנקראים bonding-oxygen. וישנם גם יוני חמצן שאינם משתתפים ביצירת מבנה הרשת ונקראים: אי גישור, non bonding-oxygen.
יש שלוש פעילויות עיקריות של מסיימי רשת:
- שבירת הקשרים A-O-A ויצירת אי גישור.
- הגברת התיאום של קטיון וחמצן.
- שילוב של שניהם.
- תוספת Na2O מורידה באופן משמעותי את טמפרטורת ההיתוך ואת הצמיגות של הזכוכית
- תוספת של Cao עוזרת להקטין את מסיסות הזכוכית במים
- כאשר היחס חמצן/סיליקון עולה על 2.5-3.0, קשה מאוד לקבל זכוכית ללא שימוש בתנאי הכנה מיוחדים, כגון קירור מהיר.
זכוכית קרמית[עריכת קוד מקור | עריכה]

בניגוד לזכוכית רגילה בעלת מבנה מולקולרי לא מסודר, זכוכית קרמית מכילה גבישים והיא בעלת מבנה דו פאזי: מיקרו-גבישים שביניהם אזורים אמורפיים. הפאזה הגבישית מהווה בין 30% ל-70% מולרי.
השימוש בזכוכית קרמיות החל בשנת 1950 והתגלה על ידי סטוקי (S.D. Stookey). סטוקי גילה במקרה את הזכוכית הקרמית. הוא השאיר בתנור שפעל בטמפרטורה גבוהה תערובת של זכוכית העשויה מליתיום סילקאט וכסף. בחזרתו, מצא סטוקי חומר קרמי לבן במקום "שלולית" של זכוכית מותכת אותה ציפה לראות. הדבר קרה מפני שהכסף היווה מרכז נוקלאציה (מרכז גיבוש), וגרם ליצירת מבנה קריסטלי של הזכוכית.
בתחילת היצור יש לחומרים אלו מבנה זכוכיתי. לאחר חימום והוספת חומרים שונים, הם הופכים להיות חומרים בעלי תכונות קרמיות. לזכוכית רגילה יש מבנה אמורפי, כלומר יש סדר מקומי אך אין מבנה קריסטלי מסודר, אין תאי יחידה שחוזרים על עצמם, בניגוד לזכוכית קרמית שבה פזורים בתווך האמורפי אזורים בהם האטומים מסודרים במבנה מסודר כלומר יש תאי יחידה שחוזרים על עצמם.
על מנת להכין זכוכית קרמית, יש להתיך את הזכוכית, ולשפוך את החומר המותך לתוך כלי בצורה הרצויה. קצב הקירור צריך לאפשר צמיחת גבישים. בתחילת המאה ה-21 עלה הביקוש לזכוכית קרמית, בעיקר בשל העובדה שניתן לעבד את החומר בקלות כמו זכוכית רגילה, ועם זאת מתקבל חומר בעל תכונות קרמיות רצויות כמו עמידות לזעזוע תרמי, קשיחות, רגישות לאור ועוד.
יתרון נוסף של הזכוכית הקרמית נעוץ בעובדה שניתן ליצור צורות מגוונות עם תכונות קרמיות מה שלא ניתן לעשות עם חומרים קרמיים אחרים. Owens-Corning Fiberglass (OCF) E-glass היא זכוכית העשויה מתרכובת של קלציום-אלומינו-סיליקאט בתוספת של מגנזיום, בור, ברזל, טיטניום וסודיום אוקסיד. לחומר זה יש עמידות גבוהה לחום ועמידות גבוהה למים.
שיטות ייצור של זכוכית קרמית[עריכת קוד מקור | עריכה]
על מנת ליצור זכוכית קרמית, יש לחמם זכוכית רגילה, לקרר ולחמם שוב. אך טיפול בחום אינו מספיק. כי צריך להוסיף חומר שיוכל לעשות נוקלאציה ובכך לאפשר את תחילת הגידול הגבישי. במטרה להפוך את הזכוכית לזכוכית קרמית בעלת מבנה קריסטלי, יש תחילה לטפל בחומר בטמפרטורה של כ-1,000°C, בין שעה לשעתיים במטרה ליצור זכוכית רגילה.
לאחר מכן לוקחים גולות במסה של 25–30 גרם, ושמים על משטח פלטינה. הגולות מחוממות ל-1,500°C במשך 30 דקות, ולאחר 30 דקות מוציאים את הגולות המותכות ומקררים אותן בטמפרטורת החדר. אם יש צורך בהוספת חומרים נוספים לקבלת חומר בעל תכונות רצויות, טוחנים את הזכוכית לאבקה, מוסיפים לה את התוסף הרצוי, ושמים שוב לחימום באותם התנאים, למשך 30 דקות נוספות. התוסף הוא בדרך כלל מלח. המלחים הנפוצים שמוספים על מנת ליצור זכוכית במבנה קריסטלי הם: ליתיום פחמתי Li2CO3, אלומיניום חמצני Al2O3, סידן חמצני CaO וטיטניום אוקסיד TiO2.
ניתן לקבל זכוכיות קרמיות עם תכונות שונות על ידי הוספת תוספים שונים וחימום לזמנים שונים. יעילות התוסף נמדדת בהתאם לעובי שכבת הזכוכית הנוצרת - ככל שהשכבה עבה יותר התוסף הוא יותר יעיל. זכוכית ללא תוספים לא יכולה ליצור מבנה קריסטלי מכיוון שאין חומר שיוכל לאפשר את תחילתו של מרכז הגיבוש.
שימושים[עריכת קוד מקור | עריכה]
בזכות תכונותיהן של הזכוכיות הקרמיות ניתן להשתמש בהם בסירי בישול, פלטות לבישול חשמלי, מראות טלסקופיות וחלונות מאובטחים.
קצב נוקלאציה (התגרענות)[עריכת קוד מקור | עריכה]
על מנת שזכוכית תעבור ממצב של מבנה אמורפי למבנה קריסטלי צריך ליצור תהליך נוקלאציה. תהליך זה מתרחש עם חימום הזכוכית, קירור הזכוכית ואז שוב חימום מעל ל-Tg.
קצב הנוקלאציה (התגרענות) תלוי בצמיגות של הזכוכית, באנרגיה החופשית של תהליך הנוקלאציה, בתדירות הוויברציה ובטמפרטורה.
– קצב הנוקלאציה
– האנרגיה החופשית של תהליך הנוקלאציה.
– תדירות הוויברציה
– צפיפות המולקולות ל-m3
תכונות זכוכית המיועדת לשימושים אופטיים[עריכת קוד מקור | עריכה]
ישנם מאפינים רבים הקובעים את התאמתה של זכוכית מסוימת לשימוש אופטי, בניהן בליעה כפונקציה של אורך גל (המשפיעה על הצבע), פגמים פנימיים בזכוכית (תכליל, inclusion) ומקדם שבירה ומספר אבה והטולרנסים (אנ') שלהם[18].[19] בנוסף ישנם מאפיינים של הזכוכית כחומר גלם לאלמנט אופטי שעבורו יש להגדיר את הסטיה מהממדים הנדרשים, טעויות מירכוז, הסטיה מהצורה המדויקת (surface figure, surface power), איכות פני שטח (S&D), חיספוס (אנ') (roughness) וכיוצא בזה[20][18]. מאפינים אלו מבוקרים על ידי תקנים בינלאומיים כמו MIL-PRF-13830B, MIL-G-174B ורבים אחרים[21][22].
תכונות אופטיות[עריכת קוד מקור | עריכה]
תכונות אופטיות של חומר מתארות את תגובת החומר למעבר אור דרכו. כאשר אור פוגע בחומר מסוים הוא יכול להיבלע בו, לחזור ממנו, או לעבור דרכו. למרבית השימושים, חשוב לבחון את יכולת החומר להעביר אור דרכו. תכונה זו כמעט הפוכה להחזרה, כאשר האור שאינו מועבר או מוחזר, נבלע. בליעת אור מתרחשת כאשר אור פוגע בחומר, והאנרגיה שלו נספגת בחומר באופן חלקי או מלא. חומר שקוף, בדומה לזכוכית שבשמשת החלון, מעביר כמעט את כל האור הפוגע בו. לכן ניתן לראות דמויות הנמצאות מצדו האחר.
הדרישה לזכוכיות בעלות תכונות אופטיות מסוימות הולכת ועולה בשנים האחרונות. תכונות אופטיות של זכוכית הן תכונות פיזיקליות, אך הן תלויות בהרכב הכימי של החומרים מהם עשויה הזכוכית. מרבית הזכוכיות יכולות להעביר דרכן את האור הנראה. זיהומים בזכוכית כגון נחושת או ברזל מורידים את היכולת של הזכוכית להעביר דרכה אור. גוון ירקרק של זכוכית (שניתן לראותו, למשל, כשמסתכלים בזכוכית מראה או חלון מהצד) נובע מהמצאות יוני ברזל.
בזכות יכולתם של הזכוכית להעביר את האור בתחום הנראה והאינפרא אדום הקרוב דרכן יש לזכוכיות שימושים רבים כגון: שמשות לחלונות, סיב אופטי, שימוש ביצירת קישוטים לבית ונברשות, עדשות למשקפיים, מצלמה ועוד.
לזכוכיות שונות יש מקדמי שבירה שונים (refractive index). מקדם שבירה - מקדם שבירה היא תכונה פיזיקלית של חומר שקוף, המציינת את שינוי הזווית של האור המועבר. מקדם השבירה תלוי בהרכב הכימי של הזכוכית ובמאמצים הפועלים בה.
זכוכית פוטוכרומית – היא זכוכית המתכהה כאשר נחשפת לאור השמש כתוצאה מפרוק גבישים של מלחי כסף באור UV ויצירת כסף מתכתי אטום. כאשר הקרינה נפסקת הגוון הכהה של הזכוכית נעלם כיוון שהכסף שוב מתחמצן לקבלת מלחים שקופים.

צבע[עריכת קוד מקור | עריכה]
צבע זכוכית תלוי בדברים הבאים:
- ביכולת של הזכוכית לבלוע אור.
- פיזור אורכי הגל של האור הנראה.
- רגישות לאור (photosensitivity).
- יכולת פלואורסצנציה.
כל הדברים לעיל מושפעים כתוצאה ממעבר אלקטרונים בשדה חשמלי, מקיומם של יוני מתכות טעונים או ממעבר של פוטונים.
זכוכית צבעונית[עריכת קוד מקור | עריכה]
זכוכית המתקבלת על ידי הוספת מלחים או תחמוצות:
- CuO - תחמוצת נחושת - גוון כחול.
- FeO - תחמוצת ברזל - גוון ירוק.
- Fe2O3 - תחמוצת ברזל - גוון חום.
- יון ניקל Ni+2 - כחול סגול או שחור.
- יון כרום Cr+3 - ירוק כהה.
שימושי הזכוכית הצבעונית הם בעיקר בתחום האומנות.
ישנן זכוכיות השקופות לחלוטין לאור נראה, ואטומות לחלוטין לאור אינפרה אדום. וישנן זכוכיות כמו קוורץ, היכולות להעביר גם את האור הנראה וגם את האור האינפרה אדום.
תכונות מכניות[עריכת קוד מקור | עריכה]
בתכנון עדשות ואלמנטים אופטיים אחרים יש לעיתים גם להתחשב בתכונות המכניות של החומר. תכונות אלו כוללות את מודול האלסטיות (קבוע יאנג), קשיות, מקדם התפשטות, צפיפות סגולית ועוד[23].[19]
תכונות כימיות[עריכת קוד מקור | עריכה]
תכונות נוספות שחשובות לשימושים שונים של זכוכית כחומר גלם אופטי מבוססות על התכונות הכימיות של סוג הזכוכית הספציפי. תכונות אלו הן, למשל, עמידות בפני חומצות ובסיסים, ועמידות בפני ספיחת מיים[24].
מיחזור הזכוכית[עריכת קוד מקור | עריכה]
התכלות טבעית של זכוכית אורכת מיליון שנה. אומנם הזכוכית אינה מזהמת קרקע או מי תהום מכיוון שהיא עשויה מחומרים טבעיים בלבד, שאינם מתפרקים, אך העדר מיחזור גורם לנזק אקולוגי מסיבות שונות:
- הזכוכית אינה מתכלה, ולכן שומרת על נפחה ומגדילה את נפח הפסולת הכולל.
- זכוכית שאינה ממוחזרת גורמת לבזבוז של חומר הגלם הטבעי של הזכוכית – החול. החול הוא משאב טבע שהולך ומצטמצם[25].
- כריית החול גורמת לרוב להרס הנוף הטבעי.
- מיחזור זכוכית תורם לחיסכון באנרגיה מכיוון שנדרשת השקעת אנרגיה פחותה בהתכת זכוכית ממוחזרת לעומת התכת חול גולמי.
- תהליך יצור הזכוכית מזכוכית ממוחזרת הוא תהליך בו פליטת המזהמים לאוויר מופחתת ביחס לייצור זכוכית מחול.
- קיימת סכנת שריפה במטמנות הפסולת השונות הנגרמת כתוצאה משברי הזכוכית שגורמים למיקוד קרני השמש.
על מנת למחזר זכוכית, על הזכוכית הנאספת לעמוד בכמה תנאים:
א. הרכב כימי ידוע: זכוכית שההרכב שלה דומה לחומרי הגלם והיא נקייה ממזהמים כגון קרמיקה, ברזל או אלומיניום.
ב. הפרדה: הזכוכית צריכה להיות מופרדת במיכלי האיסוף על פי צבעים – לבן, ירוק, חום או שקוף.
ג. תוויות: תוויות הנייר או הפלסטיק על בקבוקי הזכוכית מהווים הפרעה בשלב התכת הזכוכית הממוחזרת[26].
דוגמה לתהליך המיחזור:[27]
1. איסוף והפרדה - אריזות הזכוכית נאספות ממתקני האיסוף ומועברות למפעל ליצור זכוכית, שם הן מופרדות על פי הצבע - שקוף, ירוק או חום.
2. גריסה וניקוי - במתקן זה האריזות מנוקות משאריות התכולה (מזון בעיקר) ומתוויות הנייר, ועוברות גריסה גסה, לשם צימצום נפח הזכוכית. שברי הזכוכית נעים על סרט נע ובאמצעות זרם אוויר מסולקות שאריות הנייר. מגנט רב עוצמה מסלק את פקקי המתכת.
3. התכה ראשונה - שברי הזכוכית עוברים התכה. עבור זכוכית שצבעה ירוק, 80% מהשברים משמשים כחומר גלם ליצור זכוכית חדשה. לעומת זאת, עבור זכוכית שצבעה חום או לבן, רק 50% יכול לשמש חומר גלם.
4. הכנת תערובת - בהתאם ליעוד התוצר מכינים תערובת המכילה זכוכית ממוחזרת וחומרים נוספים.
5. התכה עיקרית - התערובת עוברת אל תנור התכה, שהוא אמבט בעומק 1.5 מטר, ובו טמפרטורה של 1500 מעלות צלזיוס. בתוך התנור פועלים שלושה מבערים בו זמנים, מתוך ששה.
6. יציקה - לאחר התכה מוחלטת של התערובת יוצקים את הנוזל החם לתוך תבניות. בסיום היציקה התוצרים עוברים לקירור מבוקר, הגורם להרפית החומר ומעניק קשיחות ועמידות לזכוכית.
7. בקרת איכות - מדגמים נבדקים לתכונות שונות. מוצרים שאינם עומדים בדרישות מוחזרים לגריסה.
ראו גם[עריכת קוד מקור | עריכה]
- בדולח
- ויטראז'
- טיפות הנסיך רופרט
- לבנת זכוכית
- זכוכית בעלת יכולת ניקוי עצמית
- מוזיאון הזכוכית
- ייצור זכוכית
לקריאה נוספת[עריכת קוד מקור | עריכה]
- Prindle WR, Danielson PS, and Malmendier JW. (1991). "Glass Processing', in Engineered Materials Handbook: Ceramics and Glasses, Vol. * ASM International, Materials Park, OH, pp. 377-394
- Duan, R.G. and Liang, K.M. (1998) "A Study on the crystallization of CaO-Al2O3-SiO2 system glasses". Journal of Materials Processing Technology, vol. 75, iss. 1-3, pp. 235-239
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- בלדד השוחי, איך עושים זכוכית?, באתר ערוץ עשר
- מבוא לאספנות זכוכית עתיקה באתר קולקט
- אורלי פיישטר; בועז גטניו, הזכוכית: שקופה, צבעונית ומתנפחת. הספרייה הווירטואלית של מטח
- ביתן הזכוכית במוזיאון ארץ ישראל בתל אביב
- פיטר גוין, מתכת שהיא זכוכית. מדע - עיתון מדעי לכל
- שושנה צובל, "זכוכית", מאי 2004, המרכז להשתלמויות מורים - שלומי(הקישור אינו פעיל)

- מה היא זכוכית קרמית? (באנגלית)
- Zanotto, E.D. (2008). Transparent glass - ceramics. International Materials Institute for New Functionality in Glass (באנגלית)
- תכונות אופטיות של זכוכית; הפקולטה למדע החומרים וקרמיקה, אוניברסיטה למדע וטכנולוגיה על שמו של סטניסלב סטאז'ץ' (באנגלית)
- זכוכית באתר אוניברסיטת סטנפורד
- זכוכית באתר של פרופ' א. נלסון מפקוטלה לחומרי כדור הארץ אוניברסיטת טוליין(הקישור אינו פעיל)
 (באנגלית)
(באנגלית)  ?Why is glass transparent סרטון המסביר מדוע הזכוכית שקופה
?Why is glass transparent סרטון המסביר מדוע הזכוכית שקופה ניפוח זכוכית, המפוח האנושי, 1938, ארכיון הסרטונים של AP
ניפוח זכוכית, המפוח האנושי, 1938, ארכיון הסרטונים של AP- זכוכית, באתר אנציקלופדיה בריטניקה (באנגלית)
 זכוכית, דף שער בספרייה הלאומית
זכוכית, דף שער בספרייה הלאומית
- http://books.ifmo.ru/book/pdf/808.pdf(הקישור אינו פעיל)
- http://www.pereplet.ru/obrazovanie/stsoros/60.html
- http://www.ngpedia.ru/cgi-bin/getpage.exe?cn=20&uid=0.612850065575913&inte=3(הקישור אינו פעיל)
- http://cryst.geol.msu.ru/courses/crchem/part2.pdf
- http://www.inmetal.ru/244-stroenie-silikatov.html
- http://www.grandinetti.org/Research/Applications/GlassStudies
- http://www.xumuk.ru/encyklopedia/2/4195.html
- http://www.megabook.ru/Article.asp?AID=674822
- http://window.edu.ru/resource/279/21279/files/0103_095.pdf
- http://ngipoteza.narod.ru/glass8.htm
- http://www.fnm.msu.ru/documents/16/4amorph.pdf(הקישור אינו פעיל)
- http://www.nanometer.ru/2011/10/02/funkcionalnie_materiali_262483/PROP_FILE_files_1/fumcmat_cer_2011.pdf
- http://www.ptc.tugraz.at/specmag/struct/random.htm
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ לעיתים נדרש קירור מהיר מאוד ולעיתים יחסית אטי. בכל אופן אין לקרר את החומר באופן אטי מדי כי אז עלול להיווצר מבנה גבישי
- ^ Glass in Nature, Corning Museum of Glass
- ^ 1 2 3 Cool Facts You Never Knew About Glassblowing, אתר של גלרית Habatat Detroit Fine Art, ספטמבר 2015
- ^ Nergis Firtina, Oldest workshop discovered in Ethiopia, dating back 1.2 million years, Interesting Engineering, פברואר 2023
- ^ AGAZI NEGASH and M. S. SHACKLEY; GEOCHEMICAL PROVENANCE OF OBSIDIAN ARTEFACTS FROM THE MSA SITE OF PORC EPIC, ETHIOPIA; Archaeometry 48, 1 (2006) 1–12
- ^ 1 2 Roman glass and its chemistry, Royal Society of Chemistry - educational resources
- ^ 1 2 The History of Glass - Glass Facts, Zibo Taiji Industrial Enamel Co.,Ltd
- ^ יוגב ישראלי, התגלתה סדנת הזכוכית הקדומה ביותר מצפון להרי האלפים, באתר ynet, 25 ביולי 2023
- ^ History of Murano Glass | History of Venetian Glass-making | Glass of Venice, Glass of Venice-בית מסחר אמריקאי לשיווק פריטי זכוכית מוראנו
- ^ ספר יוחסין מאמר שישי
- ^ בשנה העשירית לספירה הנוצרית
- ^ ד"ר יהושע בראנד, כלי זכוכית בספרות התלמוד, בצירוף מחקרים ומאמרים, ירושלים: מוסד הרב קוק, תשל"ח-1978, פרק שלישי, עמ' 16 - 41: "הזכוכית וכלי הזכוכית במקרא".
- ^ ברכות לד ע"ב.
- ^ Glass composition, glass types
- ^ זגוגית, באתר האקדמיה ללשון העברית
- ^ אבי סאייג, כיצד מחסמים חומרים כמו זכוכית ומתכת, מהו התהליך שמתרחש בחומרים הללו?, באתר מון דוידסון לחינוך מדעי- מכון ויצמן, מאי 2010
- ^ בגדי כבאים עשויים גם קוולר וספקטרה.
- ^ 1 2 Optical Glass מאמר שסוקר מאפינים של הזכוכית כחומר גלם לאלמנטים אופטיים, באתר www.edmundoptics.ca (באנגלית)
- ^ 1 2 Other Properties - Ohara Corp, 2022-11-22 (באנגלית אמריקאית)
- ^ Understanding Optical Specifications מאמר שסוקר איך מאפיינים ביצועים של אלמנטים אופטים, באתר www.edmundoptics.ca (באנגלית)
- ^ mil-g-174b Optical Glass QC, http://www.surplus-optics.com/ (באנגלית)
- ^ MIL-PRF-13830B, eksmaoptics.com (באנגלית)
- ^ Mechanical Properties - Ohara Corp, 2022-11-22 (באנגלית אמריקאית)
- ^ Chemical Properties - Ohara Corp, 2022-11-22 (באנגלית אמריקאית)
- ^ Reuters, UN warns of looming sand crisis as population and city growth lead to surging demand, ABC News, אפריל 2022
- ^ עובדות מעניינות על זכוכית, באתר הוברמן-סיטונאי אריזות זכוכית
- ^ תהליך מיחזור הזכוכית, באתר פורום המיחזור





