מספר קוונטי זוויתי

במכניקת הקוונטים, מספר קוונטי זוויתי (azimuthal quantum number), הידוע גם כמספר קוונטי אורביטלי, מסומן ב-, הוא השני מתוך 4 מספרים קוונטיים אלקטרוניים המתארים אלקטרון באטום. מספר זה קובע עבור אורביטל אטומי את התנע הזוויתי המרחבי שלו ומתאר את צורת המסלול (אורביטל) או תת-הקליפה האלקטרונית.
היסטוריה[עריכת קוד מקור | עריכה]
המספר הקוונטי הזוויתי נלקח ממודל האטום של בוהר והוצג על ידי ארנולד זומרפלד.[1] מודל בוהר נגזר מניתוח ספקטרוסקופי של האטום בשילוב עם המודל הפלנטרי של רתרפורד. הרמת הקוונטית הנמוכה ביותר נמצאה בעלת תנע זוויתי של אפס. אורביטלים עם תנע זוויתי 0 נחשבו כמטענים מתנדנדים בממד אחד ולכן תוארו כ"אורביטלי מטוטלת".[2] בשלושה ממדים האורביטלים הופכים לכדוריים ואינם מכילים צמתים (nodes) - כמו חבל המתנדנד בדילוגים על פני מעגל גדול.
פיתוח מתמטי[עריכת קוד מקור | עריכה]

משוואת הגלים של שרדינגר ניתנת לפירוק ל-3 משוואות אשר פתרונן (חלקים שונים של פונקציית הגל המהווה וקטור עצמי של ההמילטוניאן) מוביל ל-3 המספרים הקוונטיים האלקטרוניים הראשונים:
המספר הקוונטי הזוויתי נובע מתוך החלק הפולרי של פונקציית הגל, (בהקשר זה, מושגי הזווית המרחבית והאזימוט מובנים יותר כאשר עוברים למערכת קואורדינטות כדוריות).
הערכים העצמיים של אופרטור התנע הזוויתי של האלקטרון באטום, , ניתנים על ידי המשוואה הבאה:
כאשר, הוא קבוע פלאנק המצומצם ו- היא פונקציית הגל של האלקטרון. ערכי משתנים במרווחים שלמים[3] בטווח: , כאשר, הוא המספר הקוונטי היסודי המגדיר את רמת האנרגיה.
בכימיה ובספקטרוסקופיה מקובל לסמן כל סוג אורביטל אטומי באות לטינית בהתאם למספר הקוונטי הזוויתי המתאים:[4]
סוגי האורביטלים נבדלים אחד מהשני בצורתם ובשכיחותם בכל רמת אנרגיה:
- - אורביטל כדורי, קיים אחד כמותו בכל רמת אנרגיה;
- - אורביטל בעל צורה הדומה לשל שעון חול, קיימים שלושה כמותו בכל רמת אנרגיה, אחד לכל ציר במרחב: .
- לאורביטלים הבאים, ו-, צורות מורכבות יותר, כאשר מספר האורביטלים מכל סוג בכל רמת אנרגיה הוא (כאשר מסמן את מספר הסוג).
| רמת האנרגיה |
מספר אורביטלים כולל |
מספר אורביטלי s |
מספר אורביטלי p |
מספר אורביטלי d |
מספר אורביטלי f |
|---|---|---|---|---|---|
| n = 1 | 1 | 1 | |||
| n = 2 | 4 | 1 | 3 | ||
| n = 3 | 9 | 1 | 3 | 5 | |
| n = 4 | 16 | 1 | 3 | 5 | 7 |
פונקציות הגל של האורביטלים הן בעלות צורה של הרמוניה כדורית ולכן מתוארות על ידי פולינומי לז'נדר. האורביטלים השונים המתייחסים לערכי שונים נקראים תת-קליפות אלקטרוניות ומגדירות אכלוס אלקטרונים מקסימלי בצורה הבאה:
| ℓ | אות | מספר אלקטרונים מקסימלי | צורה | שם |
|---|---|---|---|---|
| 0 | s | 2 | ספירה | sharp |
| 1 | p | 6 | 2 משקוליות | principal |
| 2 | d | 10 | 4 משקוליות או צורה ייחודית אחת | diffuse |
| 3 | f | 14 | 8 משקוליות או 2 צורה ייחודיות | fundamental |
| 4 | g | 18 | ||
| 5 | h | 22 | ||
| 6 | i | 26 |

האותיות לאחר ממשיכות בסדר אלפביתי פרט ל- והאותיות שכבר נעשה בהן שימוש. בפועל, 4 האותיות מספיקות על מנת לתאר באופן מלא את כל האטומים שהתגלו עד 2017 המסודרים בטבלה המחזורית.
. ישנן מספר מנמוניקות לסדר זה:
- "Sober Physicists Don't Find Giraffes Hiding In Kitchens Like My Nephew"
- "Smart People Don't Fail"
- "Silly People Drive Fast"
- "silly professors dance funny"
- "Scott picks dead flowers"
- "son pieno di figa"
- "some poor dumb fool"
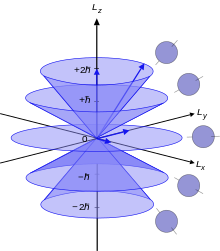
כל אחת מרמות התנע הזוויתי השונות יכולה לאכלס אלקטרונים. הדבר נובע מהמספר הקוונטי השלישי, המספר הקוונטי המגנטי, , אשר משתנה בין ל- במרווחים שלמים ומגדיר מצבים קוונטים אפשריים המבטאים אורביטלים נפרדים ומובחנים. כל אחד מאורביטלים אלו, בעל השלשה הקוונטית: , יכול להכיל עד 2 אלקטרונים עם ספינים הפוכים (המוגדרים על ידי המספר הקוונטי הרביעי, מספר קוונטי ספיני שניוני, ) ולכן בסה"כ כל תת-קליפה אלקטרונית, , יכולה להכיל עד אלקטרונים.
עבור מספר קוונטי יסודי נתון, , ערכי משתנים במרווחים שלמים בטווח: ולכן הרמה הראשונה המכילה תת-קליפת בלבד יכולה להכיל עד 2 אלקטרונים, הרמה השנייה המכילה תתי קליפות ו- יכולה להכיל עד 8 אלקטרונים, הרמה השלישית המכילה את תתי הקליפות , ו- יכולה להכיל עד 18 אלקטרונים וכן הלאה. באופן כללי רמת אנרגיה מסדר יכולה להכיל עד אלקטרונים.
המספר הקוונטי הזוויתי משפיע על מספר הצמתים (nodes) בפונקציית הגל הרדיאלית. הצמתים מתוארות כנקודות האמצע בין אמפליטודות השיא והשפל של גל אלקטרומגנטי. נקודות אלו לא זזות ולכן נמצאות כל הזמן במנוחה. נקודות אלו נוצרות כתוצאה מכך שסכום הגלים העוברים דרכן תמיד מתאפס.
- אורביטל - אין אף נקודת צומת ולכן: .
- אורביטל - ישנה נקודת צומת אחת ולכן: . במקרה זה אורך המיתר הוא: .
בהתאם לערך המספר הקוונטי היסודי, , מקבלים את הרשימה הבאה. אורכי המיתרים המפורטים הם עבור אטום מימן:
- - סדרת ליימן (אולטרא-סגול)
- - סדרת בלמר (אור נראה)
- - סדרת ריץ-פשן (אינפרא אדום)
- - סדרת ברקט (אינפרא אדום קרוב)
- - סדרת פונד (אינפרא אדום בינוני)

ראו גם[עריכת קוד מקור | עריכה]
קישורים חיצוניים[עריכת קוד מקור | עריכה]
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ Eisberg, Robert (1974). Quantum Physics of Atoms, Molecules, Solids, Nuclei and Particles. New York: John Wiley & Sons Inc. pp. 114–117. ISBN 978-0-471-23464-7.
- ^ R. B. Lindsay, Note on “Pendulum” Orbits in Atomic Models, Proc Natl Acad Sci, 6 13, 1927, עמ' 413-419
- ^ Quantum Physics of Atoms, Molecules, Solids, Nuclei, and Particles (2nd Edition), R. Eisberg, R. Resnick, John Wiley & Sons, 1985, ISBN 978-0-471-87373-0
- ^ Molecular Quantum Mechanics Parts I and II: An Introduction to Quantum Chemistry (Volume 1), P.W. Atkins, Oxford University Press, 1977, ISBN 0-19-855129-0








































