טיטניום דו-חמצני – הבדלי גרסאות
אנטרופיה |
אנתלפיית התהווות |
||
| שורה 9: | שורה 9: | ||
| טמפרטורת היתוך = 1,843 |
| טמפרטורת היתוך = 1,843 |
||
| טמפרטורת רתיחה = 2,972 |
| טמפרטורת רתיחה = 2,972 |
||
| אנתלפיית התהוות סטנדרטית = 945- |
|||
| אנטרופיה מולרית תקנית = 50 |
| אנטרופיה מולרית תקנית = 50 |
||
| CAS = 13463-67-7 |
| CAS = 13463-67-7 |
||
גרסה מ־12:50, 31 בינואר 2022
שגיאות פרמטריות בתבנית:תרכובת
פרמטרים [ נוסחה כימית ] לא מופיעים בהגדרת התבנית
 | |
 | |
| כתיב כימי |
TiO₂ |
|---|---|
| מסה מולרית | 79.866 גרם/מול |
| מראה | מוצק לבן |
| מספר CAS | 13463-67-7 |
| צפיפות | 4.23 גרם/סמ"ק |
| מצב צבירה | מוצק |
| טמפרטורת היתוך |
1,843 °C 2116.15 K |
| טמפרטורת רתיחה |
2,972 °C 3245.15 K |
| אנתלפיית התהוות סטנדרטית | 945- קילוג'ול למול |
| אנטרופיה מולרית תקנית | 50 ג'ול למול למעלה |
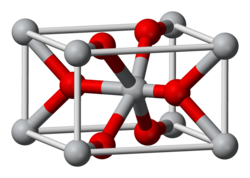
טיטניום דו-חמצני או תחמוצת טיטניום, הידועה גם בשמות טיטניום דיאוקסיד וטיטניה, היא תרכובת כימית של טיטניום וחמצן שנוסחתה TiO2. צורתה הנפוצה ביותר של טיטניום דו-חמצני הוא רוטיל. רוטיל הוא הכינוי למינרל הנפוץ של התחמוצת, ועל שמו קרוי גם המבנה הגבישי (כינוי המבנה הגבישי על שם המינרל הוא מנהג נפוץ, כאשר דוגמה נוספת בולטת הוא הפרובסקיט). במצבה הנפוץ התרכובת היא אבקה לבנה. טיטניום דו-חמצני הוא זרז המשמש לפירוק תרכובות כימיות, ובעיקר פירוק של תרכובות אורגניות. בתעשייה החומר משמש כמרכיב בצבעים, וכתוסף למשחות שיניים או באיפור מינרלי. בשיטת מספרי ה-E, כצבע מאכל, מסומנת התרכובת E171.
תחמוצת הטיטניום נפוצה בטבע בעיקר במינרלים רוטיל (rutile), אנטס (anatase) וברוקיט (brookit), ובצורות נוספות, נפוצות פחות. לתחמוצת הטיטניום מגוון של פאזות בעלות מבנים גבישיים שונים, בהם מבנה טטרגונלי (רוטיל ואנטס), מבנה אורתורומבי (ברוקיט) ומבנים אחרים, מונוקליניים וקוביים.

ניתן לייצר ננוצינורות וננו-סרטים מפאזת האנטס של טיטניה, באמצעות סינתזה הידרותרמית. למבנים אלה יש פוטנציאל לקטליזה ופוטוקטליזה.
קישורים חיצוניים
- טיטניום דו-חמצני, באתר אנציקלופדיה בריטניקה (באנגלית)
