טריפסין
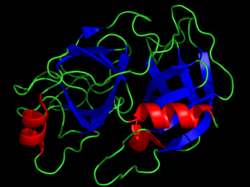
טריפסין, סרין פרוטאז הנמצא במערכת העיכול, שם הוא מפרק חלבונים. האנזים משמש למספר תהליכים ביוטכנולוגיים.
טריפסין מופרש למעיים שם הוא מפרק חלבונים לפפטידים קטנים יותר או לחומצות אמינו. האנזים חשוב לקליטת חלבון במזון. טריפסין מזרז את פירוק הקשרים הפפטידים. ה-pH האופטימלי לפעולת הטריפסין הוא בסביבות 8 וטמפרטורת הפעולה האופטימלית בסביבות 37°C.
שייר חומצה אספרטית (Asp 189) המצוי בכיס הקטליטי של טריפסין אחראי למשיכה וייצוב ארגינין ו/או ליזין הטעונים חיובית וכך הוא אחראי לספציפיות של האנזים. פירוש הדבר שטריפסין חותך לרוב חלבונים בצד הקרבוקסילי (בצד ה-C') של חומצות האמינו ליזין וארגינין, פרט למקרים שבהם לאחר אחת מהן נמצאת החומצה האמינית פרולין. טריפסין נחשב לאנדופפטידאז, כלומר ביקוע החלבון מתבצע בשרשרת הפוליפפטידית ולא בחומצות האמינו בקצה הסופי של הפוליפפטיד.
טריפסין נוצר בלבלב בצורת זימוגן לא פעיל, טריפסינוגן. לאחר מכן הוא מופרש למעי הדק שם האנזים אנטרוקינאז מפעיל אותו והופכו לטריפסין באמצעות פירוק פרוטאוליטי. מולקולות הטריפסין הנוצרות מהתהליך מפעילות בעצמן עוד טריפסינוגנים (אוטוקטליזה), כך שדי בכמות מעטה של אנטרופפטידאז להתחלת התגובה. מנגנון האקטיבציה נפוץ ברוב פרוטאזות הסרין ומשמש למניעת עיכול עצמי של הלבלב.
אחסון טריפסין נעשה בטמפרטורות נמוכות מאוד (בין 20°C- ל 80°C-) וזאת כדי למנוע אוטוליזה (איכול עצמי). ניתן למנוע אוטוליזה גם באמצעות אחסון הטריפסין בסביבת pH של 3.
