קבוצות אנטיביוטיקה
אנטיביוטיקה היא קבוצת תרכובות אורגניות הגורמות למותם או להפסקת התרבותם של חיידקים. את קבוצות האנטיביוטיקה מקובל לחלק לרוב ביוכימית: לכל התרופות המשתייכות לקבוצה מסוימת הרכב כימי וכן דרך פעולה דומים.
קבוצת הפניצילין[עריכת קוד מקור | עריכה]
 ערך מורחב – פניצילין
ערך מורחב – פניצילין

התרופות הנמנות עם קבוצת הפניצילינים נקשרות לחלבונים המכונים penicillin binding proteins (בראשי תיבות- PBP). חלבונים אלו נמצאים בקרום הפנימי של תא החיידק, ותפקידם לייצר את דופן התא. הפניצילינים מעכבים את ייצור דופן תא החיידק אשר מורכב משכבת פפטידוגליקן העוטפת את הקרום הפנימי של תא החיידק. לפעולת החלשת דופן תא החיידק מצטרפת פעולת אנזימי החיידק הקרויים autolysins אשר מזרזת את פירוק הדופן הקיימת של תא החיידק. שתי הפעולות המשולבות הללו גורמות להיחלשות דופן תא החיידק, כתוצאה מכך נכנסים מים לתוך תא החיידק והחיידק מת. מכאן שתרופות אלו הן "בקטריוליטיות" - הורגות את החיידק, גורמות לפירוקו ולא רק מונעות ממנו להתחלק.
קבוצת הצפלוספורין[עריכת קוד מקור | עריכה]
 ערך מורחב – צפלוספורין
ערך מורחב – צפלוספורין
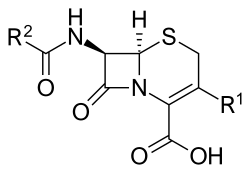
תרופות אנטיביוטיות מקבוצת ה-Cephalosporins הן תרופות, אשר בדומה לקבוצת הפניצילין, מכילות טבעת בטא לקטם. אלו הן תרופות עמידות יותר כנגד האנזים בטא לקטמאז מאשר קבוצות הפניצילין, והן מסוגלות להשמיד זני חיידקים רבים יותר. מקובל לסווג תרופות אלו על פי דורות. הדורות שונים זה מזה ביציבות בפני בטא לקטמאז, ובסוג החיידקים עליהם הן פועלות. כך למשל, ככל שמתקדמים בשלושת הדורות הראשונים, כך היעילות כנגד חיידקים גראם חיוביים מוחלפת ביעילות כנגד גראם שליליים. כיום נמצא בפיתוח דור חמישי אשר צפוי להיות עמיד הן כנגד חיידקים גראם שליליים והן חיידקים גראם חיוביים (ceftobiprole - לטיפול כנגד MRSA).
מנגנוני עמידות לצפלוספורין - תרופות אלו כוללות כאמור טבעת בטא לקטאם, אשר עלולה להינזק על ידי האנזים בטא-לקטמאז (הקרוי כאן צפלוספורינאז) - ישנם חיידקים המייצרים אנזים זה והם עמידים בפני תרופות אלו. בנוסף לשני מנגנוני העמידות הקיימים בפניצילין (שינוי באתר הקישור או ייצור בתא לקטמאז), קיימים שני מנגנוני עמידות נוספים המאפיינים משפחה זו. האחד, ESBL - בטא לקטמאז המסוגל לפרק את כל התרופות מקבוצת הצפלוספורין, והשני - מנגנון עמידות כרומוזומלי הנקרא amp-C - מכיל כמות רבה של גנים שהחיידק רכש במהלך ההיסטוריה, ולכן הסיכוי שחיידק ירכוש מנגנון זה במהלך הטיפול ויהפוך לעמיד הוא אפסי.
קבוצת קרבפנם[עריכת קוד מקור | עריכה]
 ערך מורחב – קרבפנם
ערך מורחב – קרבפנם
תרופות אלו הן הקבוצה השלישית של תרופות המכילות טבעת בטא לקטאם. לתרופות אלו יש פעילות טובה כנגד כמעט כל סוגי החיידקים, לרבות אלו המפתחים עמידות בפני תרופות אנטיביוטיות אחרות. בשל השימוש הגובר בקבוצה זו, עם הזמן מופיעה עמידות גם כנגדה. תרופות אלו ניתנות דרך הווריד בלבד, ומאחר והן רחבות טווח הן משמשות לטיפול בפרפורציה (ניקוב) במערכת העיכול, אשר גורמת לזיהום על ידי מספר חיידקים (כולל חיידקים אנאירוביים, אשר גם הם מכוסים על ידי התרופה).
מנגנוני עמידות לקרבפנם: קיים זן של קלבסיאלה אשר עמיד כנגד התרופות הללו: CRE- carbapenem resistant enterobacteria.
סוגי תרופות[עריכת קוד מקור | עריכה]
- התרופה imipenem היא ממשפחת הקרבפנמים. היא מתפרקת בכליות ולכן ריכוז התרופה הפעילה יורד. השילוב של imipenem יחד עם cilastatin (נקרא tienam) ניתן כדי לעכב את פירוק התרופה: החומר cilastatin מעכב את פירוק התרופה (פוגע באנזים שמיוצר בכליות ושגורם לפירוק התרופה imipenem). בשל זמן מחצית החיים של ה-imipenem, משטר המינון הוא כל 6 שעות.
- meropenem, ertapenem - אלו הן תרופות נוספות ממשפחת הקרבפנם. ה-ertapenem הוא בעל זמן מחצית חיים ארוך יחסית והמינון המקובל הוא אחת ליום.
קבוצת מונובקטם[עריכת קוד מקור | עריכה]
 ערך מורחב – מונובקטם
ערך מורחב – מונובקטם
תרופות מונובקטם נמנות עם הקבוצה הרביעית של תרופות המכילות טבעת בטא לקטאם. באופן עקרוני הן פחות בשימוש, אולם ניתן לתת אותן לחולים המפתחים תגובה אנפילקטית לפניצילין. התרופה aztreonam פעילה נגד חיידקים גראם שליליים והיא עמידה כנגד רוב החיידקים המייצרים את האנזים בטא לקטמאז. תופעות הלוואי הן פגיעה קלה בתפקודי הכבד.
קבוצת גליקופפטידים (ואנקומיצין)[עריכת קוד מקור | עריכה]

התרופה ואנקומיצין (Vancomycin) אינה מכילה טבעת בטא לקטם. מנגנון הפעולה של אנטיביוטיקה זו הוא עיכוב הסינתזה של דופן החיידק בתהליך הקרוי glycopeptide polymerization: התרופה היא גליקופפטיד, שמולקולת המטרה שלה אינה האנזים אשר יוצר קשרים פפטידיים בדופן החיידק, כי אם שרשרת הנקראת muramyl peptide (המהווה את יחידת הבסיס של דופן החיידק). התרופה לא מאפשרת ליצור קשרי הצלבה בין השרשראות של המורמיל פפטיד (נקשר לאזור שבו יש D-ala-D-ala ולא מאפשר המשך הצלבה ליצירת הדופן). תרופות מקבוצה זו יעילות נגד חיידקים גראם חיוביים (בקטריוצידיות - משמידות חיידקים), לרבות זנים העמידים כנגד פניצילין - MRSA.
מנגנוני עמידות לוואנקומיצין: בחיידקים עמידים לתרופה, הפפטידוגליקן הוא במבנה של D-ala-D-lactate, וכך התרופה לא מצליחה להיקשר ולהפריע ליצירת הדופן. חיידקים העמידים לוואנקומיצין נקראים VRE - Vancomycin resistant enterococci. מאחר שוואנקומיצין היא אחת התרופות הבודדות והיעילות נגד סוג החיידקים המסוכן והאלים מסוג סטפילוקוקוס מוזהב (סטפילוקוק אוראוס) הרי שיש להמעיט את השימוש בה כדי למנוע השראה של עמידות. יתרה מכך, כל זיהוי של חיידק עמיד לוואנקומיצין אצל מטופל מחייב בידוד מוחלט של המטופל כדי למנוע העברה של חיידקים עמידים ומסוכנים.
קבוצת הקינולונים[עריכת קוד מקור | עריכה]
 ערך מורחב – קינולון
ערך מורחב – קינולון

קינולון היא אנטיביוטיקה הפוגעת בתהליך שכפול ה-DNA של חיידקים וגורמת לתמותה מהירה שלהם. הקינולונים מעכבים אנזימים חיידקיים המכונים טופואיזומרז-4 או DNA-gyrase, המשתתפים בייצור חומצות גרעין חיידקיות, ומונעים מהם למלא את תפקידם. הקינולונים מאופיינים בספיגה טובה מאוד דרך הפה ומסוננים בשלפוחית השתן, ועל כן קבוצה זו משמשת בין היתר כתרופות לטיפול בדלקות הנגרמות בדרכי השתן.
קבוצת הטטרציקלינים[עריכת קוד מקור | עריכה]
 ערך מורחב – טטרציקלין
ערך מורחב – טטרציקלין
התרופות הנמנות עם משפחת הטטרציקלינים (נקראות כך היות שכוללות ארבע טבעות hydrocarbon) מונעות את ייצור החלבון בתא החיידק. אלו הן תרופות אשר מעכבות ומונעות את ריבוי החיידקים (ומכאן שאינן בקטריוצידיות אלא בקטריוסטטיות), והן בעלות פעילות רחבת טווח כנגד חיידקים (גראם שליליים וגראם חיוביים). באופן פרטני, תרופות אלו מונעות את היקשרותו של aminoacyl tRNA ל-mRNA ribosome complex. הן עושות זאת על ידי היקשרות ליחידה 30S (תת-היחידה הקטנה של הריבוזום), וספציפית ב-site A של הריבוזום. בדרך זו נמנע תהליך ייצור החלבון.
קבוצת האמינוגליקוזידים[עריכת קוד מקור | עריכה]
 ערך מורחב – אמינוגליקוזיד
ערך מורחב – אמינוגליקוזיד
קבוצת האמינוגליקוזידים, בדומה לקבוצת הטטרציקלינים, פועלת על ידי פגיעה בייצור חלבוני החיידק - Bacterial protein synthesis inhibitors- אמינוגליקוזידים נקשרים ליחידה 30S בריבוזום (בדומה לטטרציקלינים), וגורמים לבעיות בתהליך התרגום עצמו של החלבון (למשל, פגיעה ב-proofreading process, אשר גורמת לטעויות רבות וטרמינציה מוקדמת מדי של החלבון). במרבית המקרים פעילותם היא בקטריוסטטית בלבד, ואולם אם ריכוזם עולה הם הופכים להיות בקטריוצידיים (החלבון הפגום מביא למות החיידק). ההסבר לפעילותם הבקטריוצידית הוא שנמצא כי חלקים קטיוניים במולקולת התרופה גורמים לחורים בממברנה החיצונית של התא, ויוצרים דליפה של תוכן תוך-תאי החוצה, דבר המזרז את מות החיידק. אלו הן תרופות בעלות טווח פעולה צר, יעילותן היא בעיקר כנגד חיידקים מסוג גראם שליליים. תרופות אלו יעילות במיוחד כנגד חיידקים אירוביים (כגון פסאודומונס), וכנגד חיידקי המעיים. תרופות אלו חייבות לחדור מבעד לקרום התא בתהליך הדורש חמצן ואנרגיה, ועל כן חיידקים אנאירוביים עמידים כלפי תרופות אלו. חדירת תרופות אלו לתוך תא החיידק מתאפשרת ביתר קלות באמצעות תרופות החוסמות את ייצור דופן תא החיידק, ועל כן שילוב של תרופות אלו בשילוב עם תרופות הפוגעות בייצור דופן התא (כגון פניצילין וואנקומיצין) מגבירה את השפעתן (סינרגיסטית). קיים שילוב נפוץ יחסית של אמפיצילין וגנטמיצין (gentamicin - סוג של אמינוגליקוזיד) הניתן במקרים כגון אנדוקרדיטיס.[יש לציין כי ע"פ ברונר, אין לתת באותה תמיסה יחד עם תרופות המכילות בטא לקטאם מחשש לתגובה כימית].
גורמי עמידות לאמינוגליקוזידים - העמידות לתרופה מקודדת על ידי פלסמיד בתא החיידק, אשר מבצע מודיפיקציות על האנטיביוטיקה, כגון אצטילציות, פוספורילציות או אדנילציות, המונעות ממנה להיקשר לריבוזום.
תרופות אלו משמשות בעיקר לטיפול בזיהומים הנגרמים בדרכי השתן או במעי. הן יעילות כנגד חיידקים גראם שליליים כגון E. coli, פסאודומונס, קלבסיאלה.
קבוצת המקרולידים[עריכת קוד מקור | עריכה]
קבוצת המקרולידים פועלת באמצעות מניעת ייצור חלבוני החיידק - Bacterial protein synthesis inhibitors, ואולם שלא בדומה לטטרציקלינים ולאמינוגליקוזידים, קבוצה זו נקשרת ליחידה 50S (ולא 30S) על גבי הריבוזום של החיידק, ומעכבת את סינתזת החלבון. תרופות אלו הן בעלות טווח פעילות רחב, ובעלות פעילות אנטיביוטית דומה לזו של הפניצילין. הן יעילות גם עבור חיידקים חסרי דופן, חיידקים אשר עמידים לפניצילין וחיידקים אשר אין להם כיסוי אנטיביוטי אחר. תרופות אלו יעילות גם כנגד חיידקים גראם חיוביים (למעט סטפילוקוקוס אוראוס).
מנגנוני עמידות למקרולידים- מנגנון העמידות העיקרי הוא מתילציה על גבי הריבוזום (בתהליך פוסט-שעתוק) המפריעה להיקשרות התרופה. לעיתים העמידות נוצרת כבר במהלך הטיפול עצמו.
התוויות טיפוליות[עריכת קוד מקור | עריכה]
תרופות אלו ניתנות בין היתר במקרים הבאים:
- זיהומים הנגרמים על ידי סטרפטוקוקים
- עגבת, מחלת ליים
- זיהומים בדרכי הנשימה, דלקת ריאות
סוגי התרופות השונים[עריכת קוד מקור | עריכה]
תרופות ידועות ממשפחת המקרולידים הן אריתרומיצין, קלריתרומיצין (בעלת זמן מחצית חיים ארוך יותר מאריתרומיצין), ואזיתרומיצין (זמן מחצית חיים ארוך).
תופעות לוואי[עריכת קוד מקור | עריכה]
תופעות הלוואי כוללות בחילות, הקאות וכאבי בטן, וכן פגיעה חולפת בכבד (יש לבחון את תפקודי הכבד).
קבוצת sulfonamides[עריכת קוד מקור | עריכה]
הסולפונאמידים (נקראים גם "תרופות סולפה") הן התרופות האנטיביוטיות הראשונות טרם גילוי הפניצילין. תרופת הסולפה הראשונה נקראה prontosil והיא נוסתה לראשונה בשנת 1932. לאחר מכן נעשה שימוש נרחב בתרופות אלו במהלך מלחמת העולם השנייה. קבוצה זו של אנטיביוטיקות מעכבת את ייצור החומצה הפולית בחיידק. תרופות אלו הן בעלות מבנה הדומה למרכיב המכונה PABA או Para aminobenzoic acid, הדרוש לחיידקים כדי ליצור את החומצה הפולית אשר הכרחית לקיום החיידק. החיידק אינו יכול לקבל חומצה פולית מהמאכסן, אלא הוא חייב לייצר אותה מה-PABA. תרופות סולפונאמידיות כאמור מתחרות ב-PABA, באופן בו הן מעכבות בצורה תחרותית את האנזים dihydropteroate synthase, אשר הופך את PABA לשלב ביניים של החומצה הפולית (הקרוי dihydrofolinic acid). החשיבות של חומצה פולית היא בתרומתה ליצירת חומצות גרעין. בהיעדרה, תאים לא יוכלו להתחלק. לתרופות אלו יש פעילות טובה הן כנגד חיידקים גראם שליליים והן כנגד חיידקים גראם חיוביים, ובמינון המקובל מושגת פעילות בקטריוצידית ההורגת את החיידק.
מנגנוני עמידות לסולפונאמידים: המנגנון הידוע לפיתוח עמידות לסולפונאמידים הוא רכישת גן המקודד על גבי פלסמיד, אשר מייצר אנזים שאינו רגיש לתרופה (האנזים dihydropteroate synthase).
התוויות טיפוליות[עריכת קוד מקור | עריכה]
כאמור, לתרופות הסולפונאמידים יש תגובה טובה כנגד חיידקים גראם חיוביים וגראם שליליים, ובמיוחד כנגד חיידקים מסוג e.coli, ולכן התרופה טובה לטיפול כנגד דלקות בדרכי השתן.
סוגי התרופות השונים[עריכת קוד מקור | עריכה]
ניתן לחלק את תרופות הסולפה על פי זמן מחצית החיים. בין התרופות הקיימות, ניתן למנות:
- sulfamethoxazole (בקיצור SMX), שם מסחרי Gantanol: זמן מחצית החיים של תרופה זו נע בין 10-24 שעות, מאפשר מינון של פעם ב-12 שעות.
- sulfisoxazole (שם מסחרי gantrisin): זמן מחצית החיים של תרופה זו קצר יותר, בין שעתיים לשבע שעות (מאפשר מינון של פעם ב-6 שעות).
תופעות לוואי[עריכת קוד מקור | עריכה]
תופעות הלוואי בשימוש בסולפונאמידים כוללות בין היתר תגובה מסוג רגישות יתר (הכוללת תפרחת, חום, פוטוסנסטיביות), פגיעה בכליות (התרופה שוקעת בכליות וסביבה החומצית של השתן - crystalluria - נוצרים גבישים בשתן, ועל כן יש להקפיד על שתייה מרובה). כמו כן, התרופה יכולה להביא לירידה בספירת תאי הדם הלבנים, ולהרגשה כללית רעה הכוללת בחילות ושלשולים. אין לתת תרופה זו לנשים בהיריון ולילודים, היות שהתרופה נקשרת לחלבוני הדם, ודוחקת החוצה את הבילירובין. מאחר שמחסום דם־מוח אצל ילודים ועוברים איננו מפותח עדיין, הבילירובין עלול להגיע לתאי המוח ולפגוע בהם, ולגרום לשיתוק מוחין, חירשות, הפרעות בראייה וקשיי דיבור (נקרא גם "צהבת מוחית של הילוד" או kernicterus).
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- הערך "קבוצות אנטיביוטיקה", באתר "ויקיתרופות"
- הערך "קבוצות אנטיביוטיקה", באתר ויקירפואה
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.
