שיטות חלבונים
שיטות חלבונים הן טכניקות המשמשות ללימוד ולבדיקה של חלבונים. השיטות משמשות למחקר ביולוגי בסיסי ולצורך אבחון רפואי. מאחר שלכל שיטה יתרונות וחסרונות משלה, שיטות שונות משמשות למטרות שונות, ופעמים רבות יש צורך להשתמש ביותר משיטה אחת לקבלת התוצאה הרצויה.
חשוב להדגיש כי לכל שיטה וריאציות בהתאם לטיב המכשור והחומרים העומדים לרשות המעבדה המבצעת את הניסויים ובהתאם לאופי החלבון הנחקר. במקרים מסוימים השיטות המהוות המשך ניסויי אחת של קודמתה, ולכן לעיתים הן נחשבות לשלבים שונים באותה השיטה.
שיטות גנטיות[עריכת קוד מקור | עריכה]

- ריצוף קונספטואלי: רצפם של רוב החלבונים לא נקבע באופן ישיר, אלא מוסק מרצף ה mRNA על ידי שימוש בקוד הגנטי. בגלל מודיפיקציות שלאחר השעתוק לא תמיד הריצוף הקונספטואלי מספיק לריצוף החלבון בצורתו הפעילה.
- מוטגנזה מכוונת: שינוי רצף ה-DNA המקודד לחלבון באתר ספציפי - בדרך כלל שינוי הגורם לשינוי בחומצה אמינית אחת או הורדת דומיין חלבוני. השיטה מבוצעת על ידי שימוש בפריימרים המכילים את המוטציה בתגובת PCR. לאחר מכן מיוצר פלסמיד המכיל את הגן המוטנטי, הפלסמיד מוחדר לתא אאוקריוטי או לחיידק ושם מיוצר החלבון המוטנטי. מעקב אחרי פעילותו של החלבון המוטנטי ביחס לחלבון הנורמלי מאפשר להבין את חשיבותה של החומצה האמינית או הדומיין שהוחלפו לפעילותו הנורמלית של החלבון.
- חלבון כימרי: שימוש בהנדסה גנטית ליצירת חלבון כימרי המכיל את החלבון הנחקר ואלמנט קטן הניתן למעקב כמו His-TAG או חלבון פלואורסצנטי GFP. באופן זה ניתן לראות את האברון שבו נמצא החלבון בתא ולדעת עם אילו חלבונים אחרים הוא מגיב.
- ניתוח פילוגנטי של חלבונים: על פי תורת האבולוציה, במשך הזמן משתנים רצפי ה-mRNA המקודדים לחלבון. לפיכך יש הבדלים בין חלבונים אורתולוגים מיצורים שונים (לדוגמה המוגלובין מאדם, מעכבר ומדג). חלקים שונים של החלבון נוטים לעבור שינויים אבולוציוניים בתדירויות שונות, האתר הפעיל בחלבון נחשב לאזור השמור ביותר בין בעלי חיים שונים, כך ניתוח פילוגנטי מאפשר זיהוי אזורים חשובים בחלבון ורומז על תפקידו.
- מחלות גנטיות: מרבית המחלות הגנטיות הן תולדה של מצבים בהם חלבון שאינו תקין (מוטנטי) עובר בתורשה. על ידי מציאת החלבון הלא תקין ואפיון הסימפטום שהוא גורם ניתן להסיק על הפעילות הנורמלית של החלבון.
גילוי חלבונים[עריכת קוד מקור | עריכה]
קביעת כמות חלבון[עריכת קוד מקור | עריכה]
- קביעת חלבון בעזרת בליעת UV: חלבון בעל טבעות ארומטיות קולט קרינת UV באורך גל של 280nm. כדי למצוא את כמות החלבון יש להכפיל את הבליעה האורך הגל 280nm בקבוע הבליעה של החלבון ולחלק באורך שהקרן עוברת בתמיסה (1 סנטימטר). להערכה גסה של כמות חלבונים התערובת קבוע הבליעה הוא mgr*cm/ml 1.55 .
- הבדיקה מהירה ונוחה, אינה מצריכה הכנת עקום כיול ואינה הורסת את החלבון. החסרונות שבשיטה הם שלכל חלבון קבוע בליעה שונה, ולכן יש להכיר את קבוע החלבון הספציפי שאותו מעוניינים למדוד. ברור שהשיטה הופכת ללא מדויקת כאשר יש ניסיון למדוד ריכוז חלבונים בתערובת כמו סרום. כמו כן אסור שבתמיסה יהיו אלמנטים קולטי קרינה אחרים כמו חלקיקים שאינם מומסים או חומרי צבע.
- השיטה משמשת בעיקר כאשר אין צורך לדעת בדיוק את כמות החלבון, למשל בפרקציות היוצאות מעמודת הפרדה, או כאשר מכמתים חלבון יחיד וידוע כמו אלבומין.
- שיטת ברדפורד: כתוצאה מערבוב תמיסה שבה מומסים חלבונים (כגון סרום או ליזת תאים) ותמיסת ברדפורד, משנה התמיסה את צבעה והופכת לכחולה. ניתן למדוד את שינוי הצבע בעזרת ספקטרופוטומטר באורך גל 595nm וכך לקבוע את כמות החלבון. השיטה אינה ספציפית לחלבון מסוים אלא קובעת את ריכוז החלבון הכללי בתמיסה. השיטה מצריכה עקום כיול, ולכן נחשבת מסורבלת יותר משיטת הכימות בעזרת UV. יחד עם זאת השיטה מדייקת יותר בקביעת ריכוז חלבון בתערובת חלבונים, ופשוטה יותר למדידת דוגמאות רבות.
גילוי חלבון ספציפי[עריכת קוד מקור | עריכה]

- תספיג חיסוני Immunoblot: זוהי השיטה הבסיסית למציאת חלבון. השיטה מבוססת על הספגת החלבון על ממברנת ניטרוצלולוזה, חשיפת הממברנה לנוגדן ראשוני נגד החלבון, לאחר מכן לנוגדן שניוני נגד הנוגדן הראשוני המוצמד לאנזים HRP, הוספת סובסטרט שהמגע עם HRP פולט אור וחשיפה לסרט צילום.
- תספיג נקודתי: כאשר דוגמת החלבון מושמת על הממברנה ללא הפרדה באלקטרו פורזה השיטה נקראת תספיג נקודתי - היתרון בשיטה היא החיסכון בזמן וכמות הדוגמאות הרבות שניתן לבדוק בניסוי אחד.
- תספיג חלבון (Western blot): הפרדת חלבונים על יד ג'ל אלקטורפורזה, בדרך כלל על ידי SDS PAGE (לעיתים נדירות על ידי 2D ג'ל), לאחר שהחלבונים הופרדו על פי גודל או מטען חשמלי מועברים החלבונים מן הג'ל לממברנת ניטרוצלולוזה על ידי הפעלת שדה חשמלי. הממברנה עוברת תספיג חיסוני. היתרון בשיטה הוא שניתן לדעת את גודל החלבון הנבדק לכן פוחת חשש שהנוגדן נספח גם לחלבונים אחרים ועולה יעילות הבדיקה.

- ELISA ראשי תיבות של Enzyme-Linked Immunosorbent Assay - בדיקת צבע אנזימטית קשורה לנוגדן: טכניקה לגילוי אנטיגנים (לאו דווקא חלבונים) בתמיסה. באופן בסיסי הבדיקה מבוססת על בסיס קשיח- בדרך כלל פלסטיק, אליו נספחים אנטיגנים (בדרך כלל חלבונים). לאחר מכן נעשה שימוש לפחות בשני סוגים של נוגדנים: נוגדן ראשוני ספציפי לאנטיגן מסוים ונוגדן שניוני הנקשר לנוגדן הראשוני ומצומד לאנזים. כאשר סובסטרט בא במגע עם האנזים, הוא משנה את צבעו וכך נותן אינדיקציה לנוכחות האנטיגן, הוספת חומצה חזקה כמו חומצה גופרתית מסיימת את הראקציה. כמות הצבע שנוצרה נמדדת על ידי ספקטרופוטומטר באורך גל מתאים, בצורה זאת ניתן לכמת אנטיגן ספציפי.
- שיטת ELISA נחשבת לשיטה המדויקת ביותר לגילוי חלבונים. לשיטה עשרות וריאציות בהתאם לאופי החלבון הנבדק - ניתן לבדוק את נוכחותם של נוגדנים בסרום כמו בבדיקת HIV, ניתן לשפר מאוד את רגישות הבדיקה על ידי ספיחת נוגדן ראשוני לבסיס המוצק.

- אימונוהיסטוכימיה: צביעת רקמה מקובעת על זכוכית נושא (סלייד). על הסלייד מונח נוגדן ראשוני נקשר לחלבון הרצוי, לנוגדן הראשוני נקשר נוגדן שניוני המצומד לאנזים HRP, כאשר סובסטרט שמוסף בא במגע עם החלבון הוא משנה את צבעו וצובע את הרקמה - היתרון בשיטה הוא שנשמרת המורפולוגיה של הרקמה, השיטה משמשת לאבחון סרטן ובמקרים מסוימים את דרך הטיפול במחלה. החיסרון בשיטה היא שקביעת החלבון אינה כמותית בדרך כלל, ורגישותה נמוכה ביחס לשיטות אחרות, כמו כן השיטה חשופה לצביעת רקע לא ספציפית.

- אימונופלואורסצנציה - שימוש בצביעה על ידי חומרים פלואורסצנטיים. השיטה מאפשרת בדיקת מספר חלבונים שונים כאשר כל חלבון מוכר על ידי נוגדן בצבע אחר. השיטה גם מאפשרת שימוש במיקרוסקופ קונפוקלי המאפשר "חיתוך" האובייקט המצולם לשכבות בעובי של 0.1 מיקרון, כך מספיקה כמות קטנה של חלבון וניתן לראות באיזה מאברוני התא הוא ממוקם.

- Flow Cytometry - זרימה ציטומטרית: מונח המתייחס לטכניקות לבדיקת המבנה הפיזי והכימי של התאים. בהקשר של גילוי חלבונים, השיטה מבוססת על ערבוב נוגדנים פלואורסצנטיים, ספציפיים לחלבון מסוים, עם אוכלוסייה של תאים או חיידקים, ובדיקת הפלואורסצנציה הנפלטת מכל תא.
- היתרון בשימוש ב-Flow Cytometry הוא שניתן להעריך את ביטוי החלבון על התא ולבחון אם יש יותר מאוכלוסיית תאים אחת, כלומר האם רמת הביטוי של חלבון ספציפית שונה בין תאים שונים. השיטה יעילה לגילוי חלבונים המוצגים על פני הממברנה או בתוך התא (לגילוי חלבונים תוך תאיים יש לחורר את הממברנה תחילה) אך לא חלבונים מופרשים.
- ניסויים אנזימטיים: ניסויים המבוססים על פעולתו הקטליטית של חלבון, ניסויים אלו מבוססים על מעקב לאורך זמן אחרי כמויות סובסטרט או תוצר הבאים במגע עם אנזים. ניסויים אנזימטיים משמשים למציאת הקינטיקה של תרופות לפני התחלה בניסויים בבעלי חיים ובבני אדם.
- Peptide mass fingerprinting - טביעות אצבעות של מסה פפטידית (או ספקטרומטרייה של מסה): שיטה המאפשרת לזהות חלבונים לפי המסה שלהם - חלבון שרצפו אינו ידוע מנוקה ומסתו נקבעת בעזרת ספקטרומטר מסה (mass spectrometer). בהמשך החלבון נחתך לפפטידים בעזרת אנזים פפטידאז כמו טריפסין, גם מסתם של הפפטידים נקבעת על ידי הספקטרומטר. משקלם של הפפטידים והחלבון השלם מוכנסים למאגר נתונים המכיל נתונים על כל החלבונים הידועים מפרויקט הגנום (חלבונים אלו רוצפו ריצוף קונספטואלי- ראו לעיל), אם החלבון נמצא במאגר הממוחשב הוא יזוהה.
- היתרונות שבשיטה הם שאין צורך בשימוש בנוגדנים ספציפיים לחלבון כך שניתן לקבוע את ריצפו של חלבון ללא ידע מוקדם, כמו כן רק מסת החלבון נקבעת וכך אין צורך בריצוף חדש (de novo). החסרונות שבשיטה הם שהחלבון צריך להופיע במאגר הנתונים, וכדי שהשיטה תהייה יעילה החלבון צריך היות נקי לחלוטין.
בידוד חלבונים[עריכת קוד מקור | עריכה]
ריכוז וניקוי חלבונים[עריכת קוד מקור | עריכה]

- דיאליזה: דיאליזה מבוססת על ההבדל ביכולתם של חומרים שונים לחדור מבעד ממברנות סינתטיות. כאשר תמיסה מכילה פרט לחלבון אותו מעוניינים לחקור גם מלחים, מולקולות קטנות או חלבונים קטנים ניתן לנקות את החלבון בעזרת דיאליזה. התמיסה מוכנסת לשקית ממברנה המאפשרת מעבר למולקולות מסוימות (בדרך כלל רק למולקולות קטנות), השקית מוכנסת לכלי גדול המכיל תמיסה עם ריכוז המלחים אליו מעוניינים להגיע, הכלי בו נמצאות התמיסות מעורבל לאורך זמן. בשיטה זאת בסוף התהליך רק החלבונים שאינם עוברים בממברנה נותרים בשקית הדיאליזה, ריכוז החלבונים שאינם עוברים את הממברנה אינו משתנה.

- ריכוז חלבונים בעזרת פילטר: השיטה מבוססת על ההבדל ביכולתם של חלבונים בעלי גודל שונה לעבור דרך פילטר, כדי לזרז את התהליך התמיסה מסורכזת בצנטריפוגה בכבידה של עד עשרות אלפי g. מים, מלחים, מולקולות קטנות וחלבונים קטנים יוצאים מן התמיסה, חלבונים גדולים מן החרירים שבפילטר אינם עוברים וכך ריכוזם של חלבונים אלו עולה. לכל מכשיר ריכוז מוגדר cut off size, הגודל המרבי של חלבונים היכולים לעבור את הפילטר, אם הפילטר יעיל לא יעברו חלבונים גדולים מן הגודל המוגדר. כדי להיפטר באופן יעיל יותר מן החלבונים הקטנים ניתן, לאחר מחזור של ריכוז, לדלל מחדש את הדוגמה ולרכז שוב.
- בניגוד לדיאליזה ריכוז חלבונים בעזרת פילטר אינו מבוסס על מעבר מולקולות באופן דו כיווני דרך ממברנה אלא על מעבר חד כיווני. שוני נוסף הוא שריכוז המלחים בתמיסה אינו משתנה בריכוז על ידי פילטר בניגוד לדיאליזה.
- השקעת חלבון בעזרת אמוניום סולפט: אמוניום סולפט הוא מלח קל תמס, היוצר קשרים פולרים עם מים, בכך זמינות המים יורדת כך שהמים אינם יוצרים קשרים בין מולקולריים עם החלבונים (מיסוך מטענים), ללא קשרים אלו החלבון הופך למוצק ושוקע. ניתן להפריד בין התמיסה לחלבון המוצק על ידי סרכוז.
- מכיוון שכל חלבון שוקע בריכוז אמוניום סולפט אופייני (ריכוז קריטי) ניתן לשלוט בתהליך כדי להעשיר את כמותו של חלבון ספציפי, וזאת בשני שלבים - ראשית להשקיע ולהוציא חלבונים שהריכוז הקריטי שלהם נמוך מזה של החלבון הרצוי. לאחר מכן להשקיע בריכוז הקריטי של החלבון הרצוי. בדרך כלל לאחר ההשקעה החלבונים מומסים שנית ומנוקים בדיאליזה כדי להיפטר משאריות אמוניום סולפט.
- השיטה יעילה מאוד בריכוז והעשרה של תמיסות חלבונים, החיסרון שבשיטה הוא שהניקוי אינו מלא - אם בתמיסה חלבונים בעלי ריכוז קריטי קרוב ההפרדה לא תהיה מלאה. חיסרון נוסף בשיטה היא שהשקעת חלבונים עלולה לפגוע בתפקוד החלבון.

- Immunoprecipitation אימונו פרסיפיטציה: השקעת חלבון על ידי נוגדן, טכניקה המאפשרת בידוד מתוך תמיסה של חלבון ספציפי או קומפלקס חלבונים.
- לתוך תמיסת חלבונים מוכנסים נוגדנים הנקשרים לאחד החלבונים, לתמיסה מוכנס חלקיק בלתי מסיס הקושר נוגדנים בזכות הקישור הופך הקומפלקס כולו לבלתי מסיס, ניתן להפריד את המשקע הבלתי מסיס מן התמיסה על ידי סרכוז (בצנטריפוגה). בהמשך מפורק הקומפלקס מן החלקיק הבלתי מסיס, לרוב על ידי חשיפה קצרה ל pH חומצי.
- התהליך יעיל בזיהוי חלבונים הנמצאים בתצמיד כאשר ידוע חלבון אחד, ההמשך ניתן לזהות חלבונים אחרים הנמצאים בתצמיד על ידי שיטות אחרות כמו תספיג חלבון או ספקטרומטריית מסה.
- Salting out: שיטה להפרדת חלבונים המבוססת על עקרון שחלבונים פחות מסיסים בריכוזים גבוהים של מלחים. כאשר ריכוזי המלח גדולים, אחדות ממולקולות המים נמשכות על ידי יוני המלח אשר מפחיתות את מספרן של מולקולות המים הזמינות לאינטראקציות עם החלק הטעון של החלבון. כתוצאה מהביקוש הגדול למולקולות המסיסות, האינטראקציות בין חלבונים חזקות יותר מאשר אינטראקציות בין ממס למומס.
הפרדת חלבונים על ידי אלקטרופורזה בג'ל[עריכת קוד מקור | עריכה]
על ידי שדה חשמלי ניתן להפריד מולקולות על פי מאפיינים פיזיקליים כמו גודל, משקל, או מטען חשמלי. המולקולות מונחות על ג'ל, ושדה חשמלי שמופעל גורם למולקולות לנוע בג'ל בהתאם למטענן החשמלי. בהקשר להפרדות חלבונים ניתן להשתמש בשיטה כדי לאפיין שני משתנים: גודל החלבון ומטענו.
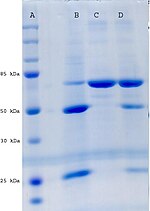
- SDS-PAGE: השיטה המקובלת ביותר למציאת גודלם של חלבונים היא על ידי SDS-PAGE: Sodium Dodecyl Sulfate Polyacrylamide Gel Electrophoresis השיטה מבוססת על הרתחת חלבונים ב-סודיום דודציל סולפט - מולקולת דטרגנט טעונה שלילית. SDS פותח את המבנה המרחבי של החלבונים ונותן לכל החלבונים בדוגמה מטען שלילי. הדוגמה מונחת על ג'ל פוליאקרילאמיד ליד האלקטרודה השלילית, עם הפעלת שדה חשמלי החלבונים נעים לכיוון האלקטרודה החיובית. החלבונים מופרדים מאחר שחלבונים כבדים נעים בג'ל לאט יותר מחלבונים קלים. לאחר ההפרדה ניתן לצבוע את כלל החלבונים בג'ל בשיטת קומסי (Coomassie blue) או בצביעת כסף (Silver staining). לחלופין ניתן למצוא חלבון ייחודי בעזרת תספיג חלבון (ראו לעיל).
- מיקוד איזואלקטרי Isoelectric focusing: שיטה המבוססת על אלקטרופורזה של חלבונים למציאת הנקודה האיזואלקטרית. דוגמת חלבונים מונחת על ג'ל פוליאקרילאמיד ללא SDS. מכיוון שהחלבונים לא עברו טיפול ב-SDS מטענם החשמלי וכושר התנועה שלהם בשדה החשמלי נקבעים על פי רצף חומצות האמינו בלבד. הג'ל בנוי בגרדיאנט pH, כאשר חלבון מגיע ל-pH הנמצא בנקודה האיזואלקטרית הוא מאבד את מטענו החשמלי ובכך מאבד את כושר התנועה.

- ג'ל דו־ממדי: שיטה להפרדת חלבונים בשני ממדים ועל פי שני קריטריונים. הקריטריונים הנבדקים הם הנקודה האיזואלקטרית והמסה, כיוון שיש סבירות נמוכה ששני חלבונים שונים הם זהים במסתם ובמטענם חשמלי, עולה יכולת ההפרדה של השיטה ביחס לשיטות החד־ממדיות (SDS-PAGE או הפרדת חלבונים על גרדיאנט).
- בשיטה זאת תערובת של חלבונים מופרדת תחילה באלקטרופורזה על גבי רצועת פוליאקרילאמיד בעלת גרדיאנט pH, החלבון מפסיק לנוע כאשר הוא מגיע לאזור שם הpH- זהה לנקודה האיזואלקטרית של החלבון. בהמשך נטבלת הרצועה ב-SDS ומונחת על ג'ל פוליאקרילאמיד עם SDS, שדה חשמלי שמופעל בזווית 90o מן הרצועה מפריד את החלבונים לפי מסה.
