HIV נגד לוקמיה
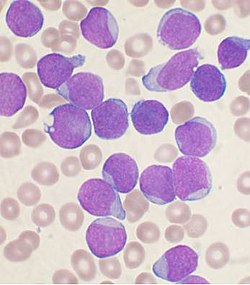
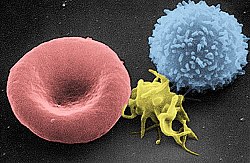

HIV נגד לוקמיה היא שיטה של ריפוי גני לטיפול בסרטן הדם, בעזרת נגיף HIV, רטרו וירוס הגורם למחלת האיידס (תסמונת הכשל החיסוני הנרכש). הנגיף "מהונדס", בצורה כזו שהוא מצדו "מהנדס" תאי לימפוציט T בדם והופך אותם לקטלניים כנגד הסרטן. בהתבסס על הצלחות של ניסויים בשיטה זו במהלך 2011 ו-2012, פיתחה חברת התרופות נוברטיס הליך בשם Tisagenlecleucel המשתמש בנשא נגיפי סינתטי[1] (במקום בנגיף HIV), המיוצר על ידי חברת אוקספורד-ביומדיקה. ההליך האחרון אושר על ידי ה-FDA האמריקאי[2] ב-30 באוגוסט 2017 והיה בכך להליך הראשון המאושר על ידי מנהל המזון והתרופות האמריקאי[3][4], הכולל שלב של ריפוי גני.
תיאור כללי של השיטה[עריכת קוד מקור | עריכה]
פרופסור קרל ג'ון מאוניברסיטת פנסילבניה הינדס את נגיף ה-HIV הגורם לאיידס, בצורה שהופכת אותו ללא מסוכן מחד גיסא, אך שומר במקביל על יכולתו להכניס גנים לתוך תאי לימפוציט T, מאידך גיסא. בעזרת נגיף מהונדס זה, הוא הכניס ללימפוציטי T, גנים, שגרמו להם להשמיד את תאי לימפוציט B, שהם הלימפוציטים החולים במחלת הלוקמיה. הטיפול נוסה בשלב ראשון על שלושה חולים סופניים, כעבור כשנה על תשעה חולים סופניים נוספים[5][6] וב-2016 הורחב לאור התוצאות הטובות של שלביו הראשונים.
פירוט[עריכת קוד מקור | עריכה]
העיקרון המנחה את השיטה הומצא בסוף שנות השמונים, על ידי פרופסור זליג אשחר, המכהן (נכון ל-2013) כראש המחלקה לאימונולוגיה במכון ויצמן למדע. אשחר הינדס תאי לימפוציט T, בשיטות שונות של הנדסה גנטית, כך שיצוידו בקולטנים ספציפיים, שיאפשרו להם להרוג תאי מטרה סרטניים ספציפיים[7][8][9]. עם זאת, השיטה שהמציא אז, הייתה יקרה, מסובכת, לא נחלה הצלחה בכל פעם שנוסתה ודרשה שיפורים מעשיים רבים. אחת הסיבות לכך הייתה אולי משום שאשחר לא חשב על השימוש בנגיפי HIV, אשר עצם גילויים היה חדש אז.
מאז ראשית שנות האלפיים פועלים מספר צוותי חוקרים ממספר מוסדות מחקר, בעיקר אמריקאיים, לשפר את השיטה של אשחר, לפשטה ולהוזילה. אחד הצוותים הללו נמצא בחברת קייט פארמה, אשר נרכשה באוגוסט 2017 על ידי גיליאד סיאנסז תמורת כ-12 מיליארד דולר. הצוות שם שיפר את שיטתו של זליג אשחר בצורה מסוימת אחת. צוות החוקרים מאוניברסיטת פנסילבניה, בראשות דוקטור קרל ג'ון שיפר את שיטתו של אשחר בדרך אחרת. הם השתמשו בנגיף איידס (HIV) מוחלש, כדי לגרום לשינויים הרצויים בתאי T. הייחוד של נגיף האיידס בהקשר זה, הוא יכולתו הטבעית לחדור לתאי T ולהזריק ל-DNA שלהם גנים משלו. תאי T הם תאי המטרה של HIV בטבע.
ג'ון וצוותו קיבלו ב-2010 את הסכמתם של שלושה חולי לוקמיה לימפוציטית כרונית מבוגרים, להיות הנסיינים האנושיים הראשונים של השיטה. שלושת החולים נמצאו במצב שבו הכימותרפיה כשלה בריפוי מחלתם ולא נותרה תקווה ממשית להצילם. החוקרים שאבו מגופו של כל אחד מן החולים, בין כמה עשרות מיליוני תאי T ועד כמיליארד תאים והרכיבו לתוך ה-DNA שלהם, בעזרת נגיף HIV מוחלש, גנים ליצירת קולטנים ספציפיים מתאימים. אחר כך הם הזריקו את תאי T המהונדסים של החולים, חזרה לגופם. לפני ההזרקה הזו חזרה, הושמדו כל תאי T הבלתי מהונדסים שנותרו בדמו של החולה, כדי למנוע מלחמה בין התאים המהונדסים לאלה הטבעיים.
עשרה ימים לאחר ההזרקה סבלו החולים במשך מספר שבועות מקדחת חום קשה ולחץ דמם ירד מאוד, עד כדי כך שהם נמצאו בסכנת חיים של ממש. אולם בסוף התהליך חזר מצבם לקדמותו ובשניים מהם הלוקמיה נעלמה לחלוטין, בעוד שאצל השלישי אובחן שיפור, הגם שלא העלמות מוחלטת של המחלה[10]. אצל אותם שני חולים שהבריאו לכאורה, הלוקמיה לא שבה, נכון לדצמבר 2012, למעלה משנתיים וחצי לאחר מכן, כך שההנחה היא שהחולים נרפאו לחלוטין. נראה כי תאי לימפוציט T מהונדסים, שהוזרקו, התרבו בגופם של החולים, השמידו את הסרטן, ואז נעלמו, משאירים מאחוריהם רק מספר תאים מצומצם, ש"יזכור" את המחלה והטיפול, למקרה שהסרטן יחזור. לא נמצא הבדל בהשפעה כתוצאה מהשוני במספר תאי T שנשאבו.
לאור תוצאות השלב הראשון החל טיפול דומה בתשעה חולים נוספים, שחלו בצורות נוספות של לוקמיה והיו אף הם בשלבים סופניים, בהם שום טיפול חלופי לא הועיל יותר. בין השאר הוחל בטיפול זה, באפריל 2012, בילדה בת שבע, אמילי ווייטהד, שחלתה שנתיים קודם לכן בלוקמיה לימפוציטית חריפה או לוקמיה לימפובלסטית חריפה (Acute Lymphoblastic Leukemia). הטיפול הוביל לתוצאה דומה מאוד לזו שתוארה לעיל, לרבות קדחת חום וירידת לחץ דם מסכנת חיים, אך בסופו של דבר להיעלמות מוחלטת של הסרטן, לפחות למשך השנים שעברו מאז הטיפול[11] (הילדה בריאה לחלוטין גם נכון ל-2017 והיא והוריה היו בין המשפיעים בעד אישור ה-FDA, המפורט להלן).
בעקבות ההצלחה[עריכת קוד מקור | עריכה]
בעקבות ההצלחה, לפחות לכאורה, של הטיפול שהוביל קרל ג'ון, השקיעה חברת התרופות נוברטיס 20 מיליון דולר בצוותו, לצורך פיתוח ושיכלול השיטה. בין הבעיות אותן צריך היה הצוות לפתור:
- לכל חולה יש ליצור "קו" ספציפי של תאי T לטיפול בסרטן הספציפי שלו.
- מדובר בטיפול יקר - העלות הישירה בלבד, עומדת, נכון ל-2012 על כ-20,000$ לחולה.
- הטיפול גורם להשמדתם של כל תאי לימפוציט B של החולה, כך שהוא יצטרך לקחת עד סוף ימיו תרופה למניעת אותם זיהומים ספציפיים נגדם לוחם בדרך כלל סוג זה של לימפוציטים.
- לא ברור מדוע ההצלחה של טיפול זה היא חלקית בלבד. ייתכן שהדבר נובע מכך שלא אצל כל החולים, כל הלימפוציטים מסוג B נושאים על פני המעטפת שלהם את האנטיגן המתאים אליו יוכלו להתחבר תאי לימפוציט T המהונדסים.
- מאידך, ייתכן שגם רקמות בריאות יישאו את אותו אנטיגן נגדו מכוונים תאי T המהונדסים, כך שגם איברים בריאים עלולים להיפגע.
למרות כל הבעיות שנמנו לעיל או אחרות שיתגלו, ייתכן ששיטה זו מעניקה תקווה ממשית לכך שהיא תהווה, לפחות עבור חלק מן החולים, תרופה לסרטן הדם לסוגיו. ייתכן אף, ששיטה זו נותנת פתח, הגם שעדיין רחוק, להנדסת תאי T, כך שיוכלו לחסל ולרפא גם סוגים אחרים של סרטן, לא רק של הדם, אלא אולי אף ברקמות מוצקות.
ניסוי נרחב על בני אדם ואישור ה-FDA (2017)[עריכת קוד מקור | עריכה]
בין אפריל 2015 לאוגוסט 2016 התנהל שלב נרחב יותר של ניסוי השיטה על בני אדם. כאמור, תחילה היא נוסתה על שלושה ולאחר מכן עוד תשעה בני אדם. בשלב השלישי השתתפו בניסויים 63 מתנדבים, רובם ילדים חולי לוקימיה, שכל שיטות הטיפול האחרות לגביהם נכשלו, והרופאים הכריזו עליהם כסופניים. הטיפול הציל בשלבו הראשוני ממוות בטוח 82.5% מהחולים הסופניים, כלומר 52 בני אדם נותרו בחיים עם רמיסיה (Remission - נסיגה במחלה). בהמשך חלה התדרדרות חוזרת במצבם של 11 מתוכם, ועוד 11 עברו טיפולים נוספים, שגרמו לכך שאי אפשר יהיה להעריך את תוצאת הניסוי כשלעצמו, לגביהם. כמו כן אחד המתנדבים פרש מהניסוי. כלומר, נכון לסוף 2016, 29 מתוך 63 המתנדבים הסופניים (כמעט מחצית), הבריאו לכאורה ממחלתם. רק 11 (17.5%) מ-63 המתנדבים מתו בשלב הראשון וגם בקרבם, לפחות אצל חלק, הייתה הקלה זמנית בסימפטומים והארכת חיים בת מספר חודשים לעומת הצפי הראשוני.
לאור תוצאות אלה, ב-12 ביולי 2017 החליט צוות מיוחד של ה-FDA, פה אחד, להמליץ שהסוכנות האמריקאית תאשר את הפיתוח הסינתטי של הטיפול, אשר איננו משתמש בנגיף ה-HIV, באופן סופי וב-30 באוגוסט 2017 הוא אושר, הריפוי הגני הראשון שאושר אי פעם על ידי מנהל המזון והתרופות האמריקאי[4][3].
ראו גם[עריכת קוד מקור | עריכה]
- סטיבן רוזנברג
- קייט פארמה
- לוקמיה מיאלואידית חריפה
- לוקמיה מיאלואידית כרונית
- שחפת נגד סרטן שלפוחית השתן
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- HIV virus used to turn white blood cells into cancer serial killers, אוגוסט 2011, באתר Geek-Cetera
- New leukemia treatment exceeds 'wildest expectations', באתר MSNBC, 8 בנובמבר 2011
- "Penn Med's Carl June discusses breakthrough cancer research", באתר The Daily Pennsylvanian, פברואר 2013
- "Drs. Zelig Eshhar and Carl June Honored with Pioneer Awards", באתר GEN, 11 בנובמבר 2014
- Pollack, Andrew (2016-08-01). "Setting the Body's 'Serial Killers' Loose on Cancer". The New York Times (באנגלית אמריקאית). נבדק ב-2020-05-30., באתר הניו יורק טיימס, 1 באוגוסט 2016
- Pharma Revs Up Cancer-Fighting CAR T-Cell Therapy, 8 ביוני 2017
- "F.D.A. Panel Recommends Approval for Gene-Altering Leukemia Treatment", באתר הניו יורק טיימס, 12 ביולי 2017
- "המדע שמאחורי האקזיט המוצלח", באתר מכון דוידסון, 29 באוגוסט 2017
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ נשא נגיפי סינתטי (אורכב 20.04.2018 בארכיון Wayback Machine)
- ^ "F.D.A. Panel Recommends Approval for Gene-Altering Leukemia Treatment", ניו יורק טיימס, 12 ביולי 2017
- ^ 1 2 ג'יימס גלאגר, "First cancer 'living drug' gets go-ahead", באתר BBC, 30 באוגוסט 2017
- ^ 1 2 שלושת מקבלי פרס נוברטיס לאימונולוגיה קלינית ל-2016, זליג אשחר, סטיבן רוזנברג וקרל ג'ון, באתר נוברטיס, 15 באוגוסט 2016
- ^ In Girl’s Last Hope, Altered Immune Cells Beat Leukemia, באתר ניו יורק טיימס, 10 בדצמבר 2012
- ^ An Immune System Trained to Kill Cancer, באתר ניו יורק טיימס, 12 בספטמבר 2011
- ^ Expression of immunoglobulin-T-cell receptor chimeric molecules as functional receptors with antibody-type specificity, דצמבר 1989, PNAS
- ^ על פרופסור זליג אשחר, באתר מכון ויצמן למדע
- ^ מגזין מכון ויצמן, מתמקדים במטרה, באתר "הידען", 27 ביולי 2011
- ^ Chimeric Antigen Receptor–Modified T Cells in Chronic Lymphoid Leukemia, אוגוסט 2011, באתר New England Journal of Medicin
- ^ שרית רוזנבלום, ידיעות אחרונות, הטיפול שהציל בת 6 מלויקמיה: נגיף איידס מהונדס, באתר ynet, 11 בדצמבר 2012
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.
