חוקי הדיפוזיה של פיק
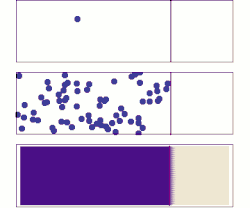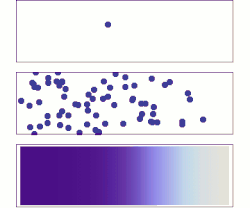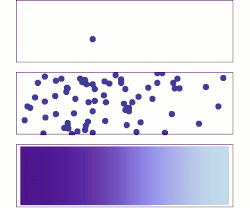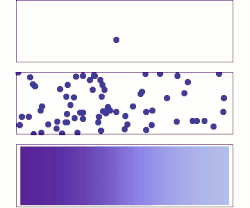
איור א: מולקולה בודדת נעה אופן אקראי.
איור ב: כשמספר המולקולות גדול, קיימת מגמה ברורה – הממס מתפזר במכל באופן אחיד ככל שעובר הזמן.
איור ג: כשמספר המולקולות המומסות רב, האקראיות נעלמת, והמומס עובר באופן רציף וסדיר מאזור הריכוז הגבוה לאזור בו ריכוז נמוך על פי חוקי פיק
חוקי הדיפוזיה (או: הפעפוע) של פיק (Fick) הם שני חוקים המתארים את תופעת הפעפוע (דיפוזיה בלעז), ונתקבלו לראשונה על ידי הרופא והפיזיולוג הגרמני אדולף פיק (אנ') ב־1855.
שני החוקים מתארים את תנועתו של חומר המיוחסת למנגנון הדיפוזיה. פיק, שהושפע מעבודתו של הכימאי תומאס גרהאם, מדד ריכוזים ושטפים של מלח, המפעפע בין שני מאגרים דרך צינורות מים, ועל בסיסם ניסח את החוקים הנקראים על שמו. עבודתו של פיק התרכזה בדיפוזיה בנוזלים, משום שבאותה תקופה דיפוזיה של מוצקים לא נחשבה לאפשרית[1]. כיום, חוקיו של פיק נמצאים בלב ההבנה של תופעת הדיפוזיה במוצקים, בנוזלים ובגזים גם יחד.
החוק הראשון של פיק[עריכת קוד מקור | עריכה]
חוק זה קובע כי הקשר בין השטף של חומר מסוים לריכוז שלו הוא קשר של נגזרת - השטף עומד ביחס ישר לגרדיאנט (נגזרת מרחבית) של הריכוז. במערכת בעלת מימד אחד נקבל:
כאשר הוא השטף הדיפוזיוני של כמות החומר, הוא קבוע הדיפוזיה, הוא ריכוז החומר כתלות במקום, ו- הוא המיקום.
במערכות בהן ריכוז החומר משתנה במספר ממדים, יש צורך להשתמש בפונקציות אשר מכלילה את הנגזרת הראשונה ולקבל: , כאשר הוא הגרדיאנט של הריכוז.
קבוע הדיפוזיה מתכונתי למהירות החלקיקים הדיפוזיוניים. מהירות החלקיקים תלויה בטמפרטורה, בצמיגות הנוזל ובגודל החלקיקים (על פי משוואת איינשטיין-סטוקס). בתמיסות מהולות, קבוע-הדיפוזיה של מרבית היונים דומה ונע בטמפרטורת החדר בתחום שבין 0.6x10-9 ובין 2x10-9 m2/s. עבור מולקולות ביולוגיות דוגמת חלבונים קבוע הדיפוזיה נע בין 10-11 ובין 10-10 m2/s.
הכוח המניע של הדיפוזיה במערכת דיפוזיה חד-ממדית מבוטא על ידי:
בתמיסה אידיאלית ביטוי זה מבטא את מפל הריכוזים. בתמיסות שאינן אידיאליות או בתערובות, הכוח המניע לדיפוזיה של כל צורון הוא מפל הריכוזים של אותו צורון. במקרה כזה חוק הראשון של פיק (במימד אחד) יכול להיכתב כ:.
כאן האינדקס i מסמל את הצורון המסוים, c הוא הריכוז, R הוא קבוע הגזים, T היא הטמפרטורה ו-μ הוא הפוטנציאל הכימי.
החוק השני של פיק[עריכת קוד מקור | עריכה]
החוק השני של פיק מתאר מערכות שבהן ריכוז של חומר משתנה בזמן. ניסוחו:
כאשר הוא ריכוז החומר, הוא הזמן, הוא קבוע הדיפוזיה ו- הוא המיקום. ניתן לגזור את החוק השני של פיק מתוך החוק הראשון תוך שימוש במשוואת רציפות:
בהנחה שקבוע הדיפוזיה D אינו משתנה במרחב, ניתן לקבל את ניסוחו של חוק פיק השני, כפי שמופיע בראשית הפסקה.
במקרה הכללי בו הדיפוזיה איננה חד-ממדית אלא בעלת שני ממדים או יותר, החוק ינוסח בעזרת אופרטור הלפלסיאן:
כאשר קבוע הדיפוזיה קבוע במרחב, המשוואה הדיפרנציאלית תצטמצם לצורה הפשוטה יותר: .
דוגמה חשובה היא המקרה שבו נמצא בשיווי משקל. במקרה כזה הריכוז איננו משתנה עם הזמן ולכן כל האגף השמאלי במשוואה שווה לאפס. במערכת המתוארת כבעלת ממד אחד כאשר קבוע הדיפוזיה הוא קבוע, הפתרון לריכוז הוא ליניארי (תלות ליניארית של הריכוז במיקום). בשני ממדים או יותר מתקבלת משוואת לפלס: , שהפונקציות המקיימות אותה נקראות פונקציות הרמוניות.
דוגמה לפתרון במימד אחד[עריכת קוד מקור | עריכה]
נדגים את המקרה של דיפוזיה משתנה בזמן במימד אחד (ציר x, בלי הגבלת הכלליות), של חומר שריכוזו נתון על ידי ממשטח גבול הממוקם ב-, כאשר הריכוז על הגבול מוחזק בגודל קבוע (חומר חצי-אינסופי). הפתרון למקרה זה הוא:
erfc היא פונקציית השגיאה המשלימה. הגודל נקרא אורך הדיפוזיה, והוא גודל אופייני הקשור לעומק שאליו פעפע החומר בזמן t.
ראו גם[עריכת קוד מקור | עריכה]
לקריאה נוספת[עריכת קוד מקור | עריכה]
- Fick, Adolf (1855). "Über Diffusion". Annalen der Physik und Chemie (בגרמנית). 170 (1): 59–86. doi:10.1002/andp.18551700105. ISSN 0003-3804.
- Fick, Adolph (1855). "V. On liquid diffusion". The London, Edinburgh, and Dublin Philosophical Magazine and Journal of Science. Informa UK Limited. 10 (63): 30–39. doi:10.1080/14786445508641925. ISSN 1941-5982.
קישורים חיצוניים[עריכת קוד מקור | עריכה]
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ Philbert, Jean (2006). "One and a Half Century of Diffusion: Fick, Einstein, Before and Beyond". Diffusion Fundamanetals. 4: 6.1–6.19.























