דחף עצבי
 | |
| שיוך |
regulation of membrane potential, bioelectric potential difference |
|---|---|
| מזהים | |
| קוד MeSH |
G04.580.100 |
| מזהה MeSH |
D000200 |

דחף עֲצַבִּי או ספייק הוא אות חשמלי המשמש להולכה של המידע למרחקים בתאים. כינוי אחר לתופעה פיזיולוגית זו הוא פוטנציאל פעולה, כתרגום מהמונח האנגלי Action Potential. פוטנציאל הפעולה מופיע בתאים שיש להם קרום תא הניתן לעירור (אקסיטבילי). פוטנציאל פעולה מתרחש כאשר מתח הקרום של תא ספציפי עולה ממתח המנוחה ויורד בהמשך.[1] עליית המתח (הנקראת גם דה-פולריזציה) גורמת לעליית מתח דומה במיקומים סמוכים וכך להעברת האות לאורך קרום התא. פוטנציאל פעולה מתרחש במספר סוגים של תאים, הנקראים תאים מעוררים (אקסיטטורים). בבעלי חיים, אלו כוללים תאי עצב, תאי שריר, תאים אנדוקריניים כגון תאי בטא של הלבלב ועוד.[2] קיימים גם תאים אקסיטטורים המוליכים פוטנציאל פעולה בצמחים.[3]
דחפים עצביים הם רכיב מרכזי של התקשורת בתוך מערכת העצבים, והם פועלים לרוב בצימוד עם תהליך העברת אותות ביוכימי שנקרא העברה סינפטית.
פוטנציאל פעולה - הגדרה[עריכת קוד מקור | עריכה]
פוטנציאל פעולה הוא שינוי מהיר במתח החשמלי שבין פנים התא לסביבתו החיצונית, זאת לעומת מצב של מתח מנוחה.
במצב מנוחה המתח בין שני צדדיו של קרום התא הוא שלילי - פנים התא נושא מטען שלילי יותר לעומת חוץ התא. התהליך של פוטנציאל פעולה מתאפיין ב"קפיצה" מהירה של המתח לערכים חיוביים יותר, המכונה דה־פולריזציה. קפיצה זו מתרחשת ברגע שמתח הממברנה עולה על ערך סף מסוים. לאחר העלייה במתח, מתח הממברנה יורד חזרה כלפי מטה לערכים יותר שליליים.
התופעה של פוטנציאל פעולה נגזרת מתכונותיהן של תעלות יונים ממותגות מתח הנמצאות על פני קרום התא. צורתו ומשכו של פוטנציאל הפעולה, וכן ערך הסף ליצירתו, משתנים בין סוגי תאים שונים ואף בין חלקים שונים של אותו התא, וזאת בשל הבדלים בכמויות ובסוגים של תעלות היונים המפוזרות על פני הממברנה. פוטנציאל הפעולה נחשב יחידת המידע הבסיסית של מערכת העצבים.
יצירת הדחף העצבי[עריכת קוד מקור | עריכה]
| מרכיביו של תא עצב טיפוסי | ||||||||
|---|---|---|---|---|---|---|---|---|
|
|
||||||||
באופן טיפוסי, פוטנציאל פעולה בתא עצב מסוים נוצר בעקבות הקלט שהוא מקבל מתאי עצב אחרים, דרך סינפסה כימית או חשמלית.
במקרה של סינפסה כימית, קלט זה מתבטא במוליך עצבי שמופרש מהתא הקדם־סינפטי ונקשר לקולטן על גבי דנדריט של תא העצב הבתר־סינפטי. פעילות הקולטן גוררת שינוי במתח קרום התא באזור הדנדריט. מצב זה מכונה פוטנציאל בתר־סינפטי. כאשר השינוי במתח מקרב אותו לערך הסף ליצירת פוטנציאל פעולה (כלומר, מביא אותו לערך יותר חיובי), זהו פוטנציאל בתר־סינפטי מעורר. לעומת זאת, כאשר הפעילות מקבעת את המתח על ערך שלילי, כלומר מקטינה את ההסתברות ליצירת פוטנציאל פעולה, נוצר בדנדריט פוטנציאל בתר־סינפטי מעכב.
הפוטנציאלים הבתר־סינפטיים שנוצרו בדנדריט מתפשטים בתוך הנוזל התוך־תאי. בסמוך לאזור בתא המכונה תלולית האקסון, מתבצעת סכימה של הפוטנציאלים החשמליים (מעוררים ומעכבים) שהגיעו מהדנדריטים השונים של אותו התא. אם סכום המתח הוא גבוה מערך הסף ליצירת פוטנציאל פעולה, ייווצר פוטנציאל פעולה בתחילת האקסון. במצב זה נהוג לומר כי תא העצב "יורה" פוטנציאל פעולה. כאשר נוצרים באקסון מספר פוטנציאלי פעולה זה אחר זה, ניתן לדבר על "קצב הירי" של הנוירון.
בתהליך הסכימה שמתבצע בתלולית האקסון, תא העצב מסכם את האותות החשמליים שהוא מקבל במרחב ובזמן. ראשית, ישנו חיבור של אותות מעוררים ומעכבים שהתקבלו באותו הזמן דרך מספר סינפסות שונות (סכימה במרחב). בנוסף, כאשר נוצרים פוטנציאלים בתר־סינפטיים במרווחי זמן קצרים זה אחר זה, הם יכולים להסתכם לכדי אות חשמלי מאוחד המשקף את העוצמה המשוקללת שלהם.
כאמור, פוטנציאל פעולה ייווצר רק אם המתח ברגע נתון הוא גבוה מערך הסף של התא. לעומת זאת, אם המתח הוא נמוך מערך הסף, האות החשמלי ידעך במהירות ולא יועבר הלאה בשרשרת ההולכה העצבית. מרגע שהמתח עובר את ערך הסף, עוצמתו ומשכו של כל פוטנציאל הפעולה הם לרוב בגדלים קבועים, אשר תלויים אך ורק במאפיינים של קרום התא. במילים אחרות, גם אם עוצמת הקלט תוגבר, פוטנציאל הפעולה לא ישתנה. בשל כך, נהוג להתייחס לדחף העצבי כאות בינארי של "הכל או לא כלום", שבו המידע היחיד שמועבר ברגע נתון הוא אם קיים פוטנציאל פעולה או לא. עם זאת, קביעה זו אינה מתקיימת בכל המקרים.[4]
פירוט התהליך האלקטרופיזיולוגי[עריכת קוד מקור | עריכה]

יצירת הדחף העצבי תלויה בתעלות יונים עצביות. תעלות אלו הן מבנים חלבוניים הממוקמים בקרום התא ומאפשרים, כאשר הם נפתחים, תנועה של יונים דרך הקרום. חלק מהתעלות נפתחות או נסגרות (באמצעות "שערים") בתלות בגודלו של המתח החשמלי על פני קרום התא, ונקראות בהתאם תעלות יונים ממותגות מתח (Voltage-gated ion channels). חלק מהתעלות הן בררניות - תעלה בררנית מוליכה יונים מסוג מסוים (אשלגן, נתרן או סידן) ביעילות רבה עד כדי ארבעה סדרי גודל לעומת יונים אחרים. הפתיחה היא מהירה והסגירה איטית. הדחף העצבי נוצר על ידי שני סוגים עיקריים של תעלות יונים ממותגות מתח - תעלות נתרן ותעלות אשלגן. במצב מנוחה נשמר ריכוז תוך־תאי גבוה של יוני אשלגן וריכוז חוץ־תאי גבוה של יוני נתרן וכלור. אלה שקולים לפי משוואת נרנסט להפרשי פוטנציאלים חשמליים, המקנים לתא פוטנציאל חשמלי שלילי של כ־70- מיליוולט ביחס לתמיסה החוץ־תאית. הקטנת הפרש הפוטנציאלים על פני הקרום מביאה לפתיחת תעלות נתרן. כאשר המתח החשמלי על פני קרום התא מגיע לערך סף מסוים, נפתחות התעלות הבררניות לנתרן וזרם של יוני נתרן חיוביים מפעפע לתוך התא שכן ריכוז יון זה גבוה בהרבה מחוץ לתא. תהליך זה הוא תהליך משוב חיובי, שכן כניסה של יוני נתרן לתוך התא רק תגביר את השינוי החיובי במתח ותעלות נוספות יפתחו. כך משתנה המתח ממתח המנוחה (כ־70- מיליוולט בתאי עצב מסוימים) לערך רגעי גבוה - כ־30+ מיליוולט, זהו בערך "מתח שיווי המשקל" של הנתרן. שלב זה נקרא 'נסיקה'. כאשר המתח בתוך התא הופך לפחות שלילי (או חיובי) תהליך זה מכונה דפולריזציה וכאשר המתח הופך שלילי יותר (פחות חיובי) תהליך זה מכונה היפר־פולריזציה. בה בעת, תעלות אשלגן נפתחות לאט יותר ומאפשרות ליוני אשלגן לפעפע מהתא החוצה. ליוני אשלגן מטען חיובי, כך שיציאתם מהתא מקטינה את הפוטנציאל החשמלי שלו ביחס לתמיסה החוץ־תאית, וכך מתחיל המתח לחזור למצב מנוחה. בינתיים נסגרות תעלות הנתרן ועוברות למצב אבטול (אינאקטיבציה) ויוני נתרן טעונים חיובית מפסיקים להיכנס לתוך התא. התא עובר רה־פולריזציה והמתח החשמלי על פני הקרום צונח לכ־90- מיליוולט ותעלות האשלגן נסגרות אף הן.
במצב זה לא ניתן לעורר דחף עצבי חדש למשך כמה מאות מילישניות, בין היתר מכיוון שתעלות הנתרן נמצאות במצב אבטול. פרק זמן זה, המכונה תקופת אי־הענות (אֶתנָח) או התקופה הרפרקטורית, אחראי על כך שהדחף העצבי מתקדם לכיוון יחיד לאורך הסיב העצבי ולא לשני הכיוונים. ריכוזי היונים נשמרים במצבם ההתחלתי הודות לפעולת משאבות נתרן־אשלגן (Na+/K+-ATPase). בתום מצב האבטול ניתן לעורר דחף עצבי נוסף.
(הדחף העצבי מכונה גם ירייה (firing) בגלל שתחת מגבר קולי קול פוטנציאל הפעולה נשמע כירי.)
הולכת הדחף העצבי באקסון[עריכת קוד מקור | עריכה]
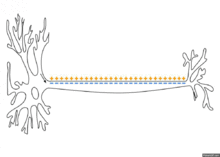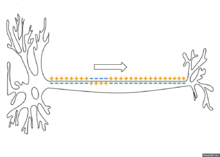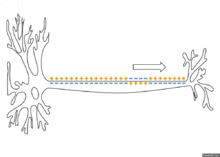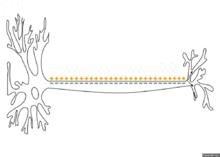
ההולכה באקסון מתפשטת מגוף תא העצב לאורך האקסון וגורמת דפולריזציה על־סיפית בקטע האקסון הסמוך לו. הדפולריזציה מביאה לפתיחת תעלות נתרן תלויות מתח ולהתפרצות פוטנציאל פעולה באותו קטע. מאחר שיש תעלות נתרן לכל אורכו של קרום האקסון, פוטנציאל הפעולה מתפרץ מחדש בצורה אקטיבית בכל נקודה ונקודה על פני האקסון ברצף. פוטנציאל הפעולה מתקדם לעבר הכפתורים הסופיים בקצב קבוע ואיטי יחסית.
באקסון בעל מעטפת מיאלין, פוטנציאל הפעולה מתפשט בצורה אחרת. באקסונים אלו, לרוב העצב יש מעטה מיאלין, אבל יש אזורים (שמופיעים לסירוגין לאורך העצב - כל 1–2 מ"מ) שנקראים מרווחי ראנוויה, שם אין מעטה מיאלין. מעטפת המיאלין המבודדת לא מאפשרת היווצרות פוטנציאל פעולה; באזורים אלו ההולכה של פוטנציאל הפעולה היא פאסיבית - זרימת זרם בין האזור האקטיבי לאזור שעדיין לא אקטיבי. הולכה זו במקטעים העטופים היא מהירה אך דועכת בהדרגה. במרווחי ראנוויה יש צפיפות גבוהה של תעלות נתרן תלויות מתח. כשגל הדפולריזציה הפאסיבית מגיע ממעלה העצב למרווח ראנוויה, נוצר זרם של דפולריזציה על ידי יוני הנתרן שנכנסים דרך תעלות הנתרן תלויות המתח, וכך נבנה מחדש פוטנציאל הפעולה. לכן, פוטנציאל הפעולה מתקדם בקפיצות בין מרווח ראנוויה אחד לזה שאחריו, תהליך שנקרא Saltatory conduction, ואילו בין המרווחים ההולכה היא פאסיבית.
ההולכה בקפיצות שבאקסון העטוף מהירה יותר מן ההולכה האקטיבית באזור החשוף, בגלל מהירותה של ההולכה הפאסיבית. ההולכה בקפיצות היא גם חסכונית יותר מן ההולכה האקטיבית משום שהיא לא צריכה השקעת אנרגיה להפעלת משאבות הנתרן והאשלגן באותם מקטעים עטופי מיאלין.
עצבים בעלי מעטפת מיאלין נמצאים בעיקר בבעלי חוליות; אבל מנגנון דומה נמצא בכמה חסרי חוליות, כגון סוגי חסילונים. לא כל העצבים של בעלי חוליות הם בעלי מעטפת מיאלין; בדרך כלל לעצבים של מערכת העצבים האוטונומית אין מעטפת מיאלין.
חסימת הולכה[עריכת קוד מקור | עריכה]
טטרודוטוקסין הוא רעלן עצבי חזק החוסם תעלות נתרן בתאי עצב. המולקולה נקשרת לפתחי תעלות נתרן ממותגות מתח ומונעת את יצירת הדחף העצבי.
מנגנון הפעולה של לידוקאין מבוסס על חסימת תעלות נתרן והורדת קצב התכווצות שריר הלב.
ירי ספונטני[עריכת קוד מקור | עריכה]
בניגוד למצב הרגיל, שבו פוטנציאל הפעולה שנוצר בתא הוא תוצאה של קלט שהגיע מתא אחר, ישנם גם מקרים שבהם פוטנציאלי פעולה נוצרים באופן ספונטני. כלומר, בתאים מסוימים המאפיינים של קרום התא (סוגי תעלות היונים והמשאבות, מספרן וכו') גורמים לכך שייווצר בתא הזה פוטנציאל פעולה אחד לפרק זמן מסוים, גם אם לא קיבל גירוי מתאים אחרים. עם זאת, גם בתא שכזה דפוס הירי מושפע מהקלט שהתא מקבל, אשר עשוי לגרום לשינוי קצב הירי או לדיכוי דפוסי הירי הספונטניים. אוכלוסיות של תאי עצב אשר יורות דחפים עצביים באופן ספונטני ממלאות תפקיד חשוב ברשתות עצביות מסוימות במערכת העצבים.
לתופעה זו יש חשיבות רבה גם בתאי שריר. דוגמה ידועה היא תאי הקוצב (pacemaker cells) בשריר הלב, אשר יורים באופן ספונטני פוטנציאלי פעולה בקצב מסוים. הירי הספונטני של תאי הקוצב מווסת על ידי מערכת העצבים האוטונומית, וקצב הירי הסופי של תאים אלה הוא זה שקובע את קצב הלב.
פתולוגיות[עריכת קוד מקור | עריכה]
באפילפסיה יכולת הירי של הנוירונים האקסיטטוריים משתנה. מצב זה עשוי להתרחש עקב שינויים בתעלות יונים או בנוירונים אינהיבטוריים אשר לא מתפקדים כראוי.[5][6]
היסטוריה של חקר התופעה[עריכת קוד מקור | עריכה]
 ערך מורחב – מודל הודג'קין-הקסלי
ערך מורחב – מודל הודג'קין-הקסלי
אופן היווצרותם של דחפים עצביים מתואר על ידי מודל הודג'קין־הקסלי, שפורסם בשנת 1952 על ידי אלן הודג'קין ואנדרו הקסלי, על יסוד מחקר שביצעו על תכונותיהם החשמליות של סיבים עצביים בדיונונים ממין Doryteuthis pealeii. עבודה זו, הנחשבת לגולת הכותרת של תקופת הביופיזיקה הקלאסית, זיכתה את השניים בפרס נובל לפיזיולוגיה או לרפואה לשנת 1963. המודל מבוסס על מערכת משוואות דיפרנציאליות רגילות לא ליניאריות, המקרבות את התכונות החשמליות של קרום התא. הוא תקף לכל סוגי התאים בכל היצורים החיים, אך השלכותיו נוגעות במיוחד למערכת העצבים.
ראו גם[עריכת קוד מקור | עריכה]
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- ארז גרטי, פוטנציאל הפעולה – הולכת אותות חשמליים בגוף, במדור "מאגר המדע" באתר של מכון דוידסון לחינוך מדעי, 5 ספטמבר 2009
- פוטנציאל פעולה - הולכת אותות חשמליים בגוף

- דחף עצבי, באתר אנציקלופדיה בריטניקה (באנגלית)
- סרטון המסביר את פוטנציאל הפעולה בתאי עצב, לימודי המשך של אוניברסיטת הרווארד:
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ A. L. Hodgkin, A. F. Huxley, A quantitative description of membrane current and its application to conduction and excitation in nerve, The Journal of Physiology 117, 1952-08, עמ' 500–544 doi: 10.1113/jphysiol.1952.sp004764 (באנגלית)
- ^ J. A. Williams, Electrical correlates of secretion in endocrine and exocrine cells, Federation Proceedings 40, 1981-02, עמ' 128–134 (באנגלית)
- ^ Colin Brownlee, Plant physiology: Anatomy of a plant action potential, Current biology: CB 32, 2022-10-10, עמ' R1000–R1002 doi: 10.1016/j.cub.2022.08.024 (באנגלית)
- ^ Sasaki T, Matsuki N and Ikegaya Y (2011). "Action-Potential Modulation During Axonal Conduction". Science. 331 (6017): 599–601. doi:10.1126/science.1197598.
- ^ Michel Le Van Quyen, Vincent Navarro, Jacques Martinerie, Michel Baulac, Toward a neurodynamical understanding of ictogenesis, Epilepsia 44 Suppl 12, 2003, עמ' 30–43
- ^ Fernando Lopes da Silva, Wouter Blanes, Stiliyan N. Kalitzin, Jaime Parra, Epilepsies as dynamical diseases of brain systems: basic models of the transition between normal and epileptic activity, Epilepsia 44 Suppl 12, 2003, עמ' 72–83
| תפקוד מערכת העצבים והמוח | ||
|---|---|---|
| תקשורת במערכת העצבים | תא עצב • דחף עצבי • סינפסה • מוליך עצבי • העברה סינפטית • רשת עצבית • הפלסטיות של מערכת העצבים • אפנון עצבי | |
| מערכות תפקודיות | מערכות חישה • המערכת המוטורית • המערכת הלימבית • מערכת החיזוק • המערכת הנוירואנדוקרינית | |
| תפקודים קוגניטיביים | תפיסה • זיכרון • קשב • תפקודים ניהוליים | |
| בדיקות למדידת תפקודים עצביים | EEG - אלקטרואנצפלוגרם • NCT - בדיקת מוליכות עצבית • fMRI - דימות תהודה מגנטית תפקודי • MEG - מגנטואנצפלוגרפיה • PET - טומוגרפיית פליטת פוזיטרונים | |

