התפתחות מוקדמת של השד
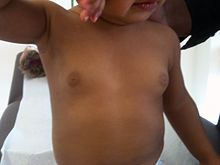 | |
| התפתחות מוקדמת דו-צדדית של שדיים אצל תינוקת. | |
| סיווגים | |
|---|---|
| ICD-10 |
E30.8 |
התפתחות מוקדמת של השד (באנגלית: Premature thelarche או בקיצור PT) היא מחלה רפואית המאופיינת בהתפתחות איבר השד אצל ילדות בגיל מוקדם. המחלה מופיעה אצל ילדות מתחת לגיל 8, כשמופע הגבוה ביותר שלה הוא לפני גיל שנתיים. התופעה הזו נחשבת נדירה, ומופיעה אצל 2.2-4.7% מהתינקות בגילאים 0 עד 2.[1] הגורם המדויק למצב עדיין אינו ידוע, אך הוא נקשר למגוון גורמים גנטיים, תזונתיים ופיזיולוגיים.[2]
תסמינים וסימנים[עריכת קוד מקור | עריכה]
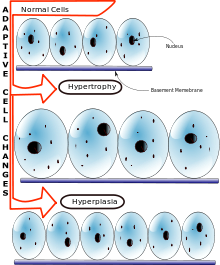
התפתחות מוקדמת של השד היא תופעה של גיל ההתבגרות המוקדמת, גיל ההתבגרות המוקדמת הוא נוכחות של מאפייני מין משניים אצל תינוק, ללא שינוי ברמות הורמון המין שלהם. אין טיפול להתפתחות מוקדמת של השד, אבל בדיקה קבועה חשובה כדי להבטיח שהיא לא תתפתח להפרעה אנדוקרינית אגרסיבית. מחלת התפתחות שד מוקדמת היא היפרטרופיה של השד לפני גיל ההתבגרות. צורה זו של היפרטרופיה פירושה עלייה ברקמת השד. המחלה מופיעה אצל בנות לפני גיל ההתבגרות (מתחת לגיל 8), בדרך כלל מופיע בשנתיים הראשונות בחייהן.[3] לרוב התפתחות השד היא דו-רוחבית: שני השדיים מראים התפתחות ובמקרים מסוימים ההתפתחות עשויה להיות חד צדדית (שד אחד מתפתח).
CPP ו-PT[עריכת קוד מקור | עריכה]
CPP – התבגרות מינית מוקדמת הנובעת מסיבה מרכזית היא הפרעה אנדוקרינית אגרסיבית עם השלכות התפתחותיות מזיקות למטופל.[4] הוא מצב חמור יותר מ-התבגרות מוקדמת ומייצג שינוי מאפייני מין משניים, עם שינוי בהורמוני המין עקב שינוי בציר ההיפותלמוס – בלוטת יותרת המוח (HPG)[1]
PT אינו דורש טיפול מכיוון שהמצב מוגבל לרקמת שד מוגדלת שלרוב פוחתת עם הזמן . CPP קשור למגוון רחב יותר של תסמינים כמו צמיחת בשער הערווה, הזדקנות מואצת של העצם, מהירות גדילה מוגברת וצמיחה מוקדמת של אפיפיזה (קצה העצם). אם אדם מושפע מ CPP הוא יצטרך להתחיל טיפול באופן מיידי. CPP מטופל בהורמונים הורמונליים המשחררים אגוניסטים הורמונליים. PT יכול להשפיע מעט על מהירות הצמיחה ועל גיל העצם, אך CPP משפיע על מאפיינים אלה עד כדי פגיעה במעמד המבוגר.[1] חולים עם חשד ל-PT חייבים לעבור בדיקות אבחון כדי להבטיח שזה לא CPP או תאי מוח מוגזמים, שלב הביניים לפני CPP.[5] הבדלי הורמונים בולטים מתרחשים בין חולי CPP ו-PT, ולכן לימוד רמות הורמונים אלו הוא האבחון הביוכימי העיקרי המשמש ב-CPP. אנשים עם CPP בדרך כלל יש רמות הורמונים הורמונליים המשחררים אגוניסטים בסיסיות גבוהות יותר.[1][3]
מעטים מחולי ה-PT (עד 9-14%) צפויים לפתח CPP.[1][3] האבחון מאפשר לרופאים לזהות את הצגת הסימפטומים המעידים על CPP בחולי PT. אין בדיקות אבחון שיכולות להצביע אם חולה PT נמצא בסיכון לפתח CPP.[3] במהלך האבחון של PT, נעשה שימוש באבחון כדי להבטיח שזה אינו CPP בשלב מוקדם. ניתן להבדיל בין CPP לבין PT באמצעות בדיקות ביוכימיות, אולטרה סאונד ואבחון שוטף.[5] אבחון CPP חשוב מאחר שהטיפול נחוץ.[1]
דפוסי PT[עריכת קוד מקור | עריכה]
ישנם ארבעה דפוסים של התפתחות PT, לרוב החולים יש היפרטרופיה ואחריה אובדן מוחלט של רקמת השד העודפת (51% מהמקרים) או אובדן של רוב הרקמות העודפות, אך חלקן נשארות עד גיל ההתבגרות (36% מהמקרים). לעיתים רחוקות יותר יש לחולים דפוסי תיוג: 9.7% סובלים מתבנית מחזורית בה גודל רקמת השד משתנה לאורך זמן, ו-3.2% חווים עלייה מתמדת בגודל הרקמה.[1]
תסמינים קשורים[עריכת קוד מקור | עריכה]
הסימפטום העיקרי של PT הוא רקמת שד מוגדלת אצל תינוקות. תפקיד האסטרוגן ב-PT מוביל גם לעליית גיל העצם ולצמיחה במקרים מסוימים.[6] ב-PT תסמינים משניים אלו הם מינימליים: גיל העצם משתנה רק מהגיל האמיתי בכמה חודשים ומהירות הצמיחה משתנה רק מעט מהמקובל. בדיקות אבחון יבדילו בין תסמינים משניים אלה של PT לבין הזדקנות העצם והצמיחה החמורה יותר המתרחשת ב CPP מוקדם[5]
פתופיזיולוגיה[עריכת קוד מקור | עריכה]
הפתופיזיולוגיה הישירה שעומדת מאחורי PT עדיין לא ידועה, אך ישנם סיבות רבות משוערות.[2]
אסטרוגן[עריכת קוד מקור | עריכה]
PT קשור לרגישות מוגברת של רקמת השד לאסטרדיול, נגזרת אסטרוגן, אצל אנשים מסוימים טרום-פרוברלטיים.[1] ייצור אסטרוגן או אסטרדיול ספורדי בבלוטת יותרת הכליה, בזקיקים או ציסטה שחלתית קשור גם הוא למצב.[2][7]
הורמון מגרה זקיק[עריכת קוד מקור | עריכה]

הורמון מגרה זקיק (FSH) מופרש מהיפופיזה הקדמית (בלוטת יותרת המוח הקדמית). (FSH) ממלא תפקיד מפתח בפיתוח, צמיחה והתבגרות, ולכן יש חשד שהוא ממלא תפקיד ב-PT. בדיקת גירוי GnRH הורמון משחרר גונדוטרופינים בקרב חלק מהחולים עם PT הראתה תגובה דומיננטית מ-(FSH). תגובה זו קשורה להפעלת מוטציות בקולטן (FSH) וביחידת משנה Gs-a ב-PT. חקירה גנטית הצביעה על כך שמוטציות אלו מהוות רק כמה מקרים של PT מוקדם.[2][8] PT עלול להיגרם גם על ידי הפעלה חלקית חולפת של ציר HPG. הפעלה חלקית תשחרר עודף של (FSH) מהיפופיזה הקדמית ללא הפרעה נוספת בציר ה-HPG.[7]
סיבות אחרות[עריכת קוד מקור | עריכה]
הצריכה או החשיפה לשיבושים אנדוקריניים מסוימים נקשרו גם ל-PT.[2]
אבחון[עריכת קוד מקור | עריכה]
התפתחות מוקדמת של השד אינה דורשת טיפול. ב PT, היפרטרופיה של השד בדרך כלל תיפסק לחלוטין והחולים יחוו רגרסיה של רקמת השד במשך 3 עד 60 חודשים. פחות נפוץ, חולים עשויים להישאר עם רקמת שד שנותרה או להמשיך במעגלים של היפרטרופיה בשד ורגרסיה עד גיל ההתבגרות.[1]
אבחונים משמשים אצל אנשים עם PT, במיוחד בהצגת מאפייני מין משניים אחרים. מטרת האבחון היא להבטיח שחולי PT אינם סובלים מ CPP.[1]
אולטרסאונד אגן[עריכת קוד מקור | עריכה]
אולטרסאונד באגן הוא אבחון רצוי שכן הם אינם פולשניים וקל לסקירה מתמדת. אולטרסאונד אגן חשוב באבחון CPP.[5]לחולים עם CPP יש גודל מוגבר של השחלה והרחם. נפח השחלה והרחם של חולי CPP דומה לזה של נשים שעוברות התבגרות.[1] אולטרסאונד האגן בעייתי כאבחון, מכיוון שאין ניתוק ספציפי לנפחי הרחם והשחלה שמעידים על כך שהמטופל סובל מ CPP. חולים עם PT צריכים להיות בעלי נפח הרחם והשחלות בטווח הנורמלי לגילם. אולטרסאונד באגן הוא אבחון רצוי שכן הם אינם פולשניים וקל לסקירה מתמדת. יש להתאים את אולטרסאונד האגן לבדיקות ביוכימיות כדי לקבוע את נוכחות CPP.[5]
בדיקות ביוכימיות[עריכת קוד מקור | עריכה]
בדיקות ביוכימיות חוקרות את רמות ההורמונים בחולים. לחולי CPP יש רמות LH גבוהות ויחס LH: FSH בשיא לעומת חולי PT. קשה להשתמש ב-LH כאבחון ל-CPP, שכן לבדיקת LH יש רגישות וספציפיות משתנים.[1] בדיקת גירוי ה-GnRH היא המבחן הביוכימי האבחנתי העיקרי המשמש להבחנה בין PT לבין CPP.[5] מבחן ה-GnRH מדגים את היענות יותרת המוח ל-GnRH. GnRH מגרה את שחרורם של LH ו-FSH מהיפופיזה הקדמית. שיא LH: FSH ביחס לחולי CPP דומה ליחס של נשים בגיל ההתבגרות. נקבות עם PT הראו יחס LH: FSH נמוך מנקבות גיל ההתבגרות.[9] החסרונות של בדיקת הגירוי של GnRH הוא שלוקח זמן רב לביצוע ודורש אוספים מרובים מהמטופל, מה שהופך את התהליך לזמן ארוך ולא נוח. הבדיקה היא מאוד ספציפית אך יש לה רגישות נמוכה מכיוון שתגובת ההורמון LH נצפית בדרך כלל בשלבים מאוחרים יותר של CPP.[5] ישנן חפיפות גם בערך הצפוי בתוצאות בדיקת GnRH של אנשים עם CPP ו-PT.[1]
גישה אבחנתית משולבת[עריכת קוד מקור | עריכה]
גישה אבחנתית משולבת ב-CPP פירושה שיש לשלב שילוב של כל אולטרסאונד האגן והבדיקות הביוכימיות עם תצפית, כדי להבטיח ש-PT לא יתקדם ל CPP.[1]
מחקר[עריכת קוד מקור | עריכה]
חשיפה לגורמים סביבתיים[עריכת קוד מקור | עריכה]
סחורות טבעיות כמו שומר פשוט, לבנדר ושמן עץ התה נקשרו ל-PT. לבנדר ושמן עץ התה הם בעלי פעילויות אסטרוגניות חלשות. תכונות אסטרוגניות אלו עלולות לגרום לחוסר איזון במסלולי האיתות האנדוקריניים, מה שמוביל ל PT אצל משתמשים רגילים במוצרים אלה.[1] תה שומר נחקר כמשבש אנדוקריני הקשור ל-PT. שמן זרעי השומר מכיל אנתול תרכובת עם השפעות אסטרוגניות. התה מכיל שמן זרעי שומר ושימוש קבוע מביא לעלייה ברמות האסטרדיול אצל התינוק. לתינוקות עם PT – שומר הקשורה ל-PT קיבלו את התה כתרופה הומאופתית לחוסר שקט. התה נצרך לפחות ארבעה חודשים לפני הצגת תסמיני PT. PT הנובע מתה שומר שוכך כחצי שנה לאחר הפסקת השימוש בתה שומר.[10]
לפטין[עריכת קוד מקור | עריכה]

לפטין הוא הורמון אדיפוציטים שיש לו השלכות חשובות על גיל ההתבגרות והפרשת הורמון המין. לפטין מוגבר נקשר להפרשת אסטרוגן ואסטרדיול. ללפטין תפקידים מרכזיים בשמירה על הרכב הגוף המתאים לגיל ומשקל הרצוי. קולטני לפטין נמצאים גם בתאי אפיתל החלב ולפטין נצפה כגורם גדילה ברקמת השד. במקרים מסוימים של PT נצפו רמות מוגברות של לפטין. העלייה ברמות הלפטין גורמת לעלייה ברמות האסטרדיול ולהתפתחות רקמת השד.[7]
מוטציה גנטית GNAS1[עריכת קוד מקור | עריכה]
צורת ה-PT עם היפרטרופיה משתנה בחולים נקשרה להפעלת מוטציות בגן GNAS1. מוטציה זו מהווה מספר מצומצם של מקרים של PT.[6]
ראו גם[עריכת קוד מקור | עריכה]
קישורים חיצוניים[עריכת קוד מקור | עריכה]
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Khokar A, Mojia A, Premature Thelarche, Pediatric Annals, 1 47, 2018, עמ' 12-15 doi: 10.3928/19382359-20171214-01
- ^ 1 2 3 4 5 Rezkalla J, Von Wald T, Hansen KA, Premature Thelarche and the PURA Syndrome, Obstetrics and Gynecology 129, June 2017, עמ' 1037-1039 doi: https://journals.lww.com/greenjournal/Fulltext/2017/06000/Premature_Thelarche_and_the_PURA_Syndrome.12.aspx
- ^ 1 2 3 4 Sømod ME, Vestergaard ET, Kristensen K, Birkebæk NH, Increasing incidence of premature thelarche in the Central Region of Denmark – Challenges in differentiating girls less than 7 years of age with premature thelarche from girls with precocious puberty in real-life practice, International Journal of Pediatric Endocrinology, 2016 doi: 10.1186/s13633-016-0022-x
- ^ ד"ר ליאת דה-פריס, פרופ' משה פיליפ, טיפול באנלוגים ל-GnRH בהתבגרות מינית מוקדמת – Treatment of precocious puberty with GnRH analogs, Israeli Journal of Pediatrics גיליון מס' 70, דצמבר 2009
- ^ 1 2 3 4 5 6 7 Lee SH, Joo EY, Lee JE, Jun YH, Kim MY, The Diagnostic Value of Pelvic Ultrasound in Girls with Central Precocious Puberty, Chonnam Medical Journal 52, January 2016, עמ' 4-70 doi: 10.4068/cmj.2016.52.1.70 קישור=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4742613/
- ^ 1 2 Codner E, Román R, Premature thelarche from phenotype to genotype, Pediatric Endocrinology Reviews 5, 2008, עמ' 5-760
- ^ 1 2 3 Dundar B, Pirgon O, Sangun O, Doguc DK, Elevated leptin levels in nonobese girls with premature thelarche, Journal of Investigative Medicine, 6 61, August 2013, עמ' 8-984 doi: 10.2310/JIM.0b013e31829cbe20
- ^ Román R, Johnson MC, Codner E, Boric MA, áVila A, Cassorla F, Activating GNAS1 gene mutations in patients with premature thelarche, The Journal of Pediatrics, 2 145, August 2004, עמ' 22-218 doi: 10.1016/j.jpeds.2004.05.025
- ^ Zevenhuijzen H, Kelnar CJ, Crofton PM, "Diagnostic utility of a low-dose gonadotropin-releasing hormone test in the context of puberty disorders", Hormone Research, 4 62, 2014, עמ' 76-168 doi: 10.1159/000080324
- ^ Okdemir D, Hatipoglu N, Kurtoglu S, Akın L, Kendirci M, Premature thelarche related to fennel tea consumption?, Journal of Pediatric Endocrinology & Metabolism, 1-2 27, January 2014, עמ' 9-175 doi: 10.1515/jpem-2013-0308
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.
