התורה האטומית – הבדלי גרסאות
מ ←הולדתה |
מ ←הולדתה |
||
| שורה 33: | שורה 33: | ||
2NO + O<sub>2</sub> → 2NO<sub>2</sub> |
2NO + O<sub>2</sub> → 2NO<sub>2</sub> |
||
אך כאשר הוא חזר על התגובה הכימית תחת תנאים אחרים, כמות כפולה בדיוק של תחמוצת החנקן (יחס של 1:2) הגיבה בשלמות עם החמצן ליצירת תוצר שונה - הידוע כיום כ[[דו חנקן תלת חמצני]] (N<sub>2</sub>O<sub>3</sub>) |
אך כאשר הוא חזר על התגובה הכימית תחת תנאים אחרים, כמות כפולה בדיוק של תחמוצת החנקן (יחס של 1:2) הגיבה בשלמות עם החמצן ליצירת תוצר שונה - הידוע כיום כ[[דו חנקן תלת חמצני]] (N<sub>2</sub>O<sub>3</sub>): |
||
4NO + O<sub>2</sub> → 2N<sub>2</sub>O<sub>3</sub> |
4NO + O<sub>2</sub> → 2N<sub>2</sub>O<sub>3</sub> |
||
גרסה מ־23:33, 27 באוגוסט 2008
| ערך זה משתתף בתחרות הכתיבה "מקצרמר למובחר" של ויקיפדיה העברית והוא בשלבי כתיבה. הערך הגיע לשלב הסופי של יצירתו, וכותבו מעוניין כעת בהערותיכם ובהשגותיכם בדף השיחה. לרשימת הערכים המשתתפים בתחרות גשו לכאן. תודה על שיתוף הפעולה ובהצלחה! |
בכימיה ופיזיקה, התורה האטומית היא תאוריה העוסקת בטיבו של החומר, וקובעת כי החומר עשוי מיחידות נפרדות "סופיות" הקרויות אטומים, בניגוד לדעה הקודמת לפיה ניתן לחלק את החומר ליחידות קטנות כרצוננו עד אינסוף. היא החלה כרעיון פילוסופי ביוון העתיקה והודו, ונכנסה לזרם המרכזי במדע בראשית המאה ה-19, כאשר תגליות בתחום הכימיה הראו כי החומר אכן מתנהג כעשוי מחלקיקים.
השם "אטום" (מהמילה היוונית "אטומוס", "בלתי ניתן לחלוקה") ניתן לחלקיק הבסיסי שמרכיב את היסודות הכימים, מאחר שהכימאים האמינו באותה תקופה כי לא ניתן לחלקו יותר. ובכל זאת, בתחילת המאה ה-20, באמצעות ניסויים שונים בתחום האלקטרומגנטיות והרדיואקטיביות, פיזיקאים גילו כי "האטום הבלתי ניתן לחלוקה" הוא למעשה גוש של חלקיקים תת-אטומים (אלקטרונים, פרוטונים ונייטרונים) אשר עשויים להתקיים גם בנפרד. זאת ועוד, בתנאים קיצוניים כגון בתוך כוכב נייטרונים, טמפרטורות גבוהות במיוחד ולחץ קיצוני מונעים מהאטומים להתקיים מלכתחילה, ורק החלקיקים התת-אטומים לבדם קיימים. התחום במדע אשר חוקר את החלקיקים התת-אטומים הוא פיזיקת החלקיקים, והפיזיקאים העוסקים בו מקווים לגלות את טיבו היסודי האמיתי של החומר.
אטומיזם פילוסופי
הרעיון לפיו החומר מורכב מיחידות בדידות ולא ניתן לחלקו ליחידות קטנות יותר היה קיים במשך אלפי שנים, אך רעיונות אלה התבססו על טיעונים פילוסופים אבסטרקטים ולא על ניסויים מדעיים. טיבם של האטומים בפילוסופיה היה שונה בצורה ניכרת בתקופות שונות ואצל תרבויות ואסכולות שונות, ולעתים נכללו בו אף אלמנטים רוחניים. הרעיון הבסיסי של האטום אומץ ע"י מדענים אלפי שנים מאוחר יותר, מאחר שהסביר באופן אלגנטי תגליות חדשות בתחום הכימיה.
הודו
חלק מהתיאוריות המוקדמות ביותר הידועות פותחו בהודו העתיקה במאה ה-6 לפני הספירה ע"י קאנדה, פילוסוף הינדי.[1] בפילוסופיה ההינדית, אסכולות הניאיה והוייששיקה פיתחו תיאוריות נרחבות שעסקו בדרכים בהן אטומים התגבשו ליצירת עצמים מורכבים יותר (ראשית בזוגות, ואז בשלשות של זוגות),[1] אך האמינו כי האינטראקציות נקבעו בסופו של דבר על ידי רצונו של האל (אישורה ההינדי), ושהאטומים עצמם היו בלתי פעילים, ללא תכונות פיזיקליות משל עצמם. מנגד, הפילוסופיה של הג'ייניזם קישרה בין התנהגות החומר לטבעם של האטומים עצמם. בפילוסופיה זו, לכל אטום היה סוג אחד של טעם, ריח וצבע ושני סוגים של מגע, אם כי לא ברור כיום למה הייתה הכוונה ב"סוג של מגע". אטומים עשויים להתקיים באחד משני מצבים: קטן, בו הם יכולים להיכנס לחללים קטנים ככל הנדרש, וגדול, בו הם מוארכים ותופסים נפח סופי בחלל. אמנם אטומים עשויים מאותו חומר יסודי, אך הם עשויים להשתלב בהתאם לתכונותיהם הבסיסיות וליצור שישה סוגים של "גושים", אשר נראה כי הם תואמים את המושג היווני של "יסודות": אדמה, מים, צל, "עצמי חושים", "חומר קארמי" ו"חומר שאינו כשר".[2]
יוון
במאה ה-5 לפני הספירה, דמוקריטוס פיתח את מושג האטומים על מנת לפשר בין שתי אסכולות שונות שעסקו בטיבה של המציאות. מצד אחד היה הרקליטוס, אשר האמין כי השינוי הוא טבעו של הקיום. מצד שני היה פרמנידס, אשר האמין כי השינוי הוא רק אשליה.
פרמנידס שלל את קיומם של תנועה, שינוי וריק. הוא האמין כי המציאות כולה היא מסה יחידה ובלתי משתנה - מושג הידוע כמוניזם, וכי שינוי ותנועה הם אשליות בלבד. מסקנה זו, וכן הטיעונים שהביאו אליה, עשויים להיראות מוזרה כאשר מתבוננים בה באמצעות השיטה האמפירית המודרנית, אך פרמנידס דחה מפורשות את התפיסה החושית כדרך להבנת היקום, והשתמש במקום זאת בטיעונים מופשטים טהורים. ראשית, הוא האמין כי אין חלל ריק במציאות, והמושג שקול לאי-קיום: "אם הריק קיים, אזי הוא אינו שום דבר; ולכן הוא אינו ריק". מכאן הוא הסיק כי תנועה היא בלתי אפשרית, מאחר שאין ריק שאפשר לנוע לתוכו.[3] הוא כתב גם כי "קיום" חייב להיות שלמות בלתי ניתנת לחלוקה, כי אם הוא היה ניתן לחלוקה, אזי היה קיים ריק שיכול היה לחלק אותו לחלקים קטנים יותר - והרי הריק אינו קיים. לבסוף, הוא קבע כי השלמות חובקת-הכל אינה יכולה להשתנות, מאחר שהיא כבר כוללת בתוכה את כל מה שקיים ושעשוי להתקיים.
דמוקריטוס קיבל את רוב טיעוניו של פרמנידס, פרט לרעיון לפיו השינוי הוא אשליה. הוא האמין כי השינוי הוא אמיתי, וגם אם אין בו אמת, עדיין יש להסביר את מהות האשליה. לכן הוא תמך במושג של חלל ריק, וקבע כי היקום עשוי מישויות "פרמנידיות" בלתי ניתנות לחלוקה אשר נעות בריק. ישויות אלה, אשר הינן "קיימות", הן אם כך בלתי ניתנות לשינוי ולחלוקה ("אטומוס", המילה היוונית ל"בלתי ניתן לחיתוך"), אך הסידור שלהן בחלל משתנה כל הזמן. כל האטומים של דמוקריטוס היו עשויים מאותו חומר, אך היו בעלי מגוון בלתי-מוגבל של צורות וגדלים; תכונה זו, ביחד עם האפשרויות השונות לסידורם בחלל, הסבירה את כל החומרים והעצמים השונים ביקום.[4]
אסלאם
במהלך המאה ה-11 (תור הזהב של האסלאם), אטומיסטים איסלאמים פיתחו תיאוריות אטומיות אשר היוו מיזוג של האטומיזם היווני וההודי. הרעיונות העתיקים של היוונים וההודים פותחו ונוספו עליהם רעיונות איסלאמים חדשים, כגון האפשרות לקיומם של חלקיקים קטנים מן האטום. האסכולה המצליחה ביותר של האטומיזם האיסלאמי הייתה האסכולה הפילוסופית של אשרית, אשר באה לידי ביטוי במיוחד בעבודתו של הפילוסוף אל-גזלי (1058-1111). באטומיזם אשריתי, האטומים הם העצמים הגשמיים הנצחיים היחידים שבנמצא, וכל שאר תכולתו של העולם היא "מקרית", או ארעית. דבר מקרי אינו יכול להיות הסיבה לשום דבר אחר, פרט לתחושות, מאחר שהוא קיים לרגע קצר בלבד. מקרים בלתי צפויים אינם נגרמים מסיבות פיזיות טבעיות, אלא הם תוצאה ישירה של התערבותו הבלתי-פוסקת של אלוהים, בלעדיה שום דבר אינו יכול להתקיים. מכאן, הטבע תלוי באלוהים באופן מוחלט, רעיון אשר משתלב עם רעיונות אשריתים איסלאמים אחרים העוסקים בסיבתיות או בהעדר סיבתיות.[5]
התיאוריה האטומית המודרנית
הולדתה

בראשית המאה ה-19, ג'ון דלטון פיתח את התיאוריה האטומית שלו, בה הציע כי כל יסוד כימי מורכב מאטומים מסוג אחד ויחיד, אשר הם בלתי ניתנים לשינוי או להשמדה, אך עשויים להתאחד על מנת ליצור מבנים מורכבים יותר - תרכובות כימיות. לא ברור כיצד בדיוק הגיע דלטון לתיאוריה שלו, אך בכל מקרה, היא אפשרה לו להסביר מגוון של תגליות חדשות בכימיה שנעשו בידיו ובידי עמיתיו.
התגלית הראשונה הייתה חוק שימור החומר, אשר ניסח אנטואן לבואזיה ב-1789, וקובע כי סך המסה בתגובה כימית נשאר קבוע, כלומר למגיבים אותה מסה כוללת כמו לתוצרים.[6] דלטון הסיק מחוק זה כי החומר אינו ניתן להשמדה.
התגלית השניה הייתה חוק היחסים הקבועים. את החוק הוכיח הכימאי הצרפתי ז'וזף לואי פרוסט ב-1799.[7] חוק זה טוען כי אם תרכובת מתפרקת למרכיביה היסודיים, אזי המסות של המרכיבים יהיו תמיד באותו יחס, ללא קשר לכמות או למקור של התרכובת המקורית. כך לדוגמא אם נפרק מים למרכיביהם - חמצן ומימן - נקבל תמיד שמסת החמצן הנוצר היא פי שמונה מסת המימן הנוצר, מכיוון שמולקולת המים מכילה אטום חמצן שמסתו 16 יחידות אטומיות, ושני אטומי מימן שמסתם 1. פרוסט יצר נחושת פחמתית במספר רב של דרכים, ומצא שבכל פעם המרכיבים היו באותה כמות יחסית כפי שהיו כאשר הוא פירק נחושת פחמתית טבעית.
דלטון למד את עבודתו של פרוסט והרחיב אותה באמצעות פיתוח חוק היחסים הכפולים: אם שני יסודות עשויים ליצור יותר מתרכובת אחת, אזי היחסים בין המסות של היסוד השני, כאשר הן משתלבות עם מסה קבועה של היסוד הראשון, יהיו יחסים של מספרים שלמים קטנים. זוג אחד של תגובות אשר חקר דלטון היו צירופים של "אוויר חנקני", אשר ידוע כיום כתחמוצת החנקן (NO), עם חמצן (O2). תחת תנאים מסוימים, גזים אלו הרכיבו תוצר שהיה בלתי ידוע בזמנו - אשר היום אנו יודעים כי הוא היה דו-תחמוצת החנקן (NO2) - ביחס צירוף מסוים:
2NO + O2 → 2NO2
אך כאשר הוא חזר על התגובה הכימית תחת תנאים אחרים, כמות כפולה בדיוק של תחמוצת החנקן (יחס של 1:2) הגיבה בשלמות עם החמצן ליצירת תוצר שונה - הידוע כיום כדו חנקן תלת חמצני (N2O3):
4NO + O2 → 2N2O3
דלטון האמין גם כי התורה האטומית תוכל להסביר מדוע המים סופגים גזים שונים ביחסים שונים; לדוגמה, הוא מצא כי מים סופגים פחמן דו חמצני הרבה יותר טוב משהם סופגים חנקן. דלטון טען כי ההבדל היה נעוץ בהבדלי המסות והמורכבות של החלקיקים שמרכיבים את הגזים. ואכן, מולקולות פחמן דו חמצני (CO2) הן כבדות וגדולות יותר ממולקולות חנקן (N2).
ב-1803 הציג דלטון בעל-פה את הרשימה הראשונה שלו של משקלים אטומים של מספר חומרים. המאמר פורסם ב-1805, אך דלטון לא ציין בו כיצד הוא הגיע לערכים אלו.[8] השיטה נחשפה לראשונה ב-1807 ע"י ידידו תומס תומסון, במהדורה השלישית של ספר הלימוד של תומסון, "מערכת הכימיה". בסופו של דבר פירסם דלטון הסבר מלא בספר הלימוד שלו, "מערכת חדשה של פילוסופיה כימית", בשנים 1808 ו-1810.
דלטון העריך את המשקלים האטומים באמצעות יחסי המסות בהם הם התרכבו, כאשר המימן היווה את היחידה הבסיסית. למרות זאת, דלטון לא הבין כי ביסודות מסוימים, האטומים קיימים בצורה טבעית כמולקולות - לדוגמה, חמצן טהור קיים בטבע כ-O2. הוא גם האמין, בצורה שגויה, כי התרכובת הפשוטה ביותר של שני יסודות תמיד מכילה אטום אחד מכל סוג (כלומר, מים הם HO ולא H2O).[9] טעויות אלה, נוסף על חוסר בדיוק של הציוד בו הוא השתמש, גרמו לטבלה שתהיה בעלת שגיאות רבות. לדוגמה, הוא האמין כי אטומי חמצן היו כבדים פי 5.5 מאטומי מימן, מאחר שבמים הוא מדד 5.5 גרם של חמצן לכל גרם אחד של מימן. אטום חמצן הוא למעשה כבד פי 16 מאטום מימן.
הפגמים בתיאוריה של דלטון תוקנו ב-1811 ע"י אמדאו אבוגדרו. אבוגדרו הציע כי נפחים שווים של כל שני גזים, בטמפרטורה ולחץ שווים, מכילים מספר שווה של מולקולות - במלים אחרות, המסה של חלקיקי הגז אינה משפיעה על נפחו.[10] חוק אבוגדרו איפשר לו להסיק את טבעם הדו-אטומי של גזים רבים ע"י מדידת הנפחים בהם הם יצרו תגובות. לדוגמה: מאחר ששני ליטרים של מימן מגיבים עם ליטר אחד בלבד של חמצן ליצירת שני ליטר של אדי מים (בלחץ וטמפרטורה קבועים), הרי שמולקולת חמצן יחידה מתפרקת לשני חלקים ליצירת שני חלקיקי מים. לכן אבוגדרו הצליח להציע הערכות מדויקות יותר למשקל האטומי של חמצן ויסודות רבים אחרים, ולבסס את ההבחנה בין מולקולות ואטומים.
ב-1827, הבחין הבוטנאי רוברט בראון כי חלקיקי אבקה אשר צפו במים התנועעו בקביעות ללא סיבה נראית לעין. ב-1905, אלברט איינשטיין שיער כי התנועה הבראונית הזו נגרמת ע"י מולקולות מים אשר פוגעות ללא הרף בחלקיקי האבקה, ופיתח מודל מתמטי משוער שתיאר אותה.[11] המודל אושר בניסוי ב-1908 ע"י הפיזיקאי הצרפתי ז'אן בפטיסט פרין, וסיפק אישור נוסף לתיאוריה החלקיקית (ומכאן, לתיאוריה האטומית).
גילוי החלקיקים התת-אטומים

האטומים נחשבו לחלקיקים הקטנים ביותר של החומר, עד שב-1897 גילה ג' ג' תומסון את האלקטרון באמצעות עבודתו עם קרניים קתודיות.[12] שפופרת קרוקס היא מיכל זכוכית אטום ובו שתי אלקטרודות מופרדות באמצעות ריק. כאשר יוצרים מתח חשמלי באלקטרודות, נוצרות קרניים קתודיות, אשר גורמות לשטח קטן לזהור במקום בו הן פוגעות בזכוכית, בצדו השני של המיכל. באמצעות ניסויים, גילה תומסון כי הקרניים עשויות להיות מוסטות באמצעות שדה חשמלי (בנוסף להטיה באמצעות שדה מגנטי, אשר הייתה כבר ידועה). הוא הסיק כי קרניים אלו לא היו גלים, אלא חלקיקים טעונים שלילית להם הוא קרא "גופיפים". מאוחר יותר קיבלו החלקיקים את שמם המוכר כיום, אלקטרונים.
תומסון האמין כי הגופיפים נוצרו מהאטומים שבאלקטרודות. מכאן הוא הסיק, כי את האטומים ניתן לחלק, וכי הגופיפים היו אבני הבניין שלהם. על מנת להסביר את מטענו הנייטרלי של האטום בכללותו, הוא הניח כי הגופיפים פוזרו בים או ענן של מטען חשמלי; מודל זה ידוע כמודל עוגת הצימוקים.[13]
מאחר שנתגלה כי האטומים דווקא כן ניתנים לחלוקה, בסתירה לשמם, הפיזיקאים המציאו מאוחר יותר את המונח חלקיקים יסודיים לתיאור חלקיקים שהינם באמת בלתי ניתנים לחלוקה.
גילוי הגרעין

למעלה - התוצאות המשוערות: חלקיקי אלפא עוברים דרך אטום "עוגת צימוקים", הסטיות במסלול הן מזעריות.
למטה - התוצאות בפועל: חלק קטן של החלקיקים הוסטו מנתיבם בצורה ניכרת, דבר המצביע על קיומו של מטען חיובי המרוכז בשטח קטן.
מודל עוגת הצימוקים של תומסון הופרך ב-1909 ע"י אחד מתלמידיו, ארנסט רתרפורד, אשר גילה כי רוב המסה והמטען החיובי של האטום מרוכז בחלק קטן מאוד מנפחו, כנראה בדיוק במרכז.
בניסוי עלה הזהב, הנס גייגר וארנסט מרסדן - עמיתים של רתרפורד אשר עבדו בהדרכתו - שיגרו חלקיקי אלפא דרך יריעה דקה של זהב ולעבר מסך פלואורסנט אשר הקיף את היריעה.[14] עקב המסה הזעירה של האלקטרונים, התנע הגבוה של חלקיקי האלפא והפיזור האחיד של המטען החשמלי שנחזה ע"י מודל עוגת הצימוקים, הנסיינים ציפו כי כל חלקיקי האלפא יעברו דרך האטומים ללא הסטה ניכרת, או יספגו בהם. לתדהמתם, חלק קטן מחלקיקי האלפא חוו הסטה משמעותית. תוצאה זו הביאה את רתרפורד להציע את המודל הפלנטרי של האטום, בו אלקטרונים נקודתיים נעו במסלולים בחלל מסביב לגרעין האטום - כמו כוכבי הלכת (פלנטות) הנעים סביב השמש.[15]
גילוי האיזוטופים
ב-1913, בעת ניסויים עם תוצרי התפרקויות גרעיניות, הרדיוכימאי פרדריק סודי הבחין כי נראה שיש יותר מיסוד אחד בכל תא בטבלה המחזורית.[16] המונח איזוטופ נטבע עבור היסודות האלו ע"י מרגרט טוד.
באותה שנה, ג' ג' תומסון ערך ניסוי בו הוא ניתב זרם של יוני נאון דרך שדות מגנטים וחשמליים, אשר פגעו בלוח צילום בצד השני. תומסון הבחין בשני אזורים זוהרים על לוח הצילום, אשר הצביעו על שני מסלולי הסטה שונים. תומסון הסיק מכאן כי לחלק מיוני הנאון הייתה מסה שונה מלאחרים, ולכן הם נעו במסלול אחר. [17] טבעה של המסה המשתנה יוסבר לאחר מכן ע"י גילוי הנייטרונים ב-1932.
גילוי החלקיקים הגרעיניים
ב-1918, ארנסט רתרפורד הפציץ גז חנקן בחלקיקי אלפא והבחין כי גרעיני מימן נפלטו מן הגז. רתרפורד הסיק כי גרעיני המימן בקעו מגרעיני החנקן עצמם - כלומר, הוא ביקע את האטום. [18] מאוחר יותר הוא גילה כי המטען החיובי של כל אטום שווה תמיד לזה של מספר שלם של גרעיני מימן. גילוי זה, בנוסף לעובדה כי המימן היה היסוד הקל ביותר הידוע, וכי המסה האטומית של כל יסוד אחר היתה כפולה שלמה בקירוב של המסה האטומית של המימן, הביאו אותו למסקנה כי גרעיני המימן הינם חלקיקים ייחודיים והם המרכיבים היסודיים של כל הגרעינים האטומים: פרוטונים. ניסויים נוספים שערך רתרפורד מצאו כי מסת הגרעינים של רוב האטומים עולה על זו של הפרוטונים שבגרעין. הוא הניח כי המסה העודפת מורכבת מחלקיק שהיה בלתי ידוע עד אז, שהיה בעל מטען חשמלי נייטרלי; לחלקיקים אלה הוא קרא באופן זמני "נייטרונים".
ב-1928, ואלתר בותה הבחין כי כאשר מפציצים בריליום בחלקיקי אלפא, הוא פולט קרינה נייטרלית מבחינה חשמלית, אשר חודרת דרך חומר בקלות. מאוחר יותר נתגלה כי קרינה זו עשויה לשחרר אטומי מימן מתוך שעוות פרפין. בתחילה סברו כי זו קרינת גמא, מאחר שלקרינה זו (המורכבת מפוטונים באנרגיה גבוהה) הייתה השפעה דומה על אלקטרונים במתכת, אך ג'יימס צ'דוויק מצא כי אפקט היינון היה חזק מכדי להיגרם ע"י קרינה אלקטרומגנטית. ב-1932 הוא חשף יסודות שונים כגון מימן וחנקן ל"קרינת הבריליום" המסתורית, ובאמצעות מדידת האנרגיה של החלקיקים הטעונים הנרתעים מהחומר, הוא הסיק כי הקרינה הורכבה למעשה מחלקיקים נייטרלים, בעלי מסה דומה לזו של הפרוטון - הנייטרונים. [19] על גילוי הנייטרונים קיבל צ'דוויק את פרס נובל בשנת 1935.
המודל הקוונטי של האטום
המודל הפלנטרי של האטום סבל ממספר בעיות. ראשית, לפי נוסחת לרמור של תורת החשמל והמגנטיות הקלאסית, מטען חשמלי מאיץ פולט גלים אלקטרומגנטים; מכאן, חלקיק בעל מטען חשמלי, כגון האלקטרון, יאבד אנרגיה בקצב קבוע וינוע במסלולים קרובים יותר ויותר לגרעין, עד שיתנגש בו תוך שבריר שניה. תופעה נוספת שהמודל הפלנטרי לא הצליח להסביר היא מדוע אטומים מעוררים פולטים קרינה בספקטרום שאינו רציף - כלומר, רק באורכי גל מסוימים.
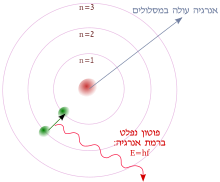
תורת הקוונטים גרמה למהפכה רבתי בפיזיקה בתחילת המאה ה-20, כאשר מקס פלאנק ואלברט איינשטיין העלו את ההשערה כי אנרגיית האור נפלטת או נקלטת במנות בדידות הקרויות קוונטים. ב-1913, נילס בוהר שילב את הרעיון הזה במודל האטום של בוהר, בו האלקטרונים מקיפים את הגרעין אך ורק במסלולים מסוימים בעלי ערכים קבועים של תנע זוויתי ואנרגיה, כאשר המרחק מהגרעין - רדיוס המסלול - הינו פרופורציונלי לאנרגיה של האלקטרון. במודל זה, האלקטרונים לא קרסו אל עבר האלקטרון, מאחר שהם לא יכלו לאבד אנרגיה בצורה רציפה; במקום זאת, הם יכלו לבצע רק קפיצות קוונטיות בין רמות האנרגיה הקבועות מראש. כאשר זה קרה, נפלט או נקלט אור בתדירות פרופורציונלית לשינוי באנרגיה - ומכאן התדירויות הבדידות של האור שנצפו בתהליך זה. [20]
המודל של בוהר הצליח לחזות רק את קווי הספקטרום של המימן; הוא לא הצליח לחזות את אלה של אטומים מרובי אלקטרונים. וחמור מכך, כאשר טכנולוגיית הספקטרוגרפיה השתפרה, נתגלו גם באטום המימן קווי ספקטרום נוספים, אשר מודל בוהר לא הצליח להסביר אותם. ב-1916, ארנולד זומרפלד הוסיף מסלולים אליפטים למודל בוהר, על מנת להסביר את קווי הפליטה הנוספים, אך שינוי זה הפך את המודל לקשה מאוד לשימוש, והוא עדיין לא פתר את בעיית האטומים מרובי האלקטרונים.
ב-1924, לואי דה ברויי שיער כי כל החלקיקים הנעים - ובפרט, חלקיקים תת-אטומים כגון אלקטרונים - מפגינים תכונות דמויות-גל. ארווין שרדינגר, אשר הוקסם מהרעיון, חקר האם ניתן להסביר את תנועתם של האלקטרונים באטום כגלים ולא כחלקיקים. משוואת שרדינגר, אשר פורסמה ב-1926, [21] מתארת את האלקטרון כפונקציית גל במקום כחלקיק נקודתי, והיא חזתה בצורה אלגנטית רבות מהתופעות הספקטרליות אשר מודל בוהר נכשל בהסברתן. למרות שרעיון זה היה נוח מבחינה מתמטית, היה קשה להמחישו בדמיון, והוא נתקל בהתנגדות. [22] אחד ממבקריו, מקס בורן, שיער כי פונקציית הגל של שרדינגר לא תיארה את האלקטרון, אלא את כל המצבים האפשריים שלו, ולכן ניתן להשתמש בה על מנת לחשב את ההסתברות למציאת אלקטרון בכל מיקום נתון מסביב לגרעין. [23]

מאחר שפונקציית גל כוללת זמן בנוסף למיקום, אין זה אפשרי להפיק ממנה ערכים מדויקים הן עבור המיקום והן עבור התנע של חלקיק בכל נקודה נתונה בזמן; עקרון זה ידוע כעקרון אי-הוודאות. עקרון זה סתר את מודל בוהר, עם המסלולים המעגליים המסודרים והמוגדרים היטב שלו. המודל המודרני של האטום מתאר את מיקומי האלקטרונים באטום במונחים של הסתברויות. אלקטרון עשוי, באופן פוטנציאלי, להימצא בכל מרחק אפשרי מהגרעין, אך - בתלות ברמת האנרגיה שלו - נוטה להתקיים לעתים קרובות יותר באזורים מסוימים מסביב לגרעין מאשר מבאחרים. האזור בו הסיכוי למציאת אלקטרון מסוים הוא מירבי נקרא אורביטל אטומי.
ראו גם
הערות שוליים
- ^ 1 2 Teresi, Dick (2003). Lost Discoveries: The Ancient Roots of Modern Science. Simon & Schuster. pp. 213–214. ISBN 074324379X.
- ^ Gangopadhyaya, Mrinalkanti. Indian Atomism: History and Sources. Atlantic Highlands, New Jersey: Humanities Press, 1981. ISBN 0-391-02177-X
- ^ Bertrand Russel. (1946). History of Western Philosophy. pg 75. ISBN 0-415-32505-6
- ^ Andre G. van Melsen. (1952) From Atomos to Atom. ISBN 0-486-49584-1
- ^ Gardet, L. “djuz’” in Encyclopaedia of Islam CD-ROM Edition, v. 1.1. Leiden: Brill, 2001.
- ^ Weisstein, Eric W. "Lavoisier, Antoine (1743-1794)." scienceworld.wolfram.com.
- ^ Proust, Joseph Louis. "Researches on Copper", excerpted from Ann. chim. 32, 26-54 (1799) [as translated and reproduced in Henry M. Leicester and Herbert S. Klickstein, A Source Book in Chemistry, 1400-1900 (Cambridge, MA: Harvard, 1952)].
- ^ Dalton, John. "On the Absorption of Gases by Water and Other Liquids", in Memoirs of the Literary and Philosophical Society of Manchester. 1803.
- ^ Johnson, Chris. "Avogadro - his contribution to chemistry."
- ^ Avogadro, Amedeo. "Essay on a Manner of Determining the Relative Masses of the Elementary Molecules of Bodies, and the Proportions in Which They Enter into These Compounds." 1811. Journal de Physique, 73, 58-76.
- ^ Einstein, Albert. "On the Movement of Small Particles Suspended in Stationary Liquids Required by the Molecular-Kinetic Theory of Heat." Annal der Physik.
- ^ Thomson, J.J. "Cathode rays." Philosophical Magazine, 44, 293 (1897). [facsimile from Stephen Wright, Classical Scientific Papers, Physics (Mills and Boon, 1964).]
- ^ Thomson, J.J. "On the Structure of the Atom: an Investigation of the Stability and Periods of Oscillation of a number of Corpuscles arranged at equal intervals around the Circumference of a Circle; with Application of the Results to the Theory of Atomic Structure." Philosophical Magazine March 1904. Series 6, Vol 7, No 39.
- ^ Geiger, H. "The Scattering of the α-Particles by Matter." Proceedings of the Royal Society February 17, 1910. Series A 82: 495–500.
- ^ Rutherford, Ernest. "The Scattering of α and β Particles by Matter and the Structure of the Atom." Philosophical Magazine. May 1911. Series 6, Vol. 21.
- ^ "Frederick Soddy, The Nobel Prize in Chemistry 1921". Nobel Foundation. נבדק ב-2008-01-18.
- ^ Thomson, J.J. "Rays of positive electricity." Proceedings of the Royal Society. 1913. A 89, 1–20 [as excerpted in Henry A. Boorse & Lloyd Motz, The World of the Atom, Vol. 1 (New York: Basic Books, 1966)].
- ^ Rutherford, Ernest. "Collisions of alpha Particles with Light Atoms. IV. An Anomalous Effect in Nitrogen." Philosophical Magazine. 1919. 6th series, 37, 581.
- ^ Chadwick, James. (February 27, 1932), "Possible Existence of a Neutron." Nature. February 27, 1932. p. 312
- ^ Bohr, N. "On the constitution of atoms and molecules." Philosophical Magazine. July 1913. 26, 1-25.
- ^ Schrödinger, Erwin. "Quantisation as an Eigenvalue Problem." Annalen der Physik.
- ^ Mahanti, Subodh. "Erwin Schrödinger: The Founder of Quantum Wave Mechanics."
- ^ Mahanti, Subodh. "Max Born: Founder of Lattice Dynamics."
