משתמש:Hopeshtein/טיוטה
פתיח :[עריכת קוד מקור | עריכה]
בגוף האדם קיימת מערכת חיסונית, שמגינה עלינו מפני פלישה של מזהמים ורעלנים
המערכת הזאת פועלת בשני קווים - על ידי תאים שבולעים את הפולש מצד אחד (כדוריות הדם הלבנות מסוג T), ועל ידי תאים (כדוריות דם לבנות מסוג B) המייצרים פרודות (מולקולות) חלבוניות ייעודיות שנקראות נוגדנים.
הנוגדנים, כמו תאי הדם הלבנים, עוברים בגוף ממקום למקום באמצעות זרם הדם.
מערכת ההגנה הזאת מזהה תאים וחומרים זרים באמצעות מערכת מולקולות אחרות שמופיעות על גבי תא זר שנקראות - אנטיגנים.
המערכת יודעת להבדיל בין האנטיגנים של הגוף שלנו, לבין אנטיגנים זרים, שנגדם צריך "להילחם".
מערכת ההגנה מייצרת את הנוגדנים רק אחרי שהיא פוגשת את הפולש עם האנטיגן הזר בפעם הראשונה, והנוגדנים הנוצרים "יודעים" להתחבר רק לאותו סוג אנטיגן ולא לאנטיגן אחר, כמו מפתח ומנעול שמתאימים רק אחד לשני.
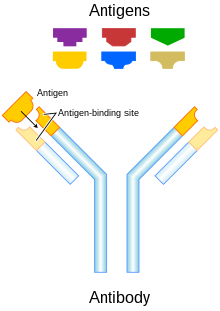
הנוגדן בנוי בצורת האות Y , כאשר ה"רגל" היא החלק האחורי, ושתי ה"ידיים" הן החלק המתחבר (המפתח) לאנטיגן (מנעול). חיבור זה נקרא חיבור אנטיגן-נוגדן. קיימים מספר סוגי נוגדנים, אך אנו נתמקד בשני סוגים : מסוג IgG שהינו מולקולת נוגדן בסיסית יחידה וקטנה, ומסוג IgM שהינו מולקולה גדולה המורכבת מחמש יחידות IgG שמחוברות יחד בצורת מחומש (פנטאמר).
בזמן ההיריון, ישנו חילוף חומרים בין האם והעובר דרך השליה. השליה מאפשרת מעבר חומרי הזנה וחמצן לתינוק והוצאת חומרי הפסולת מהתינוק לאם, וגם עוזרת לחסום מעבר מולקולות גדולות וחיידקים. מחסום השליה חוסם מעבר נוגדנים גדולים מסוג IgM , אך מאפשר מעבר של הנוגדנים הקטנים מסוג IgG מהאם לעובר.
לעובר שהתאים שלו בנויים על סמך קוד גנטי שבא גם מהאם, אבל גם מהאב, יש באופן טבעי אנטיגנים שבאים גם מהאם וגם מהאב, המצויים על כדוריות הדם שלו.
במצב תקין, המערכת החיסונית של האם לא פועלת נגד האנטיגנים של העובר שבאים מהאב, אך קיימים מקרים שבהם לאם ישנם נוגדנים כאלו, מכיוון שנוצרו אצלה כתוצאה מחשיפה קודמת- כמו קבלת עירוי מנת דם.
באופן טבעי קיימים בגוף נוגדנים כנגד האנטיגנים של סוג הדם – קבוצת ה-ABO שאינם נמצאים על כדוריות הדם האדומות. כך למשל, אדם שיש לו סוג דם B הוא בעל נוגדנים כנגד סוג דם A . אדם שיש לו סוג דם A, יהיו לו נוגדנים נגד האנטיגנים מסוג B. נוגדנים אלו הינם לרוב מסוג IgM ולכן, אצל אישה בהריון הם לא עוברים את מחסום השליה ולא פוגעים בעובר, גם אם סוג הדם שלו שונה מזה של האם.
עד השבוע ה-28 אין מספיק מעבר דם בין העובר לאם, ולכן קיים סיכוי יחסית נמוך לחשיפה של מערכת החיסון של האם לאנטיגנים הזרים שעל כדוריות הדם האדומות של העובר.
החל משבוע זה תיתכן חשיפה ולכן עולה הסיכון להיווצרות נוגדן ספציפי. קיימים עשרות אנטיגנים שונים הקשורים לתהליך זה, אך החשובים מבחינה קלינית והנפוצים ביותר הינם אנטיגנים מקבוצת Rh (גורם רזוס) ובהם אנטיגן D (גם אנטיגן E ואנטיגן C) ואנטיגנים מקבוצת Kell.
קבוצות אלו בנויות משרשרת חלבונית ארוכה שעליה קיימים מספר אזורים (אתרים) שנוגדן יכול להתחבר אליהם. חלבון Rh הוא הראשון שהתגלה ( בשנת 1937), והאנטיגן החשוב ביותר שעליו הינו Rh-D . אם האתר D קיים על השרשרת – אז סוג הדם נחשב חיובי ( פלוס) ואם לא קיים, סוג הדם נחשב שלילי (מינוס).
Immunogenicity- הסיכוי להיווצרות נוגדן אחרי חשיפה בפעם הראשונה. באנטיגן Rh-D הסיכוי הוא הגבוה ביותר ומגיע ל-70% , כאשר הבא אחריו מבחינת הסיכוי להיווצרות נוגדן הוא האנטיגן Kell המגיע ל-10% - ז"א רק במקרה 1 מתוך 10 חשיפות לאנטיגן ייווצר נוגדן.
האם עלולה לפתח נוגדנים כנגד העובר. אחרי החשיפה הראשונית נוצרים נוגדנים מסוג IgM שלא עוברים את מחסום השלייה, אך אחרי מספר ימים נוצרים נוגדנים מסוג IgG שעוברים את המחסום ויכולים לגרום להרס (המוליזה) כדוריות הדם של העובר,
התוצאה יכולה להיות המוליזה קלה עד קשה ואף להביא למוות תוך רחמי. לרוב החשיפה הראשונית הגדולה נוצרת בזמן הלידה, כאשר מתרחש מעבר דם רב בין העובר לאם (תהליך זה נקרא Feto-Maternal Hemorrhage) [1], ולכן האם מייצרת את הנוגדן אחרי שהתינוק הראשון נולד והוא לא מושפע מכך.
קיימת גם העברה "אנכית" רבה יחסית במקרים של הפלה או פעולות פולשניות אחרות כגון בדיקת מי שפיר.
רק בהריון השני, כשכבר קיים הנוגדן שנוצר מההיריון או הלידה הראשונים, תתרחש תקיפה של הנוגדן את העובר.
זריקת Anti D[עריכת קוד מקור | עריכה]
בשל חשיבות אנטיגן Rh-D- תפוצה באוכלוסייה (85% מהאנשים "חיוביים" ו-15% "שליליים") וגם סיכוי גבוה להיווצרות נוגדן, קיים חיסון סביל הנקרא זריקת אנטי D, שבו מוזרקים לאם עם סוג דם Rh שלילי נוגדנים כנגד האנטיגן Rh-D(אישה עם סוג דם חיובי אינה זקוקה לחיסון מפני שאינה מייצרת נוגדנים כנגד האנטיגן העצמי שלה).
אם לעובר יש את האנטיגן על כדוריות הדם שלו (אם העובר Rh חיובי) אז הנוגדנים שהאם מקבלת מבחוץ ייקשרו לאנטיגן, במקרה של מעבר דם מהעובר לאם, ולמעשה יכסו ויסתירו את האנטיגן D ובכך לא יאפשרו למערכת החיסון של האם להתעורר ולייצר נוגדנים אלו בעצמה. [2]
החיסון ניתן בשבוע ה-28 להריון ומנה נוספת ניתנת עד שלושה ימים מהלידה, במידה שמתברר שסוג הדם של העובר הוא Rh חיובי בשל הנחה שקיים מעבר דם בין העובר האנטיגן לאם בזמן הלידה , כדי למנוע ריגוש של המערכת החיסונית של האם, ולמנוע סיבוכים בהיריון הבא..
אצל נשים שלא קיבלו טיפול של זריקת אנטי-D, נבדק סוג הדם של האב. אם סוג הדם שלו Rh שלילי אז אין צורך בטיפול. במידה וסוג הדם Rh חיובי, יש לבדוק את כייל (טיטר) הנוגדנים של האם בשבוע 24 כדי לבדוק את עוצמת התגובה החיסונית של האם.
אם הטיטר גבוה, אז ישנו סיכון גבוה לתגובה חיסונית קשה של האם כנגד כדוריות הדם האדומות של העובר. במקרה כזה מומלץ לבצע דיקור של חבל הטבור על מנת לבדוק את מידת ההמוליזה של העובר. במידה ויש המוליזה משמעותית - יש לתת עירוי דם דרך חבל הטבור לעובר.
מהשבוע בו מושגת בשלות ריאתית (שבוע 32-34) במקרים של טיטר קריטי, או במצבים בהם יש התדרדרות המודינמית למרות עירויים חוזרים, או במצבים בהם יש מיימת (הידרופס פטאליס) קשה, יש ליילד את העובר.
במידה והטיטר נמוך (קטן מ 1:16), יש להמשיך לבצע מעקב באולטרא- סאונד וביצוע בדיקת טיטר חוזרת לאחר 4 שבועות.
בדיקת סקר נוגדנים[עריכת קוד מקור | עריכה]
מבוצעת במטרה לזהות אם קיים אצל האם נוגדן כנגד אנטיגן עוברי .
נקראת גם קומבס בלתי ישיר (באנגלית Indirect Coombs Test או ABSC-Antibody Screen ) היא בדיקה לזיהוי נוגדנים כנגד אנטיגנים של קבוצות דם נבחרות בנוזל דם הנבדק. תשובה שלילית פירושה שנוגדנים אלו לא קיימים או לא נמצאו , ותשובה חיובית פירושה שנמצא נוגדן אחד או יותר, שלאחריו מבוצעות בדיקות נוספות לזיהוי וטיטר (כייל) הנוגדן.
בדיקה זו מבוצעת לנשים בהריון לחיפוש נוגדנים היכולים לגרום למחלה המוליטית של היילוד (Hemolytic Disease of the Newborn או HDN) או לפני פעולות אשר מצריכות קבלת מנת דם לדוגמת ניתוח.
בבדיקת סקר נוגדנים לנשים בהריון נבדק הסרום של האם להימצאות נוגדנים, בעיקר מסוג IgG, שיכולים לעבור דרך מחסום השלייה, ולהקשר לכדוריות הדם האדומות של העובר ולגרום להידרופס עוברי אימוני או למחלה המוליטית של היילוד (HDN) [3]
תהליך זה מתרחש כאשר על כדוריות הדם של העובר קיימים האנטיגנים אותם ירש מהאב, שאליהם הנוגדנים של האם מכוונים.
לפי הנחיות משרד הבריאות בישראל " יש לבצע בדיקת סקר נוגדנים לכל הדגימות מנשים בהריון לפחות פעם אחת בכל הריון. בבדיקת סקר נוגדנים חיובית יש לבצע בדיקה לאפיון הנוגדנים"
נוגדנים מסוג Anti D, C, c, E, e, Kell, Kidd, Duffy, MN, P מוגדרים כמסוכנים לפי הספרות המקצועית.[4]
בדיקת סקר נוגדנים מבוצעת בנשים אחרי זריקת אנטי D על מנת לספק מידע על הימצאות טיטר הנוגדן בנוזל הדם והצורך בזריקה נוספת אם הטיטר נמוך מדי.
נשים בעלות Rh חיובי נדרשות לבצע בדיקת סקר נוגדנים בהריון, אך אינן מקבלות את זריקת Anti-D ואינן נבדקות לבדיקת טיטר הנוגדן Anti-D.
לעיתים ישנה התייחסות של הצוות הרפואי לבדיקת סקר נוגדנים כאל בדיקת סקר ל-Rh D, אך מדובר על סקר נוגדנים כללי המאפשר גילוי גם של נוגדנים נוספים.
אופן ביצוע הבדיקה[עריכת קוד מקור | עריכה]
דגימת דם נלקחת לנבדק, כאשר על הדגימה חייבים להיות רשומים השם המלא ותעודת הזהות של הנבדק, לפי הנחיות משרד הבריאות.

הדגימה נשלחת לבדיקה במעבדת בנק דם, ובמעבדה נבדק נוזל הדם שבו נמצאים הנוגדנים.
משתמשים ביכולת של הנוגדן להיקשר באופן ספציפי לאנטיגן מסוים (מפתח ומנעול) על מנת לזהות קיום הנוגדן והסוג שלו.
במעבדה משתמשים במספר כדוריות דם בעלות סוגי אנטיגנים שונים (כד"א תעשייתיות) אשר נמצאות במבחנות שונות, ואל המבחנות הללו מטפטפים את נוזל הדם של הנבדק.
מבצעים אינקובציה (בחום של 37 מעלות צלסיוס מכיוון שזוהי טמפרטורת הגוף שבו הנוגדן פעיל בצורה המיטבית) וממתינים לפעולת הנוגדן שיתחבר אל האנטיגן.
במקרה שלא קיים נוגדן אצל הנבדק, לא ייוצר קישור נוגדן-אנטיגן ותשובת סקר הנוגדנים תהיה שלילית.
במקרה שקיים נוגדן, הנוגדן יצור קשר עם האנטיגן של כדורית הדם ויקשור אותה. מצרפים לתהליך גם ריאגנט קומבס על מנת שיעזור בתהליך הקישור.
הקישור של הנוגדנים לאנטיגנים שעל הכדוריות גורם לכדוריות הדם להידבק אחת לשנייה ולא לנוע באופן חופשי נקרא צימות (אגלוטינציה), וניתן לזיהוי בעין או במיקרוסקופ.
האגלוטינציה מתרחשת רק במבחנות שבהן נמצא האנטיגן, ולא מתרחשת במבחנות שבו אינו נמצא, ועל ידי כך מאפשרת זיהוי של הנוגדן.
דוגמא - מתוך 11 מבחנות המכילות סוגי אנטיגנים שונים, רק במבחנות 1 ,2 ,3 ו-8 קיים האנטיגן Rh-D. מצרפים את נוזל הדם של הנבדק לכל המבחנות, אך רק במבחנות 1, 2, 3 ו-8 מתרחשת האגלוטינציה, ולכן הנוגדן מזוהה כנוגדן ספציפי Anti-D.
כאשר ישנה בעיה בזיהוי הנוגדן בסקר נוגדנים רגיל, ניתן להשתמש בשיטות זיהוי מתקדמות כמו סקר נוגדנים עם אנזים, בקור או ביצוע אלוציה.
טיטר הנוגדן[עריכת קוד מקור | עריכה]
אחרי זיהוי הנוגדן, יש לזהות את ריכוז הנוגדן בסרום הנבדק, על מנת להבין את עוצמת התגובה החיסונית.
מתבצע תהליך טיטרציה שבו מדללים את הסרום פי 2 עם נוזל סליין עד לדילול מרבי שבו ניתן לזהות צימות של כד"א. הדילול מתחיל ביחס של 1:1 (בין כד"א לסרום), 1:2,1:4,1:8,1:16 והלאה.
לרוב מתייחסים ליחס 1:16 כאל ערך סף שמעליו מוגדר טיטר גבוה.
ריאגנט הקומבס[עריכת קוד מקור | עריכה]
ריאגנט הקומבס (הנקרא גם Coombs antiglobulin או Anti Human Globulinאו AHG ) הינו חומר המכיל נוגדנים המכוונים כנגד נוגדנים אנושיים/הומניים.
ריאגנט הקומבס נוצר ע"י הזרקה שם חלבון אנושי לבעלי חיים, אשר כתגובה מהחשיפה מייצרים נוגדנים ספציפיים כנגד אימונוגלובולינים אנושיים (Anti-IgG) וכנגד פקטורים ממערכת המשלים (Anti-C3d).[5]
נוגדני הקומבס נקשרים לרגל של נוגדן הומני (אזור ה-Fc) ויכולים ליצור גשר בין 2 כדוריות דם אדומות. בשל הבדלי הגודל בין כדורית הדם האדומה לנוגדן שנקשר לאנטיגן שעליה, לנוגדן כמעט בלתי אפשרי לקשור בזרוע השנייה כדורית דם אחרת כדי ליצור צימות (אגלוטנציה). ריאגנט הקומבס יוצר קשר בין 2 נוגדנים שונים, אשר כל אחד מהם קושר כדורית דם אדומה אחרת, ובכך יוצר את הגשר ואת הצימות.
קריאה נוספת[עריכת קוד מקור | עריכה]
Transfusion by AABB (American Association of, AABB, & A.A.B.B, 1961)
קישורים חיצוניים[עריכת קוד מקור | עריכה]
נוהל בדיקת ABO Rh וסקר נוגדנים בנשים בהריון מהקהילה
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ Sebring, E., & Polesky, H, (1990). Fetomaternal hemorrhage: Incidence, risk factors, time of occurrence, and clinical effects., Transfusion, 30(4), 344-357
- ^ Finn, R., Clarke, C. A., Donohoe, W. T. A., McConnell, R. B., Sheppard, P. M., Lehane, D., & Kulke, W., (1961). Experimental studies on the prevention of rh haemolytic disease. Rhesus haemolytic disease, (pp. 153-158) Springer.
- ^ BOWMAN, J. M, (1996). Hemolytic disease of the newborn, Vox Sanguinis, 70(S3), 62-67
- ^ Howard, H., Martlew, V., McFadyen, I., Clarke, C., Duguid, J., Bromilow, I., & Eggington, J, (1998). Consequences for fetus and neonate of maternal red cell allo-immunisation., Archives of Disease in Childhood.Fetal and Neonatal Edition, 78(1), F62-6
- ^ Wiener, A. S, . (1944). A new test (blocking test) for rh sensitization. Rhesus haemolytic disease, (pp. 81-85) Springer
