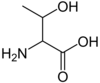
תראונין
| שם באנגלית | Threonine | ||
|---|---|---|---|
| סימון ארוך | Thr | ||
| סימון קצר | T | ||
| נוסחה כימית | C4H9NO3 | ||
| משקל מולקולרי | 119 גרם למול | ||
| נקודה איזואלקטרית | 5.87 | ||
| pKa קרבוקסיל | 2.1 | ||
| pKa אמין | 9.62 | ||
| pKa שייר | אין | ||
| |||
| מספר CAS |
72-19-5 | ||
תראונין (Threonine) היא אחת מ-20 חומצות האמינו הנפוצות בטבע. מבוגרים זקוקים לכעשרים מ"ג תראונין ביום לכל ק"ג ממשקל גופם[1], אולם תאי גוף האדם אינם מסוגלים לסנתז תראונין ולכן היא מהווה חומצת אמינו חיונית, אותה יש לקבל דרך המזון.
כימיה
[עריכת קוד מקור | עריכה]השייר של תראונין מורכב מאטום פחמן הקשור לאטום מימן, לקבוצת מתיל (CH3) ולקבוצת הידרוקסיל (OH). שייר זה זהה כמעט לשייר של חומצת אמינו אחרת: ולין, כשהשניים נבדלים זה מזה בכך שקבוצת ההידרוקסיל מוחלפת בוולין בקבוצת מתיל נוספת. קבוצת ההידרוקסיל היא קוטבית ומסוגלת ליצור קשרי מימן עם מולקולות מים. תראונין היא לפיכך הידרופילית, זאת לעומת ולין ההידרופובית.
מקורות תזונה
[עריכת קוד מקור | עריכה]תראונין, כמו כל חומצת אמינו חיונית, קיימת כמעט בכל מזון[2], וכמו כל חומצת אמינו חיונית, המקורות המשמעותיים ביותר שלה הם מזונות עשירים בחלבון, כגון בשר בקר, דגים ועוף, חלב, ביצים, קטניות (כגון פולי תורמוס, פולי סויה, עדשה תרבותית, שעועית, חומוס, פול ואפונה) וגרעינים מסוימים.
ביולוגיה
[עריכת קוד מקור | עריכה]פגמים במנגנונים לעיבוד תראונין קושרו למחלות עצבים כאלצהיימר[3][4]ופרקינסון[5].
קישורים חיצוניים
[עריכת קוד מקור | עריכה]- תראונין, באתר אנציקלופדיה בריטניקה (באנגלית)
הערות שוליים
[עריכת קוד מקור | עריכה]- ^ Panel on Macronutrients, Panel on the Definition of Dietary Fiber, Subcommittee on Upper Reference Levels of Nutrients, Subcommittee on Interpretation and Uses of Dietary Reference Intakes, Dietary Reference Intakes for Energy, Carbohydrate, Fiber, Fat, Fatty Acids, Cholesterol, Protein, and Amino Acids, Washington, D.C.: National Academies Press, 2005-10-28
- ^ תכולת התראונין במזונות על פי משרד החקלאות האמריקאי
- ^ Erez Podoly, Geula Hanin, Hermona Soreq, Alanine-to-threonine substitutions and amyloid diseases: butyrylcholinesterase as a case study, Chemico-Biological Interactions 187, 2010-09-06, עמ' 64–71 doi: 10.1016/j.cbi.2010.01.003
- ^ Qing Tian, Jianzhi Wang, Role of serine/threonine protein phosphatase in Alzheimer's disease, Neuro-Signals 11, 2002-09, עמ' 262–269 doi: 10.1159/000067425
- ^ Mahaboobi Jaleel, R. Jeremy Nichols, Maria Deak, David G. Campbell, Frank Gillardon, Axel Knebel, Dario R. Alessi, LRRK2 phosphorylates moesin at threonine-558: characterization of how Parkinson's disease mutants affect kinase activity, The Biochemical Journal 405, 2007-07-15, עמ' 307–317 doi: 10.1042/BJ20070209
| עשרים חומצות האמינו הסטנדרטיות הנפוצות בטבע | ||
|---|---|---|
|