Haemophilus influenzae

| |
| מיון מדעי | |
| ממלכה: | חיידקים אמיתיים |
| מערכה: | פרוטאובקטריה |
| מחלקה: | Gamma Proteobacteria |
| סדרה: | pasteurellales |
| משפחה: | Pasteurallaceae |
| סוג: | Haemophilus |
| מין: | H. influenzae |
| שם מדעי | |
Haemophilus influenzae (בקיצור: H. influenzae, בתעתיק לעברית: המופילוס אינפלואנזה. נקרא בעבר Pfeiffer's bacillus, וגם Bacillus influenzae) הוא מין של חיידק גראם-שלילי, בעל צורה נקדית-מתגית (Coccobacillus), קפנופילי, אל-אווירני פקולטטיבי, ששייך למשפחת Pasteurellaceae[1]. H. influenzae תואר לראשונה בשנת 1892 על ידי ריצ'רד פייפר במהלך מגפת שפעת[2]. עד לשנת 1933, טרם גילוי נגיפי השפעת, נחשב החיידק בטעות כמחולל מחלת השפעת. H. influenzae אחראי על מגוון רחב של זיהומים אופורטוניסטיים מקומיים ופולשניים. מין זה היה האורגניזם החי הראשון שכל הרצף הגנומי שלו פוענח [3].
סרוטיפים[עריכת קוד מקור | עריכה]
בשנת 1930 הוגדרו שתי קבוצות עיקריות של H. influenzae: זנים שהם ללא קפסולה (unencapsulated) וזנים שהם בעלי קפסולה (encapsulated). זנים בעלי קפסולה סווגו על בסיס האנטיגנים הקפסולריים הנבדלים שלהם. ששת סוגי הזנים של H. influenzae הם: a, b, c, d, e ו-f [4]. השונות הגנטית בין זנים חסרי קפסולה גדולה יותר מזו שבקבוצה בעלת הקפסולה. זנים חסרי קפסולה נחשבים כלא ניתנים לאפיון (נקראים nontypable-NTHi) בשל העדר סרוטיפים קפסולריים; עם זאת, ניתן לסווגם על פי רצף הבסיסים הנוקלאוטידים. הפתוגנזה של זיהומים על רקע H. influenzae אינה ברורה במלואה, אם כי נוכחות של הקפסולה בסוג B (Hib), סרוטיפ הגורם למצבים כגון דלקת מכסה הגרון, ידועה כגורם מרכזי לאלימות החיידק. הקפסולה שלהם מקנה להם עמידות כנגד פגוציטוזיה וליזיס בתיווך מערכת המשלים של המאכסן הבלתי מחוסן. זנים חסרי קפסולה הם כמעט תמיד פחות פולשניים; עם זאת, הם עלולים, לייצר תגובה דלקתית בבני אדם, אשר עלולה להוביל לתסמינים רבים. חיסון עם תרכיב נגד Hib יעיל במניעת זיהום Hib, אך לא מונע זיהום עם זני NTHi [5].
מחלות[עריכת קוד מקור | עריכה]
רוב הזנים של H. influenzae הם פתוגנים אופורטוניסטים; כלומר, הם בדרך כלל חיים בפונדקאי שלהם מבלי לגרום בהם למחלה, אך גורמים לבעיות בשילוב עם גורמים אחרים (כגון מזיהום ויראלי, מירידה בתפקוד המערכת החיסונית או ברקמות דלקתיות כרוניות, למשל מאלרגיות) ליצירת הזדמנות. הם מדביקים את הפונדקאי על ידי כך שהם נדבקים לתא הפונדקאי באמצעות חלבוני הדבקות חוץ ממברנליים (trimeric autotransporter adhesins).
מחלה נרכשת באופן טבעי, שנגרמה על ידי H. influenzae, מתרחשת כנראה בבני אדם בלבד. אצל תינוקות וילדים קטנים הזן Hib עלול לגרום לבקטרמיה, דלקת ריאות, דלקת מכסה הגרון, ודלקת קרום המוח חיידקית חריפה. לפעמים, נגרמים גם צלוליטיס, דלקת העצם, וכן דלקת מפרקים זיהומית. זוהי גם אחת מהסיבות לזיהום ולדי[6].
בשל השימוש השגרתי בחיסון תרכיב Hib בארצות הברית מאז 1990, שכיחות מחלת Hib הפולשנית ירדה ל-1.3 לכל 100,000 ילדים. ברם, Hib נשאר כגורם העיקרי לדלקות בדרכי הנשימה התחתונות אצל תינוקות וילדים במדינות מתפתחות, שבהן החיסון אינו מצוי בשימוש נרחב. זנים לא קפסולרים של H. influenzae אינם מושפעים על ידי תרכיב Hib, וגורמים לדלקות אוזניים (דלקת האוזן התיכונה), דלקות עיניים (דלקת הלחמית) וסינוסיטיס אצל ילדים, וכן לדלקת ריאות במבוגרים.
אבחון[עריכת קוד מקור | עריכה]

תכונות קליניות עשויות לכלול סימפטומים ראשוניים של דלקת בדרכי הנשימה העליונות המחקות זיהום וירלי, כרוכה לעיתים בחום, בדרך כלל ברמה נמוכה. הדבר עלול להתקדם תוך כמה ימים לדרכי הנשימה התחתונות, עם סממנים הדומים לעיתים קרובות לאלה של ברונכיטיס חרחורי. הכיח עשוי להיות צמיגי ולעיתים קרובות בעל צבע אפור או קרם. השיעול עלול להימשך שבועות ללא הטיפול ההולם. מקרים רבים מאובחנים רק לאחר הדגמת זיהומים שאינם מגיבים לפניצילין בחזה או לדור הראשון של צפלוספורינים. בצילום רנטגן חזה או בטומוגרפיה ממוחשבת של הראות (CT) ניתן לזהות קונסולידציה אלוואולרית[7].
אבחון קליני של H. influenzae מבוצע בדרך כלל על ידי תרבית חיידקים או על ידי מבחן אגלוטינצית לטקס חלקיקית. האבחנה נחשבת כמאושרת כאשר החיידק מבודד מאתר סטרילי בגוף. במובן זה, H. influenzae שתורבת מחלל הלוע והאף (nasopharyngeal), או מהכיח, לא יהווה אישור חד-משמעי למחלה של H. influenzae, כיוון שבאתרים אלו ניתן למצוא את החיידק באנשים ללא מחלה[8]. עם זאת, H. influenzae המבודד מנוזל שדרה-מוח, או מדם יהווה אינדיקציה לזיהום ודאי.
תרבית[עריכת קוד מקור | עריכה]
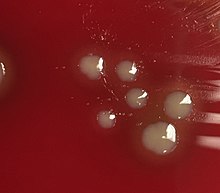
תרבית חיידקים של H. influenzae מתבצעת על צלחות אגר, בעדיפות לאגר שוקולד, תוך הוספת הגורמים X (המין) ו- V (ניקוטינאמיד אדנין דינוקלוטיד - NAD) והדגרה ב-37 מעלות צלזיוס באינקובטור בסביבה מועשרת ב-CO2 [9]. צמיחת אגר הדם מושגת רק כתופעת לוואי סביב חיידקים אחרים. מושבות של H. influenzae מופיעות כמושבות קמורות, חלקות, חיוורות, אפורות או שקופות.
בחינה מיקרוסקופית של תבחינים בצביעת גראם של H. influenzae תדגים קוקובצילים גראם-שליליים. ניתן לאפיין יותר את האורגניזם המתורבת באמצעות בדיקות קטלאז ואוקסידאז, ששניהם אמורים להיות חיוביים. יש צורך בבדיקה סרולוגית נוספת כדי להבחין בפוליסכריד הקפסולרי ולהבחין בין H. influenzae למינים שאינם קפסולריים.
על אף רגישותה של תרבית החיידקים לבידוד החיידק, שימוש באנטיביוטיקה לפני איסוף הדגימה מפחית במידה נכרת את שיעור בידודי H. influenzae[10]. מעבר לכך, H. influenzae הוא חיידק הדורש תשומת לב מרובה לגידולו בתרבית, וכל שינוי של נוהלי התרבית עלל להפחית מאוד את שיעורי הבידוד. הרמה הנמוכה של מעבדות רפואיות במדינות מתפתחות גרמה לשיעור בידודו הנמוך.
H. influenzae יכול לצמוח בסביבה ההמוליטית של Staphylococcus aureus על צלחות אגר דם; המוליזה של כדוריות דם אדומות באגר דם על ידי Staphylococcus aureus משחררת פקטור V החיוני לצמיחתו של H. influenzae. לכן H. influenzae לא יצמח מחוץ לאזור ההמוליטי של S. aureus, בשל היעדר בחומרים מזינים כמו פקטור V באזורים אלה. אגר פילדס מועדף לצורכי בידוד. במדיום לוינטל, זנים קפסולויים מדגימים נצנוץ ססגוני מובהק (Iridescence).
אגלוטינצייה חלקיקית בלטקס[עריכת קוד מקור | עריכה]
מבחן אגלוטינציה חלקיקית בלטקס (agglutination particle latex -LAT) היא שיטה רגישה יותר לגילוי H. influenzae מאשר בתרבית[11]. מכיוון שהשיטה מסתמכת על מציאותו של אנטיגן ולא על חיידקים ברי קיימא, התוצאות אינן מופרעות בגין שימוש קודם באנטיביוטיקה. יש לה גם את היתרון הנוסף של שיטה מהירה בהרבה משיטות תרבית. עם זאת, בדיקת רגישות לאנטיביוטיקה אינה אפשרית בשיטת LAT בלבד, ולכן יש צורך להשתמש במקביל בשיטת התרבית.
שיטות מולקולריות[עריכת קוד מקור | עריכה]
סוג אבחון נוסף הוא אבחון מולקולרי באמצעות PCR, שהוא רגיש יותר מאשר מבחני הלטקס או תרבית חיידקים. שיטות PCR הוכחו כרגישות יותר מבדיקות LAT או תרבית, והן ספציפיות ביותר[12]. עם זאת, מבחני PCR טרם הפכו לשגרה במסגרות קליניות.
ריצוף[עריכת קוד מקור | עריכה]
H. influenzae היה האורגניזם הראשון שכל הגנום שלו רוצף. הפרויקט הושלם על ידי קרייג ונטר (Craig Venter and his team) וצוותו ב"מכון לחקר הגנום" ( The Institute for Genomic Research). חיידק זה נבחר מכיוון שאחד ממובילי הפרויקט, חתן פרס נובל המילטון סמית', עבד על כך במשך עשרות שנים והצליח לספק ספריות DNA איכותיות. הגנום מורכב מ־1,830,140 זוגות בסיסים של DNA בכרומוזום מעגלי יחיד המכיל 1740 גנים המקודדי חלבון, 2 גנים של tRNA ו- 18 גנים נוספים של RNA. שיטת הרצוף ששימשה הייתה של ריצוף גנום שלם "בשיטת רובה הציד", שהושלם ופורסם בעיתון המדעי Science בשנת 1995[13].
אינטראקציה עם החיידק Streptococcus pneumoniae[עריכת קוד מקור | עריכה]
הן את H. influenzae והן את S. pneumoniae ניתן למצוא בדרכי הנשימה העליונות של בני האדם. במחקר שנערך התברר ש-S. pneumoniae תמיד התגבר על השפעתו של H. influenzae על ידי התקיפה שלו בהידרוגן פרארוקסיד, תוך הסרת מולקולות השטח החיוניות להישרדורתו של H. influenzae[14].
כאשר שני החיידקים ממוקמים יחד בתוך חלל האף, תוך שבועיים, רק H. influenzae שורד. כאשר כל אחד מהם ממוקם בנפרד בחלל האף, כל אחד מהם שורד. כאשר בדקו את רקמת דרכי הנשימה העליונות בעכברים שנחשפו בו זמנית לשני מיני החיידקים, נמצא מספר גדול במיוחד של נויטרופילים (תאי חיסון). בעכברים שנחשפו רק לאחד המינים, לא נצפתה נוכחות של תאים נויטרופילים.
בבדיקות המעבדה נמצא כי נויטרופילים שנחשפו לחיידקי H. influenzae מתים, היו תוקפניים יותר בתקיפת S. pneumoniae מאשר נויטרופילים שלא נחשפו. לחשיפה לחיידקי H. influenzae מתים לא הייתה כל השפעה על חיידקי H. influenzae חיים.
שני תרחישים עשויים להיות אחראים לתגובה זו:
- כאשר חיידקי H. influenzae מותקפים על ידי חיידקי S. pneumoniae קיים איתות למערכת החיסון לתקוף את S. pneumoniae.
- השילוב של שני המינים מעורר תגובה של מערכת החיסון שאינה מתרחשת על ידי אף אחד מהמינים בנפרד.
לא ברור מדוע H. influenzae אינו מושפע על התגובה החיסונית[15].
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- Haemophilus influenzae, באתר ITIS (באנגלית)
- Haemophilus influenzae, באתר NCBI (באנגלית)
- Haemophilus influenzae, באתר האנציקלופדיה של החיים (באנגלית)
- Haemophilus influenzae, באתר GBIF (באנגלית)
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ Kuhnert, P; Christensen, H, eds. (2008). Pasteurellaceae Biology, Genomics and Molecular Aspects. Caister Academic Press. ISBN 978-1-904455-34-9.
- ^ About the J. Craig Venter Institute, J. Craig Venter Institute website, retrieved November 21, 2015
- ^ J. Craig Venter, About the J. Craig Venter Institute, J. Craig Venter Institute website, retrieved, https://www.jcvi.org/about, November 21, 2015
- ^ Ryan, KJ; Ray, CG, eds. (2004). Sherris Medical Microbiology (4th ed.). McGraw Hill. pp. 396–401. ISBN 978-0-8385-8529-0.
- ^ Slack, MP; et al. (1998). "Enhanced surveillance of invasive Haemophilus influenzae disease in England, 1990 to 1996: impact of conjugate vaccines". Pediatr Infect Dis J. 17 (9 suppl): S204–7. doi:10.1097/00006454-199809001-00026. PMID 9781764.
- ^ Baucells, B.J.; Mercadal Hally, M.; Álvarez Sánchez, A.T.; Figueras Aloy, J. (2015). "Asociaciones de probióticos para la prevención de la enterocolitis necrosante y la reducción de la sepsis tardía y la mortalidad neonatal en recién nacidos pretérmino de menos de 1.500g: una revisión sistemática". Anales de Pediatría. 85 (5): 247–255.
- ^ WHO, Measuring impact of Streptococcus pneumoniae and Haemophilus influenzae type b conjugate vaccination, Immunization, Vaccines and Biologicals
- ^ Puri J; Talwar V; Juneja M; Agarwal KN; et al. (1999). "Prevalence of antimicrobial resistance among respiratory isolates of Haemophilus influenzae". Indian Pediatr. 36 (10): 1029–32. PMID
- ^ Levine OS; Schuchat A; Schwartz B; Wenger JD; Elliott J; Centers for Disease Control (1997). "Generic protocol for population-based surveillance of Haemophilus influenzaetype B" (PDF). World Health Organization. WHO/VRD/GEN/95.05.
- ^ John TJ; Cherian T; Steinhoff MC; Simoes EA; et al. (1991). "Etiology of acute respiratory infections in children in tropical southern India". Rev Infect Dis. 13: Suppl 6:S463–9. doi:10.1093/clinids/13.supplement_6.s463. PMID 1862277.
- ^ Kennedy WA, Chang SJ, Purdy K, LE T, et al. (2007). "Incidence of bacterial meningitis in Asia using enhanced CSF testing: polymerase chain reaction, latex agglutination and culture". Epidemiol Infect. 135 (7): 1217–26. doi:10.1017/S0950268806007734. PMC 2870670. PMID 17274856
- ^ Kennedy WA, Chang SJ, Purdy K, LE T, et al. (2007). "Incidence of bacterial meningitis in Asia using enhanced CSF testing: polymerase chain reaction, latex agglutination and culture". Epidemiol Infect. 135 (7): 1217–26. doi:10.1017/S0950268806007734. PMC 2870670. PMID 17274856.
- ^ Fleischmann R; Adams M; White O; Clayton R; et al. (1995). "Whole-genome random sequencing and assembly of Haemophilus influenzae Rd". Science. 269 (5223): 496–512. Bibcode:1995Sci...269..496F. doi:10.1126/science.7542800. PMID 7542800.
- ^ Pericone, Christopher D.; Overweg, Karin; Hermans, Peter W. M.; Weiser, Jeffrey N. (2000). "Inhibitory and Bactericidal Effects of Hydrogen Peroxide Production by Streptococcus pneumoniae on Other Inhabitants of the Upper Respiratory Tract". Infect Immun. 68 (7): 3990–3997. doi:10.1128/IAI.68.7.3990-3997.2000. PMC 101678. PMID 10858213.
- ^ Lysenko E; Ratner A; Nelson A; Weiser J (2005). "The role of innate immune responses in the outcome of interspecies competition for colonization of mucosal surfaces". PLoS Pathog. 1 (1): e1. doi:10.1371/journal.ppat.0010001. PMC 1238736. PMID 16201010.
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.
