מערכת מצומדת
בכימיה, מערכת מצומדת היא מערכת אטומים הקשורים קוולנטית אחד לשני בקשרים כפולים וקשרים יחידים, לסירוגין (לדוגמה: C=C-C=C-C), במולקולה של תרכובת אורגנית. במערכת זו קיים אל-איתור של האלקטרונים לאורך אורביטלי p של האטומים, המקבילים זה לזה. תופעת האל-איתור משפרת את יציבות המולקולה, כלומר מפחיתה את האנרגיה הכוללת שלה.
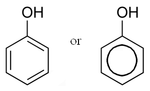
תופעת האל-איתור יוצרת תחום בו האלקטרונים אינם מוגבלים לקשר או אטום בודד, אלא לקבוצת קשרים או אטומים. דוגמה לכך היא החומר פנול (C6H5OH בנזן עם קבוצת הידרוקסיל), לו מערכת של 6 אלקטרונים מעל ומתחת לטבעת המישורית, וכמו כן סביב קבוצת ההידרוקסיל. בשרטוט, המולקולה מסומנת כבעלת קשרים כפולים ויחידים לסירוגין, אך במציאות אין הבחנה בין הקשרים, והאלקטרונים משתתפים בכולם באופן דומה. זוהי דוגמה לחומר ארומטי.

צימוד יכול להתרחש גם במקרים נוספים, מעבר למקרה הקלאסי של קשרים יחידים וכפולים לסירוגין. כל עוד לכל אטום בשרשרת אורביטל p, השרשרת יכולה להיות מצומדת. לדוגמה, פוראן (בשרטוט משמאל) הוא טבעת מחומשת, בעלת שני קשרים כפולים, ואטום חמצן בעמדה 1. לחמצן שני זוגות אלקטרונים בלתי קושרים; אחד מהזוגות תופס אורביטל p בכיוון המתאים לשאר המערכת, ובכך שומר על הצימוד. נוכחות חנקן בטבעת או קבוצות בעמדת α לטבעת, כמו קרבוניל (C=O), אימין (C=N), ויניל (C=C) או אניון יכולים לשמש מקור לאורביטלי p, ליצירת מערכת מצומדת.
למערכות מצומדות תכונות מיוחדות, הנותנות לתרכובות צבעים חזקים. בפיגמנטים רבים מערכות מצומדות, כמו השרשרת הפחמימנית המצומדת של בטא-קרוטן, היוצרת צבע כתום חזק. כאשר אלקטרון בשרשרת בולע פוטון של אור באורך הגל המתאים, הוא מעורר לרמה אנרגטית גבוהה יותר (ראו מודל חלקיק בקופסה). ככל שאורך המערכת גדל, כך ההפרשים בין רמות האנרגיה קטנים, והחומר יבלע פוטונים באורכי גל ארוכים יותר (תדירויות נמוכות יותר). רוב המעברים האלקטרונים הם מאורביטל פאי קושר לאורביטל פאי אנטי-קושר (π ל- *π), אך גם אלקטרונים לא-קושרים יכולים לבצע מעבר (n ל- *π). מערכות מצומדות בעלות פחות משמונה קשרים כפולים מצומדים בולעים קרינה רק בטווח העל-סגול, ואין להם צבע נראה.
ניתן לכמת את בליעת האור בטווח העל-סגול והאור הנראה בעזרת ספקטרוסקופית UV/VIS. בליעת האור מהווה את הבסיס לתחום הפוטוכימיה.

מערכות מצומדות מהוות את הבסיס לכרומופורים, שהם החלקים בולעי האור של מולקולה, וגורמים לה להיות צבעונית. ניתן למצוא כרומופורים בתרכובות אורגניות שונות, ולעיתים גם בפולימרים צבעוניים או זוהרים בחושך. הכרומופורים הם בדרך כלל מערכת מצומדות טבעתיות עם קשרים כמו C=O או N=N בנוסף לקשרי C-C המצומדים.
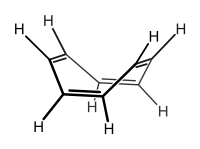
קיום קשרים כפולים ויחידם לסירוגין אינו תנאי מספיק לצימוד חזק במערכת. קיימים פחמימנים טבעתיים, כמו ציקלואוקטטטראן, המקיימים תנאי זה, אך הצימוד בהם חלש. הסיבה לכך היא הקונפורמציה של המולקולה, בצורת "סירה", ולא בצורה מישורית. כיוון שאורביטלי p של המולקולה אינם מקבילים, קשה לאלקטרונים לעבור ביניהם, ולכן הצימוד ביניהם חלש. עדיין ניתן לומר שזוהי מערכת מצומדת, אך היא אינה ארומטית.
דוגמאות לחומרים מצומדים[עריכת קוד מקור | עריכה]
ראו גם[עריכת קוד מקור | עריכה]
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- מערכת מצומדת, באתר אנציקלופדיה בריטניקה (באנגלית)
