סיליקט
בכימיה, סיליקט הוא תרכובת הכוללת אניון שבמרכזו אטום צורן אחד או יותר המוקף בליגנדים שמטענם החשמלי שלילי. הגדרה זו רחבה מספיק על מנת לכלול סוגי תרכובות כמו הקסאפלואורסיליקט ("פלוּאוֹסיליקט"), -2[SiF6], אך בסוגי הסיליקטים הנפוצים ביותר חמצן משמש כליגנד. המטען החשמלי של אניוני הסיליקט הוא שלילי ולכן חייב לבוא פיצוי בעזרת קטיונים אחרים על מנת ליצור תרכובת נטולת מטען חשמל.
לעיתים מתייחסים לסיליקה (צורן דו-חמצני), SiO2, כאל סיליקט אף על פי שתרכובת זו היא מקרה מיוחד שכן היא נטולת מטען חשמלי שלילי ולכן אינה זקוקה לפיצוי של יונים בעלי מטען חשמלי חיובי. בטבע ניתן למצוא סיליקה כמינרל קוורץ והפולימורפים שלו.
ברוב המכריע של הסיליקטים, כולל המינרלים הסיליקטיים, המבנה הבסיסי הוא של טטרהדרון (ארבעון – פירמידה בעלת 4 מישורים שווי צלעות). הצורן מצוי במרכז הטטרהדרון והחמצנים מהווים את ארבעת הקדקודים. סוג הקשרים בין הטטרהדרונים משתנה בין סוגי המינרלים. הטטרהדרונים יכולים להיות מנותקים זה ממזה, מחוברים בזוגות או מקובצים למבנים הכוללים טבעות משולשות או משושות, שרשרות, שרשרות כפולות, לוחות, ומבנים תלת־ממדיים. המינרלים הסיליקטים מסווגים לקבוצות בהתאם למבנים אלו. רשימת הסוגים מפורטת בהמשך.
תחת לחץ גבוה יכול הצורן ליצור מבנה של אוקטהדרון (תמניון) שקודקודיו הם שישה אטומי חמצן, כמו בסטישהוביט, פולימורף של סיליקה המצוי בחלקה התחתון של מעטפת כדור הארץ, והנוצר גם תחת גל הלם עקב התנגשות של מטאוריט. מכיוון שהיחס בין נפח אטום הצורן לנפח אטום החמצן הוא 1/3 (מספר הקוארדינציה של הצורן הוא 4) הרי שחוסר המקום סביב אטומי החמצן גורם שמבנה זה הוא נדיר בלחץ אטמוספירי רגיל, אך הוא מוכר באניון ההקסאהידרוקסיליקט, -2[Si(OH)6], כבמינרל תאומאסיט.
מקור השם[עריכת קוד מקור | עריכה]
סיליקט הוא כינוי שניתן בתחילת המאה ה-19 למלח של חומצה צורנית. בכימיה מקובל לכנות מלח של חומצה של יסוד כימי מסוים בתחילית שם היסוד בתוספת הסיומת "אט". כך למשל מלח של חומצה זרחתית (פוספור בלעז) מכונה פוספט (בעברית זרחה), מלח של חומצה חנקתית מכונה ניטרט (חנקה). היסוד צורן מכונה בלעז סיליקון (מילה שמקורה בלטינית, Silex הוא אבן צור). ומכאן המלח הנוצר מהחומצה שלו הוא סיליקט.
מבנה סיליקטים[עריכת קוד מקור | עריכה]
יחידת המבנה של המינרלים הסיליקטים כל אטום צורן מחובר לארבעה אטומי חמצן כך שהוא נמצא במרכז טטראדר לאטום הצורן יש דרגת חמצון 4+ ודרגת החמצון של חמצן הוא 2-, על כן סך דרגת החמצון של יחידת המבנה של הסיליקטים הוא 2-. מבנה בו הטטראדרים נפרדים (כל אטום חמצן נמצא בטטראדר סיליקטי אחד בלבד) נקרא nesosilicate והוא קיים באוליבין.


הטטראדר יכול לקשור פינה- כלומר אטום חמצן אחד משותף לשני טטראדרים, קישור זה נמצא במבנים רבים.
בדידים: מולקולות sorosilicate[עריכת קוד מקור | עריכה]
Si2O7-6

טבעות נפרדות (cyclosilicate)[עריכת קוד מקור | עריכה]
ניתן לראות כי כל טטראדר קשור בפינות כדי ליצור טבעות. מבנה של טבעות נפרדות. Si6O18-12
רשת אחת אינסופית[עריכת קוד מקור | עריכה]
ניתן לראות שלכל טטרהדר a קשורים שניים נוספים בפינות כדי ליצור רשתות בודדות inosilicate

SiO3-2
שרשראות כפולות אינסופיות (להקות)[עריכת קוד מקור | עריכה]
Si4O11-6 ניתן לראות שכל טטראדר קשור בפינות כדי ליצור שרשראות כפולות. מבנה בעל מקבילים הנראים כרשתות כפולות של טטראדר סיליקט, inosilicate.
גיליונות אין סופיים[עריכת קוד מקור | עריכה]
Si2O5-2 ניתן לראות שכל טטראדר קשור בשלוש פינות כדי ליצור דף. מבנה בעל גיליונות מקבילים של טטראדר סיליקט, נקרא phyllosilicate

מבנה מסגרת צורני[עריכת קוד מקור | עריכה]
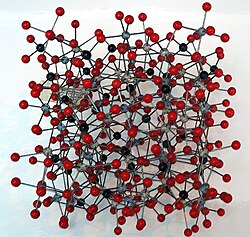
ניתן לראות כי כל טטראדר קשור בכל פינה כדי ליצור מסגרת. בגלל מבנה בעל מסגרת תלת־ממדית של סיליקט טטראדר, מבנה הקוורץ הוא מסגרת תלת־ממדית.
קטיונים[עריכת קוד מקור | עריכה]
קטיונים הם מתכות בעלות מטען חשמלי חיובי, בסיליקטים משתמשים במתכות מהטור הראשון והשני בטבלה המחזורית, כמו +Na,
+K,
+Ca,
+Mg
דרוש מספר שונה של מטענים חיוביים (קטיונים) על מנת לאזן את המטען של הסיליקט.
לדוגמה, ל- SiO4-4 דרושים שני יוני מגנזיום, Mg+2 והנוסחה היא MgSiO4/
דוגמה נוספת, SiO3-2 דרוש יון מגנזיום אחד- Mg+2, והנוסחא היא MgSiO3
סלע סיליקטי[עריכת קוד מקור | עריכה]
בגאולוגיה ובאסטרונומיה המונח "סיליקטי" מציין סוגים של סלעים הבנויים בעיקר ממינרלים סיליקטיים. סלעים אלו כוללים מגוון סוגים נרחב של סלעי יסוד, סלעים מותמרים וסלעי משקע. רוב מעטפת כדור הארץ וקרום כדור הארץ בנויים מסלעים סיליקטיים. דבר זה נכון גם לגבי כוכבי הלכת הארציים (כוכב חמה, נגה, כדור הארץ ומאדים).
על פני כדור הארץ יש מגוון נרחב של מינרלים סילקטיים בצרופים רבים עוד יותר כתוצאה מתהליכים המעצבים והבונים מחדש את קרום כדור הארץ. תהליכים אלו כוללים התכה חלקית, התגבשות, המסה, התמרה, בליה ודיאגנזה (כלל התהליכים החלים בסלעי משקע אחרי שלב ההשקעה, לפני במהלך ואחרי ההתקשות). אורגניזמים חיים תורמים אף הם ליצירת סיליקטים על פני השטח של כדור הארץ. סוג של פלנקטון המכונה צורניות וחד-תאיים המכונים קרנוניות, החיים בעיקר באזורים עמוקים וקרים של הים, בונים שלד צורני מסיליקה שהם סופחים ממי הים. השלדים הצורניים של צורניות הם מרכיב עיקרי בדיאטומיט, משקע שעל הקרקעית העמוקה של האוקיינוסים.
גשם סיליקטי[עריכת קוד מקור | עריכה]
בעזרת טלסקופ וב גילו כי בכוכב הלכת Wasp-107b מקבוצת הכוכבים בתולה עולים אדי סיליקט בטמפרטורה של כ-1000 מעלות צלזיוס. האדים מתקררים ויוצרים גרגרי חול מיקרוסקופיים. ענני החול נעשים דחוסים ומורידים גשם של חול. כשטיפות הסיליקט מגיעות לאזור נמוך וחם באטמוספירה של הכוכב, הם מתאדים שוב. חלקיקי החול שבעננים מסתובבים במהירות של קילומטרים אחדים בשנייה[1].
מינרלוגיה[עריכת קוד מקור | עריכה]
המינרלים הסיליקטיים הם הקבוצה החשובה ביותר בין המינרלים יוצרי הסלעים, כ-95% מקרום כדור הארץ בנוי ממינרלים סיליקטיים. במינרלוגיה מסווגים את המינרלים הסיליקטיים בהתאם למבנה אניון הסיליקט לקבוצות הבאות.
- נזוסיליקטים (נזו ביוונית אי – סיליקטים במבנה איים, טטרהדרון בודד) - -4[SiO4], כמו האוליבין.
- סורוסיליקטים (סורו ביוונית ערימה - טטרהדרונים כפולים) - -6[Si2O7], כמו האפידוט.
- ציקלוסיליקטים (ציקלו ביוונית טבעת - טסיליקטים במבנה טבעת) - -2n[SinO3n], כמו קבוצת הטורמלין.
- אינוסיליקטים (אינו ביוונית שריר - שרשרת פשוטה) - -2n[SinO3n], לדוגמת קבוצת הפירוקסן.
- אינוסיליקטים (שרשרת כפולה) - -6n[Si4nO11n], כמו קבוצת האמפיבול.
- פילוסיליקטים (פילו ביוונית עלה - סיליקטים במבנה לוחות) - -2n[Si2nO5n], כמו הנציצים ומינרלי חרסית.
- טקטוסיליקטים (טקטו ביוונית בנאי - סיליקטים בעלי מבנה מרחבי) - [AlxSiyO2(x+y)]x-, כמו הקוורץ, פצלות השדה והזאוליטים.
לטקטוסיליקטים יכולים להצטרף קטיונים נוספים אם חלק מאטומי הצורן מוחלפים בקטיון בעל ערכיות נמוכה יותר כמו האלומיניום (שהוא תלת־ערכי חיובי) כך שהמטען הכללי הוא שלילי. החלפה זו יכולה להתבצע גם בסוגים אחרים של סיליקטים.
בכמה מינרלים נדירים מבנה הגביש מכיל יותר מסוג אחד של מבנה האניון, או שהוא בנוי מאניניונים בעלי מבנה מורכב שהם מבני ביניים בין הסוגים הפשוטים שתוארו לעיל.
קישורים חיצוניים[עריכת קוד מקור | עריכה]
 סיליקט, דף שער בספרייה הלאומית
סיליקט, דף שער בספרייה הלאומית
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ גרדיאן, הטלסקופ ג'יימס ווב גילה כוכב לכת שבו גרגירי חול נושרים כטיפות גשם, הארץ, 22 בנובמבר 2023
