ריברוקסבאן
 | |
| שם IUPAC | |
|---|---|
|
(S)-5-chloro-N-{[2-oxo-3-[4-(3-oxomorpholin-4-yl) phenyl]oxazolidin-5-yl]methyl} thiophene-2-carboxamide | |
| שמות מסחריים בישראל | |
| קסרלטו | |
| נתונים כימיים | |
| כתיב כימי | C19H18N3ClO5S |
| מסה מולרית | 435.882 g/mol |
| נתונים פרמוקוקינטיים | |
| זמינות ביולוגית | בין 80% ל-100%; ריכוז מקסימלי בדם כעבור שעתיים עד 4 שעות מהנטילה (במתן של 10 מ"ג דרך הפה) |
| מטבוליזם | CYP3A4, CYP2J2 ומנגנון שאינו תלוי ב־CYP |
| זמן מחצית חיים | בין 7 ל-11 שעות (במתן של 10 מ"ג דרך הפה) |
| הפרשה | 2/3 עובר מטאבוליזם בכבד, ושליש עובר פינוי ללא שינוי |
| בטיחות | |
| מעמד חוקי | Rx תרופת מרשם בלבד |
| קטגוריית סיכון בהריון |
קטגוריית סיכון C (אוסטרליה), קטגוריית סיכון C |
| דרכי מתן | מתן פומי |
| מזהים | |
| קוד ACT |
B01AF01 |
| מספר CAS | 366789-02-8 |
| PubChem | 6433119 |
| ChemSpider | 8051086 |
ריברוקסבאן (הנמכרת על ידי חברת באייר בשם המסחרי קסרלטו ועל ידע חברת טבע בשם רִיבָר) היא תרופה שפועלת כנוגד קרישה. היא פותחה במטרה למנוע היווצרות קרישי דם, העלולים לגרום לפקקת, לתסחיפים ולאיסכמיה.
ריברוקסבאן פועלת כמעכב פקטור Xa, נספגת דרך המעי ומגיעה לריכוז המקסימלי בדם כארבע שעות מרגע נטילתה.
ניסויים קליניים עיקריים
[עריכת קוד מקור | עריכה]בסך הכל, יותר מ-75,000 נבדקים השתתפו במחקרים השונים של תרופת הריברוקסבאן, שבוצעו במימון חברות באייר וג'ונסון אנד ג'ונסון:
ריברוקסבן במקום אנוקספרין למניעת פקקת אחרי ניתוחי החלפת ירך או ברך
[עריכת קוד מקור | עריכה]ב-2008–2009 פורסמו תוצאות ארבעה מחקרים קליניים מבוקרי הקצאה אקראית ששמם RECORD (רקורד, ראשי תיבות באנגלית של בקרת קרישה בניתוח אורתופדי למניעת פקקת ורידים עמוקים ותסחיף ריאתי: REgulation of Coagulation in ORthopedic Surgery to Prevent DVT and PE). רקורד-1 בדק מנותחי מפרק ירך למשך כשבועיים;[1] רקורד-2 בדק מנותחי מפרק ירך למשך כחודש;[2] רקורד-3 בדק מנותחי החלפת ברך למשך כחודש;[3] ורקורד-4 בדק מנותחי החלפת ברך למשך - 17 יום.[4] בכל ניסויי רקורד, שכללו מעל 12,000 מטופלים בוגרים בניתוחים אלקטיביים, השוו נטילה יומית של 10 מ"ג ריברוקסבן (קסרלטו, הניתנת כגלולה, בבליעה) מול זריקה יומית עצמית של 40 מ"ג אנוקספרין (קלקסאן). החוקרים דיווחו כי ריברוקסבן נמצא יעיל יותר מאנוקספרין במניעת אירועי פקקת ורידית (VTE), אם כי הסיכוי לדימום היה גבוה יותר עם ריברוקסבאן (ללא הבדל משמעותי סטטיסטית בין 2 הקבוצות), ומטופל אחד מתוך 6000 נוטלי הריברוקסבן נפטר מהרעלת כבד. לגבי ניסוי רקורד-4 יש לציין שיו"ר ועדת ההיגוי של המחקר (ושקיבל תשלום מחברת באייר) פרסם ב-12.2022 התנצלות על גילוי מאוחר של התנהלות לא ראויה ודיווח חסר על תופעות לוואי, שהתגלו עוד טרם פרסום המאמר בבקרה של מנהל המזון והתרופות האמריקאי (FDA, שפסל את המחקר הזה).[5]
ריברוקסבן במקום אנוקספרין ווארפרין למטופלים עם פקקת ורידים עמוקים חריפה
[עריכת קוד מקור | עריכה]ב-2010 התפרסמו תוצאות ניסויי EINSTEIN (איינשטיין) מבוקרי ההקצאה האקראית.[6] מחקר EINSTEIN-DVT (Deep Vein Thrombosis, פקקת ורידים עמוקים) השווה בין נטילת תרופת הריברוקסבאן לבדה (15 מ"ג פעמיים ביום למשך שלושה שבועות, ולאחר מכן 20 מ"ג פעם ביום) לבין קבלת זריקות תת-עוריות של אנוקספרין ובהמשך נטילת אנטגוניסט לוויטמין K (וורפרין [א] או אקסנוקומרול) למשך 3, 6, או 12 חודשים אצל מטופלים עם DVT תסמיני.[7] למחקר זה נערך גם מחקר-המשך אקראי רנדומאלי בשם EINSTEIN–Extension,[8] אשר השווה בין נטילת ריברוקסבאן לבדה (20 מ"ג פעם ביום) מול פלצבו למשך 6 או 12 חודשים אצל מטופלים שסיימו טיפול בפקקת ורידית למשך 6 עד 12 חודשים.
הכותבים דווחו כי קסרלטו יכולה לשמש כתרופה בלעדית לטיפול קצר טווח וטיפול ממושך עבור פקקת ורידית, כמו כן היא משפרת את יחס הרווח/הסיכון של תרופות נוגדות קרישה. ריברוקסבאן הציג יעילות דומה לזו של השילוב אנוקספרין-אנטגוניסט לוויטמין K במחקר הראשוני (עם 36 אירועים [2.1%], אל מול 51 אירועים [3.0%] עם אנוקספרין ואנטגוניסט ויטמין K ; יחס סיכון, 0.68; ברמת ביטחון של 95% [CI], 0.44 ל-1.04; non-inferior; 0.001>P). נקודת הבטיחות שהוגדרה התרחשה אצל 8.1% מהמטופלים בכל קבוצה. במחקר ההמשך, אשר כלל 602 מטופלים בקבוצת הריברוקסבאן ו-594 מטופלים בקבוצת הפלסבו, ריברוקסבאן הראה יעילות גבוהה (8 אירועים [1.3%], אל מול 42 עם הפלסבו [7.1%]; יחס סיכון, 0.18; 95% CI, 0.09 ל-0.39; 0.001>P). לארבעה מטופלים מקבוצת הריברוקסבאן היה דימום רציני אך לא קטלני (0.7%), בקבוצת הפלצבו לא היו מקרים כאלו (0.11=P).
ריברוקסבן במקום וארפרין לחולים עם פרפור עליות
[עריכת קוד מקור | עריכה]ב-2011 פורסמו תוצאות ניסוי ROCKET AF (רוקט איי אף, השוואת ריברוקסבן מול חוסמי ויטמין K במניעת תסחיפים; ראשי תיבות באנגלית של Rivaroxaban Once-Daily Compared with Vitamin K Antagonism for Prevention of Embolism Trial in Atrial Fibrillation) המבוקר הקצאה אקראית, ובו נמצא כי לריברוקסבאן במינון 20 מ"ג הייתה השפעה דומה לטיפול בוארפרין (הדורש ניטור מינון) במטופלים עם פרפור פרוזדורים שאינו על רקע מסתמי.[9][10]
ריברוקסבן לאחר אירוע כלילי חריף
[עריכת קוד מקור | עריכה]ב-2012 פורסמו תוצאות ניסוי מבוקר הקצאה אקראית בשם ATLAS ACS 2–TIMI 56 (אטלס איי סי אס 2 טימי 56; ראשי תיבות באנגלית: Anti-Xa Therapy to Lower Cardiovascular Events in Addition to Standard Therapy in Subjects with Acute Coronary Syndrome –Thrombolysis in Myocardial Infarction 46) על טיפול ומניעה משנית של אירועים בלב ובכלי דם אצל 15,526 מטופלים עם תסמונת כלילית חריפה (acute coronary syndrome ACS). בניסוי הושוו תוצאות מינונים של 2.5 מ"ג, 5 מ"ג או פלסבו (כולם פעמיים ביום) למשך 13 חודשים בממוצע. דווח על ירידה באירועי תמותה ממחלות לב וכלי דם מ-4.1% בקבוצה עם פלסבו ל-2.7% בקבוצה עם מינון 2.5 מ"ג וכן על ירידה בתמותה מכלל-הסיבות מ-4.5% ל-2.9% באותן קבוצות.[11][12]
ריברוקסבן במקום אנוקספרין למאושפזים עם מחלה חריפה
[עריכת קוד מקור | עריכה]ב-2013 התפרסמו תוצאות ניסוי MAGELLAN (מגלן) בו השתתפו 8101 מאושפזים עם מחלה חריפה שהוקצו באקראי לנטילה יומית של 10 מ"ג ריברוקסבן ל-35 יום (וזריקת פלסבו ל-10 ימים) מול זריקה יומית עצמית של 40 מ"ג אנוקספרין [ב] ל-10 ימים (וכדור פלסבו ל-35 יום). החוקרים דיווחו על יתרון קליני לריברוקסבן, שהפחית אירועי פקקת ורידית אך הגביר אירועי דימום. התמותה ב-97 יום הייתה 6.7% בקבוצה שהוקצתה לריברוקסבן, ו-6.2% בקבוצה שהוקצתה לאנוקספרין.[13][14][15]
ריברוקסבן לחולי טרשת עורקים יציבה
[עריכת קוד מקור | עריכה]ב-2017 פורסמו תוצאות ניסוי COMPASS המבוקר הקצאה אקראית, שבו נבדקו 27,395 מטופלים עם טרשת עורקים יציבה למשך 23 חודשים בממוצע, נמצא כי בהשוואה לאספירין 100 מ"ג בלבד, שילוב של ריברוקסבאן במינון 2.5 מ"ג, פעמיים ביום, עם אספירין 100 מ"ג, הפחית באופן מובהק את שיעור סך אירועי הלב וכלי הדם (מוות ממחלת לב וכלי דם, שבץ מוחי, התקף לב) מ-5.4% ל-4.1%, אך שיעור אירועי דימום קשים עלה מ-1.9% ל-3.1%. ההשפעה על התמותה הכוללת לא הגיעה למובהקות שהוגדרה מראש.[16]
ב-2018 פורסם ניתוח נוסף של תוצאות ניסוי COMPASS. ניתוח, שכלל רק את 24,824 המטופלים שהיו עם טרשת עורקים כליליים יציבה. החוקרים דיווחו על השפעה מובהקת על התמותה הכוללת, שירדה מ-4% בקבוצת האספירין בלבד, ל-3% בקבוצת השילוב של ריברוקסבאן במינון 2.5 מ"ג, פעמיים ביום, עם אספירין.[17]
ריברוקסבן לחולי אי ספיקת לב
[עריכת קוד מקור | עריכה]ב-2018 פורסמו תוצאות ניסוי COMMANDER HF (קומנדר איי אף, במימון חברת יאנסן) שבו נבדקו 5022 אנשים עם אי ספיקת לב סיסטולית באמצעות הקצאה אקראית לנטילת ריברוקסבאן במינון 2.5 מ"ג, פעמיים ביום, או פלסבו: לא נמצא הבדל משמעותי-סטטיסטית בתוצאות העיקריות שנבדקו.[18]
מינון והתוויות
[עריכת קוד מקור | עריכה]קסרלטו מאושרת בישראל לשימוש במינונים שונים לשבע ההתוויות הבאות:[19] במינון 20 מ"ג, פעם ביום, למניעת שבץ מוחי באנשים שאובחנו עם פרפור עליות (בתנאים מסוימים);
במינון 15 מ"ג, פעמיים ביום, ל-3 שבועות, לטיפול בפקקת ורידים עמוקים ותסחיף ריאתי;
במינון 20 מ"ג פעם ביום, לחצי שנה, למניעת הישנות פקקת ורידים עמוקים ותסחיף ריאתי בחולים בוגרים;
במינון 10 מ"ג, פעם ביום, למניעה כנ"ל אחרי מעל לחצי שנה וכן למניעת פקקת ורידים עמוקים ותסחיף ריאתי (Deep Vain Thrombosis) בחולים לאחר ניתוח אלקטיבי להחלפת פרק ירך או ברך;
ובמינון 2.5 מ"ג, פעמיים ביום, (יחד עם אספירין 100 מ"ג) לחולי טרשת עורקים תסמינית יציבה ולחולים לאחר אוטם שריר הלב.
זמן מחצית החיים של התרופה הוא 7–11 שעות, ופעילותו של פקטור Xa חוזרת לתפקוד רגיל רק לאחר כ-24 שעות, לכן בדרך כלל התרופה ניתנת במינון יומי קבוע.[20]
למניעת פקקת ורידים תסחיפית: מחקר רחב בשם EINSTEIN CHOICE שהוצג בכתב העת New England Journal of Medicine בדק את היעילות של נוגד הקרישה קסרלטו מול אספירין בהפחתת הסיכון לאירוע חוזר של פקקת ורידים תסחיפית. תוצאות המחקר הראו כי מתן קסרלטו למטופלים הפחית את הסיכון לאירוע חוזר של פקקת ורידים תסחיפית ב-66% בקבוצת המטופלים בקסרלטו לעומת קבוצת המטופלים באספירין. תוצאות מחקר EINSTEIN CHOICE התפרסמו ב-New England Journal of Medicine והוצגו במושב המרכזי בכנס האיגוד הקרדיולוגי האמריקאי (ACC). המחקר כלל 3,396 חולים והתקיים במעל 200 מרכזים רפואיים ב-31 מדינות בעולם, בהן ישראל. 11 מרכזים רפואיים השתתפו במחקר בישראל, בהם רמב"ם, איכילוב, בילינסון.
מנגנון פעולה
[עריכת קוד מקור | עריכה]ריברוקסבאן פותחה במטרה למנוע היווצרות קרישי דם העלולים לגרום לשני סיכונים עיקריים: שבץ מוחי ופקקת ורודים עמוקים. שבץ מוחי נגרם בגלל קריש דם שחוסם עורק המוביל דם למוח. הקריש יכול להיווצר באזור החסימה או להגיע לאזור ממקום אחר בגוף (אז הוא מכונה תסחיף, כי הוא נסחף בזרם הדם).[21] אנשים המצויים בסיכון להיפגע מקריש דם מטופלים בדרך כלל בנוגדי קרישה.
התרופה פועלת באמצעות חסימת מנגנון קרישת דם על ידי חסימת הפעילות של פקטור Xa - אנזים חיוני במנגנון הקרישה. חסימת פקטור Xa בולמת, בתורה, את היווצרותו של האנזים תרומבין, החיוני להמשך תהליך הקרישה, ובכך פוגמת התרופה בתהליכי קרישת הדם ומונעת את היווצרות הקרישים. ריברוקסבאן אינו מעכב תרומבין (פקטור פעיל II), ולא נצפו השפעות של פעולתו על טסיות הדם. מנגנון הפעילות של התרופה מבטיח תגובה יציבה ורציפה ללא צורך בשינוי המינון או במעקב אחר תפקודי הקרישה. לריברוקסבאן יש השפעה דומה בקרב ספקטרום רחב של מטופלים (גילאים, מגדרים, משקלים וגזעים שונים), וניסויים קליניים מראים שהתרופה בעלת פעילות נוגדת קרישה צפויה, המאפשרת מינון קבוע ללא התאמות ושינויים. ניסויים אלו לא כללו מטופלים עם מחלות כבד, ביניהם מחלות כבד סופניות, לכן השימוש בתרופה אצל מטופלים אלו עלול להיות מסוכן.
אישורים והתויות בישראל ובעולם
[עריכת קוד מקור | עריכה]אישורים והתוויות בישראל:
ב-2010 קסרלטו אושרה למניעה ראשונית של פקקת ורידים תסחיפית (VTE) אצל מטופלים בוגרים אשר עברו ניתוחים להחלפת מפרקי ירך או ברך.
ב-2012 אושרה למניעת שבץ מוחי באנשים שאובחנו עם פרפור עליות.
ב-2013 אושרה לטיפול בפקקת ורידים תסחיפית, ולמניעת הישנות פקקת ורידים תסחיפית.
התרופה כלולה בסל התרופות לפי קריטריונים רפואיים.[22]
אישורים והתוויות בעולם:
2008 - משרד הבריאות הקנדי אישר את שיווקה של ריברוקסבאן (קסרלטו) במינון של 10 מ"ג פעם ביום, למטופלים שעברו ניתוחים להחלפת מפרקי ירך או ברך[23] על מנת למנוע VTE - פקקת ורידים תסחיפית.
2008 - הסוכנות האירופית לתרופות (EMA) אישרה שימוש בריברוקסבאן (קסרלטו) למניעת VTE - פקקת ורידים תסחיפית - אצל מטופלים בוגרים אשר עברו ניתוחים להחלפת מפרקי ירך או ברך.[24]
2011 - מנהל המזון והתרופות האמריקאי (FDA) אישר את השימוש בריברוקסבאן כטיפול מונע עבור DVT - פקקת ורידים עמוקה, אשר עלולה לגרום לתסחיף ריאתי אצל מטופלים בוגרים אשר עברו ניתוחים להחלפת מפרקי ירך או ברך. התרופה רשומה בהתוויה זו גם בישראל מפברואר 2010.
2011 - מנהל המזון והתרופות האמריקאי (FDA) אישר את השימוש בריברוקסבאן (קסרלטו) כתרופה למניעת שבץ מוחי ותסחיף סיסטמי אצל מטופלים עם פרפור פרוזדורים שאינו על רקע מסתמי (הפרעה בקצב הלב).
2011 - הסוכנות האירופית לתרופות (EMA) אישרה את השימוש בריברוקסבאן באינדיקציה זו (מניעת שבץ מוחי ותסחיף סיסטמי בחולים עם פרפור פרוזדורים), וכן לטיפול בפקקת ורידים עמוקה (DVT) ומניעת הישנות פקקת ורידים תסחיפית (פקקת ורידים עמוקה ותסחיף ריאתי)[25]
2011 - מנהל המזון והתרופות האמריקאי (FDA) אישר את השימוש בריברוקסבאן (קסרלטו) כתרופה למניעת שבץ מוחי ותסחיף ריאתי אצל מטופלים עם פרפור פרוזדורים ובדצמבר 2011 הרשות הרגולטורית האירופאית אישרה אף היא את השימוש בריברוקסבאן בהתוויה זו, וכן לטיפול בפקקת ורידים עמוקה (DVT) ומניעת הישנות פקקת ורידים תסחיפית (פקקת ורידים עמוקה ותסחיף ריאתי)[26]
ריברוקסבאן למניעת שבץ מוחי
[עריכת קוד מקור | עריכה]לפי הקווים המנחים (Guidelines) של האיגוד הקרדיולוגי האירופי מספטמבר 2016, נוגדי קרישה מהדור החדש (קסרלטו, פראדקסה ואליקויס) יהיו הסטנדרט הטיפולי בחולי פרפור פרוזדורים. משמעות ההנחיה לעבור באופן כמעט גורף לנוגדי הקרישה החדשים היא שיפור משמעותי בהגנה מפני קרישי דם, שכן בתרופות החדשות קל בהרבה להשתמש ולהתמיד בשימוש. לפי הודעת האיגוד הקרדיולוגי האירופי: "מאחר שנוגדי הקרישה החדשים הראו בניסויים קליניים שהם יעילים לפחות כמו קומדין במניעת שבץ; ובנוסף, מציגים יתרון עקבי בבטיחות התרופה והפחתה במספר הדימומים התוך-מוחיים (זה הסיבוך שממנו חוששים יותר מכל - בטיפול בנוגדי קרישה), נוגדי הקרישה החדשים צריכים להיות בחירת הטיפול העדיפה (broadly preferred) על פני קומדין, ברוב המוחלט של המקרים".[27]
בכינוס השנתי של האיגוד הקרדיולוגי האירופי (ספטמבר 2016) הוצגו נתונים ולפיהם ניתן למנוע 90% ממקרי השבץ המוחי, אולם אחוזים גדולים של מטופלים מקבלים מינון נמוך מכפי שהיו אמורים לקבל, לפי נתוניהם הרפואיים. נתוני המחקר הצביעו על כך שמתן תרופות נוגדות קרישה במינון נמוך מהרצוי, מעלה את הסיכון לשבץ בקרב המטופלים.[28] קסרלטו הראתה יעילות מובהקת בהפחתה של 42% בשיעור מקרי השבץ לעומת מי שנטלו אספירין בלבד.[29][16]
חיסרון עיקרי בנוגדי הקרישה מהדור החדש, למעט דגיבטרן, הוא העדרה של תרופת נגד (אנ') שתאפשר עצירת דימומים מסכני חיים.[30]
כימיה
[עריכת קוד מקור | עריכה]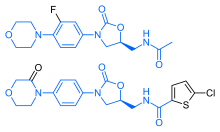
לריברוקסבאן יש מבנה כימי כמעט זהה לתרופה האנטיביוטית לינזוליד: שתי התרופות חולקות את אותו המבנה של משפחת התרופות האוקסלידינונים. בהתאם לכך, ריברוקסבאן נחקר עבור השפעות אנטיביוטיות. מחקרים הראו שאין לריברוקסבאן או למטאובוליטים שלו השפעה אנטיביוטית נגד חיידקים גראם-חיוביים.
תרופות דומות
[עריכת קוד מקור | עריכה]ישנם מספר נוגדי קרישה אשר מעכבים את פעילותו של פקטור Xa. הפרין בלתי מפוצל (Unfractionated Heparin, UFH), הפרין של משקל-מולקולרי-נמוך (LMWH), ו-fondaparinux (משווק בשם אריקסטרה) מעכבים את פקטור Xa באופן עקיף, על ידי היקשרותם לאנטיטרומבין (AT III). את התרופות האלו ניתן לקבל רק בזריקה.
וורפין, פרנפרוקומון, ואקסנוקומרול הם אנטגוניסטים לוויטמין K שניתנים לנטילה פומית. תרופות אלו מפחיתות את הסינתזה בכבד של מספר גורמים הקשורים לקרישת דם, ביניהם פקטור X.
סדרה חדשה יותר של תרופות פומיות, אשר מעכבות את פעילות של פקטור Xa, כוללת את ריברוקסבאן, אפיקסבאן, אדוקסבאן (DU-176b), בֶּטְרִיקְסָבָּאן, YM150 (דָרֶקְסָבָּאן (אנ')), ו-LY517717.
דביגטראן, היא תרופה לנטילה פומית, המעכבת את פעילות פקטור II (תרומבין).
כלכלה, חברה ומשפט
[עריכת קוד מקור | עריכה]על פי סוכנות תרופות אמריקאית, עלות השימוש בקסרלטו היא פי 70 מעלות השימוש בוורפרין (קומדין).[31] היצרנית באייר דיווחה על מכירות התרופה ב-2020 בסכום של 4.5 מיליארד אירו.[32]
ב-25 במרץ 2019, בעקבות מעל ל-25,000 תביעות משפטיות בעניין התרופה בארצות הברית, שולמו לנפגעים 775 מיליון דולר. התובעים האשימו את יצרניות התרופות (באייר וג'ונסון אנד ג'ונסון) שלא הזהירו כראוי מפני הסיכון לדימומים, וטענו כי ניתן היה למנוע נזק בריאותי אילו נמסר לרופאים ולמטופלים מידע הולם.[33]
בדצמבר 2022 מסר העיתון לאנסט על פתיחת חקירה בעניין פרסום ניסוי רפואי בתרופה לאחר החלפת ברך (ניסוי שנקרא Record4, ופורסם בעיתון ב-2009),[34] בשל דיווח ה-FDA על תקלות חמורות בביצוע ובאובדן דיווחים על תופעות הלוואי.[35]
קישורים חיצוניים
[עריכת קוד מקור | עריכה]- פרופ' שלמה מטצקי, התרופה שמחוללת מהפכה במדללי דם, באתר ynet, 06 בספטמבר 2017
- רותם אליזרע, מחקרים מצאו: נוגדי הקרישה "מהדור החדש" יעילים יותר, באתר ynet, 15 במאי 2017
- פרופ' נתן בורנשטיין, כך נמנע שבץ מוחי וגם נחסוך עלויות, באתר כלכליסט, 02 בפברואר 2015
 פרופסור ראובן צימליכמן, הרופאים מפחדים - והסיכון לשבץ מוחי עולה, באתר הארץ, 28 בנובמבר 2016
פרופסור ראובן צימליכמן, הרופאים מפחדים - והסיכון לשבץ מוחי עולה, באתר הארץ, 28 בנובמבר 2016- ליאת רותם מלמד, מחקר ענק: נטילת קומדין אינה מגינה מפני שבץ, באתר ynet, 06 בדצמבר 2012
- ליאת רותם מלמד, חשים "דפיקות לב"? זה עלול להסתיים במוות, באתר ynet, 14 בנובמבר 2013
- "קרישי דם, האויב השקט" "דוקטורס"
- עמותת נאמן לנפגעי שבץ מוחי
- התוויות לשימוש בקסרלטו מאגר התרופות, אגף הרוקחות במשרד הבריאות
ביאורים
[עריכת קוד מקור | עריכה]- ^ ווארפרין מוכר יותר בשמו המסחרי: קומדין, היא תרופה המצריכה ניטור מינון באמצעות בדיקות בדיקות תפקודי קרישה.
- ^ אנוקספרין מוכר בארץ בשמו המסחרי קלקסן.
הערות שוליים
[עריכת קוד מקור | עריכה]- ^ Bengt I. Eriksson, Lars C. Borris, Richard J. Friedman, Sylvia Haas, Menno V. Huisman, Ajay K. Kakkar, Tiemo J. Bandel, Horst Beckmann, Eva Muehlhofer, Frank Misselwitz, William Geerts, Rivaroxaban versus Enoxaparin for Thromboprophylaxis after Hip Arthroplasty, New England Journal of Medicine 358, 2008-06-26, עמ' 2765–2775 doi: 10.1056/NEJMoa0800374 (באנגלית)
- ^ Ajay K. Kakkar, Benjamin Brenner, Ola E. Dahl, Bengt I. Eriksson, Patrick Mouret, Jim Muntz, Andrea G. Soglian, Akos F. Pap, Frank Misselwitz, Sylvia Haas, RECORD2 Investigators, Extended duration rivaroxaban versus short-term enoxaparin for the prevention of venous thromboembolism after total hip arthroplasty: a double-blind, randomised controlled trial, Lancet (London, England) 372, 2008-07-05, עמ' 31–39 doi: 10.1016/S0140-6736(08)60880-6 (באנגלית)
- ^ Michael R. Lassen, Walter Ageno, Lars C. Borris, Jay R. Lieberman, Nadia Rosencher, Tiemo J. Bandel, Frank Misselwitz, Alexander G. G. Turpie, RECORD3 Investigators, Rivaroxaban versus enoxaparin for thromboprophylaxis after total knee arthroplasty, The New England Journal of Medicine 358, 2008-06-26, עמ' 2776–2786 doi: 10.1056/NEJMoa076016 (באנגלית)
- ^ Alexander G. G. Turpie, Michael R. Lassen, Bruce L. Davidson, Kenneth A. Bauer, Michael Gent, Louis M. Kwong, Fred D. Cushner, Paul A. Lotke, Scott D. Berkowitz, Tiemo J. Bandel, Alice Benson, Frank Misselwitz, William D. Fisher, RECORD4 Investigators, Rivaroxaban versus enoxaparin for thromboprophylaxis after total knee arthroplasty (RECORD4): a randomised trial, Lancet (London, England) 373, 2009-05-16, עמ' 1673–1680 doi: 10.1016/S0140-6736(09)60734-0 (באנגלית)
- ^ Alexander G. G. Turpie, Revisiting RECORD4, Lancet (London, England) 400, 2022-12-10, עמ' 2047–2048 doi: 10.1016/S0140-6736(22)02422-9 (באנגלית)
- ^ Oral Direct Factor Xa Inhibitor Rivaroxaban In Patients With Acute Symptomatic Pulmonary Embolism (PE) With Or Without Symptomatic Deep-Vein Thrombosis: Einstein-PE Evaluation
- ^ Oral Direct Factor Xa Inhibitor Rivaroxaban In Patients With Acute Symptomatic Deep-Vein Thrombosis (DVT) Without Symptomatic Pulmonary Embolism: Einstein-DVT Evaluation
- ^ Once-Daily Oral Direct Factor Xa Inhibitor Rivaroxaban in the Long-Term Prevention of Recurrent Symptomatic Venous Thromboembolism in Patients With Symptomatic Deep-Vein Thrombosis or Pulmonary Embolism. The Einstein-Extension Study
- ^ Randomized, Double-Blind Study Comparing Once Daily Oral Rivaroxaban With Adjusted-Dose Oral Warfarin for the Prevention of Stroke in Subjects With Non-Valvular Atrial Fibrillation
- ^ Manesh R. Patel, Kenneth W. Mahaffey, Jyotsna Garg, Guohua Pan, Daniel E. Singer, Werner Hacke, Günter Breithardt, Jonathan L. Halperin, Graeme J. Hankey, Jonathan P. Piccini, Richard C. Becker, Christopher C. Nessel, John F. Paolini, Scott D. Berkowitz, Keith A. A. Fox, Robert M. Califf, ROCKET AF Investigators, Rivaroxaban versus warfarin in nonvalvular atrial fibrillation, The New England Journal of Medicine 365, 2011-09-08, עמ' 883–891 doi: 10.1056/NEJMoa1009638 (באנגלית)
- ^ A Randomized, Double-Blind, Placebo-Controlled, Event-Driven Multicenter Study to Evaluate the Efficacy and Safety of Rivaroxaban in Subjects With a Recent Acute Coronary Syndrome
- ^ Jessica L. Mega, Eugene Braunwald, Stephen D. Wiviott, Jean-Pierre Bassand, Deepak L. Bhatt, Christoph Bode, Paul Burton, Marc Cohen, Nancy Cook-Bruns, Keith A.A. Fox, Shinya Goto, Sabina A. Murphy, Alexei N. Plotnikov, David Schneider, Xiang Sun, Freek W.A. Verheugt, C. Michael Gibson, Rivaroxaban in Patients with a Recent Acute Coronary Syndrome, New England Journal of Medicine 366, 2012-01-05, עמ' 9–19 doi: 10.1056/NEJMoa1112277 (באנגלית)
- ^ MAGELLAN - Multicenter, Randomized, Parallel Group Efficacy Superiority Study in Hospitalized Medically Ill Patients Comparing Rivaroxaban with Enoxaparin
- ^ Johnson & Johnson Pharmaceutical Research & Development, L.L.C., Multicenter, Randomized, Parallel-group Efficacy and Safety Study for the Prevention of Venous Thromboembolism in Hospitalized Medically Ill Patients Comparing Rivaroxaban With Enoxaparin. The MAGELLAN Study, 2016-08-03, עמ' טבלה 12 (באנגלית)
- ^ Venous Thromboembolic Event (VTE) Prophylaxis in Medically Ill Patients (MAGELLAN)
- ^ 1 2 Rivaroxaban with or without Aspirin in Stable Cardiovascular Disease
- ^ Stuart J. Connolly, John W. Eikelboom, Jackie Bosch, Gilles Dagenais, Leanne Dyal, Fernando Lanas, Kaj Metsarinne, Martin O'Donnell, Anthony L. Dans, Jong-Won Ha, Alexandr N. Parkhomenko, Alvaro A. Avezum, Eva Lonn, Liu Lisheng, Christian Torp-Pedersen, Petr Widimsky, Aldo P. Maggioni, Camilo Felix, Katalin Keltai, Masatsugu Hori, Khalid Yusoff, Tomasz J. Guzik, Deepak L. Bhatt, Kelley R. H. Branch, Nancy Cook Bruns, Scott D. Berkowitz, Sonia S. Anand, John D. Varigos, Keith A. A. Fox, Salim Yusuf, COMPASS investigators, Rivaroxaban with or without aspirin in patients with stable coronary artery disease: an international, randomised, double-blind, placebo-controlled trial, Lancet (London, England) 391, 2018-01-20, עמ' 205–218 doi: 10.1016/S0140-6736(17)32458-3 (באנגלית)
- ^ Faiez Zannad, Stefan D. Anker, William M. Byra, John G.F. Cleland, Min Fu, Mihai Gheorghiade, Carolyn S.P. Lam, Mandeep R. Mehra, James D. Neaton, Christopher C. Nessel, Theodore E. Spiro, Dirk J. van Veldhuisen, Barry Greenberg, Rivaroxaban in Patients with Heart Failure, Sinus Rhythm, and Coronary Disease, New England Journal of Medicine 379, 2018-10-04, עמ' 1332–1342 doi: 10.1056/NEJMoa1808848 (באנגלית)
- ^ באייר, קסרלטו 2.5, 5, 10, 20 מג, מדריך לרופא (עמ' 7), באתר משרד הבריאות, 31.01.2021
- ^ קסרלטו באתר "אינפומד"
- ^ "אירוע מוחי", אתר "שירותי בריאות כללית"
- ^ קסרלטו 10 מ"ג - עלון לצרכן עם התוויות לשימוש, אגף הרוקחות במשרד הבריאות
- ^ to Help Prevent Deep Vein Thrombosis in Patients Undergoing Knee or Hip Replacement Surgery Bayer's Xarelto Approved in Canada
- ^ Bayer’s Novel Anticoagulant Xarelto now also Approved in the EU
- ^ Rivaroxaban approved in Europe for AF and DVT treatment
- ^ FDA Approves Oral Anticoagulant Rivaroxaban for DVT Prevention at Surgery
- ^ 2016 ESC Guidelines for the management of atrial fibrillation,European Heart Journal
- ^ Effectiveness And Safety Of Reduced Dose Non-Vitamin K Antagonist Oral Anticoagulants In Patients Without Severe Renal Impairment,Value in Health Volume 19, Issue 3, May 2016, Pages A2
- ^ פרדיגמת טיפול חדשה בהפחתת אירועים קרדיו-וסקולריים, המתבססת על תוצאות מחקר COMPASS
- ^ S. Galliazzo, M. P. Donadini, W. Ageno, Antidotes for the direct oral anticoagulants: What news?, Thrombosis Research 164 Suppl 1, 2018-04, עמ' S119–S123 doi: 10.1016/j.thromres.2018.01.006 (באנגלית)
- ^ "New blood thinner 'antidote' to help doctors move past warfarin". Reuters (באנגלית). 2015-12-23. נבדק ב-2023-01-13.
- ^ Stefan Oelrich, President of the Pharmaceuticals Division, Capital Markets Day 2021 (עמ' 3), www.bayer.com, 10/03/2021 (באנגלית)
- ^ "Bayer, Johnson & Johnson settle more than 25,000 lawsuits over blood thinner Xarelto for $775 million". Washington Post (באנגלית אמריקאית). ISSN 0190-8286. נבדק ב-2023-01-13.
- ^ Alexander G. G. Turpie, Michael R. Lassen, Bruce L. Davidson, Kenneth A. Bauer, Michael Gent, Louis M. Kwong, Fred D. Cushner, Paul A. Lotke, Scott D. Berkowitz, Tiemo J. Bandel, Alice Benson, Frank Misselwitz, William D. Fisher, RECORD4 Investigators, Rivaroxaban versus enoxaparin for thromboprophylaxis after total knee arthroplasty (RECORD4): a randomised trial, Lancet (London, England) 373, 2009-05-16, עמ' 1673–1680 doi: 10.1016/S0140-6736(09)60734-0
- ^ Maryanne Demasi, Rivaroxaban: Lancet opens investigation into anticlotting drug trial after BMJ report, BMJ (Clinical research ed.) 379, 2022-12-30, עמ' o3071 doi: 10.1136/bmj.o3071
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.
