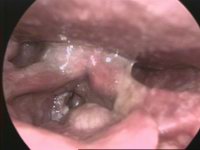
סרטן הגרון
 | |
| תחום |
אונקולוגיה |
|---|---|
| טיפול | |
| קישורים ומאגרי מידע | |
| eMedicine | 848592 |
| MeSH | D007822 |
| סיווגים | |
| ICD-10 | C32 |
| ICD-11 |
2C23 |
סרטן הגרון הוא גידול ממאיר המתפתח ב"בית הקול" (לרינקס) – האזור שמתחיל בעצם הלשון ומסתיים מעל הגבול העליון של קנה הנשימה. רוב סרטני הגרון יופיעו במיתרי הקול והגלוטיס (סדק הקול) כאשר היתר יוצגו מעליהם ולעיתים נדירות מתחתם. סוג הגידול הראשי והעיקרי בתחום (95% מהמקרים) הוא קרצינומה של תאי קשקש (SCC – Squamous Cell Carcinoma), שמקור שמו בתאים הקשקשיים המצפים את קירות הגרון. סרטן הגרון יכול להתפשט על ידי גרורות לבלוטות לימפה צוואריות או על גבי זרם הדם לאיברים מרוחקים יותר (האתר השכיח ביותר להופעת גרורות – הריאות). סימנים מוקדמים להופעת המחלה יכולים להיות צרידות ממושכת, תחושה של גוף זר, כאבים בלעיסה ובבליעה שעלולים להקרין לאוזן או הפרעות בבליעה. חולה שאובחן אצלו גידול יזדקק לבדיקות אשר יגדירו את גבולות הגידול ואת מאפייני רקמת הגידול, כדי לתכנן את הטיפול המיטבי בעבורו.
תסמינים[עריכת קוד מקור | עריכה]
תסמיני סרטן הגרון תלויים בגודל ובמיקום הגידול ובתגובה הדלקתית של הגוף (כחלק מתגובת המערכת החיסונית המנסה להגיב נגד הגידול). מנעד התסמינים אמנם תלוי בגידול הספציפי, במיקומו בגרון ובמצב הרפואי הכללי של החולה, אך הם יכללו בדרך כלל אחד או יותר מהבאים:
- צרידות או שינויי קול (זהו בדרך כלל התסמין הראשון שמופיע בסרטן הממוקם על פני מיתרי הקול עצמם), בדרך כלל במשך יותר מ-4 שבועות
- גוש בצוואר
- כאב גרון או תחושה שמשהו "תקוע" בגרון
- שיעול טורדני וממושך
- הפרעות נשימה: קוצר נשימה, צפצופים/חרחורים (סטרידור)
- היעדר קול (Dysphonia/aphonia)
- קשיי אכילה (Dysphagia)
- כאב בעת בליעה
- ריח פה לא נעים
- כאב אוזן קבוע (כאב מקרין)
- חנק (aspiration)
- תשישות וחולשה
- רזון
אפידמיולוגיה (שכיחות באוכלוסייה)[עריכת קוד מקור | עריכה]
יחסית לסוגי סרטן אחרים, כמו סרטן הריאה, השד, הערמונית והמעי, שבכל אחד מהם נרשמים אלפי חולות וחולים חדשים בישראל בשנה (כ-4,000 בסרטן שד, כ-2,500 בסרטן ערמונית וכך הלאה) – הרי שהתחלואה בסרטן גרון שכיחה הרבה פחות. בישראל, בשנת 2010, היו כ-200 חולים חדשים בסרטן הגרון. המחלה אמנם נדירה, אך שכיחה יותר בקרב גברים לעומת נשים. בקרב האוכלוסייה היהודית בישראל, שיעור היארעות סרטן הגרון בקרב גברים הוא כ-4 ל-100,000 ואצל נשים – כ-0.63 ל-100,000. באוכלוסייה הלא- יהודית בישראל, שיעור היארעות המחלה בקרב גברים מעט גבוה יותר ועומד על כ-6 ל-100,000.
בארצות הברית שיעור ההיארעות של המחלה הוא 5 ל-100,000 (12,500 מקרים חדשים לשנה). מספר החולים הנמוך, יחסית (פחות מ-200 אלף איש באמריקה בשנה) אף הביא אותו להיכלל ברשימת המחלות של המשרד למחלות נדירות של הסוכנות הלאומית לבריאות (ORD of National Institute of Health).
בשנת 2013 נפטר השחקן והקומיקאי הישראלי ספי ריבלין מהישנות (חזרה של המחלה, לאחר הפוגה וריפוי זמני) של סרטן הגרון, לאחר תקופת התמודדות ממושכת שבמהלכה אף נאלץ לעבור ניתוח כריתת גרון מלאה.
בשנת 2004 נפטרה מסרטן הגרון יהודית נאות, פרופ' למיקרוביולוגיה בפקולטה לרפואה של הטכניון, ח"כ ושרה בממשלת ישראל ה-30.
פתופיזיולוגיה (אופן התפתחות המחלה)[עריכת קוד מקור | עריכה]
גידולים ממאירים של הגרון עלולים להשפיע על פיזיולוגיית הגרון (צורת ומבנה האיבר) כתלות במיקום הסרטן וגודלו. גידולים מעל הגלוטיס (החלק האמצעי של הגרון, שבו נמצאים מיתרי הקול) עשויים שלא להשפיע על תפקוד הגרון עד שהם מתפתחים לגודל גדול יחסית. במצב זה, שינוי גוון הקול, הפרעות בבליעה וכאבי בליעה עלולים להיות התסמינים הראשונים.
לעומת זאת, גידולים בגלוטיס משנים את איכות הקול עוד בשלבים המוקדמים של התפתחותם ולכן מאובחנים בדרך כלל בשלבים מוקדמים של המחלה עקב צרידות מתמשכת.
התפתחות הגידולים הממאירים של הגרון ושגשוגם מתרחשים ברמה המולקולרית וההיסטולוגית. בעוד שהמנגנון המולקולרי עדיין איננו ברור במלואו, המנגנון ההיסטולוגי ידוע ומתרחש במספר שלבים: החל מרקמת מוקוזה (רירית) נורמלית, דרך מוקוזה דיספלסטית, קרצינומה לא פולשנית (in-situ) ועד קרצינומה פולשנית. התקדמות זו מבוססת על מוטציות גנטיות, המובילה לגידולים בגרון. ההתקדמות לא מופיעה בהכרח בכל חולה, וחולים מסוימים מתגלים לראשונה עם שלב אחרון של התקדמות סרטנית זו (דהיינו סרטן חודרני).
גורמי הסיכון[עריכת קוד מקור | עריכה]
גורמי הסיכון לסרטן הגרון אינם ידועים במלואם וההערכה היא כי ישנם מספר גורמים התורמים במשולב להתפתחות המחלה. עם זאת, ישנם מספר גורמים שנמצאו כי מעלים את שכיחותה:
- עישון סיגריות
- שתיית אלכוהול
- זיהום ויראלי מסוג פפילומה (HPV)
- שכיחות גבוהה יותר בגברים
- גיל מתקדם
סרטן הגרון מתגלה לרוב מעל גיל 55 ומצוי בשכיחות גבוהה יותר בגברים. קרוב לוודאי עקב כך שעישון וצריכת אלכוהול נהוגים יותר בקרב גברים. עישון נמצא כי מעלה את הסיכוי למוות מסרטן הגרון פי 20 ביחס לאנשים שאינם מעשנים. גם לשתיית אלכוהול השפעה משמעותית. בשילוב של שני גורמי סיכון אלו נוצר אפקט סינרגיסטי אשר מעלה את הסיכון אף יותר, במיוחד בצריכה לטווח ארוך.
אבחנה[עריכת קוד מקור | עריכה]
האבחנה תורכב מראיון רפואי על מצב החולה ועברו הרפואי, בדיקה גופנית, מבט על הגרון שעשוי לכלול בדיקת ראי גרון (לרינגוסקופיה) ישירה או עקיפה (באמצעות סיב אופטי) וכן בדיקות הדמיה (כגון CT, MRI ורנטגן) וביופסיה (בדרך כלל בהרדמה מלאה).
הבדיקה הגופנית תהיה בדיקה כללית של החולה לאמוד מצב בריאותי כללי ותכלול מישוש ובדיקה חיצונית של כלל אזור הצוואר לנפיחויות כלליות ולימפתיות או לרמזים למחלה גרורתית.
בדיקת גרון (לרינגוסקופיה) - חלל הפה והגרון נבדקים על ידי ראייה ישירה על מנת לקבוע הימצאות גידול, מיקומו וגבולותיו. חלל הגרון נבדק באמצעות בדיקת ראי גרון עקיפה הכוללת שימוש בפנס ומראה מעוקלת המחוברת לידית ארוכה (בדומה למראת רופא השיניים), או בדיקת ראי גרון ישירה המבוצעת על ידי טלסקופ גמיש המוחדר לגרון דרך האף או הפה. בדיקה זו מאפשרת קביעת הימצאות גידול, מיקומו, גבולות חדירה ראשוניים ומידותיו.
ביופסיה - במקרה ויש חשד לגידול סרטני תבוצע ביופסיה, בדרך כלל תחת הרדמה כללית. בבדיקה זו מתבצעת בדיקת תאים מהדגימה תחת מיקרוסקופ. בצורה זו מתאפשרת אבחנה מבדלת של מאפייני רקמת הגידול וניתן להוכיח בצורה היסטולוגית קיום סרטן, סוגו ושלב הגידול. תוצאות הביופסיה מתקבלות כעבור כשבוע. במקרה שיש גידול קטן הממוקם בצורה ברורה, המנתח עשוי לבצע ביופסיה חיתוכית שמהווה ניסיון להסיר את הגידול לחלוטין בזמן הביופסיה הראשונית. במקרה הזה תפקיד הבדיקה הפתולוגית בנוסף למתן הדיאגנוזה הסרטנית יהיה לאבחן אם הגידול הוסר בשלמותו. בדיקה אנדוסקופית מלאה של חלל הגרון, קנה הנשימה והושט בדרך כלל מבוצעת בזמן הביופסיה.
הדמיה (רנטגן, סיטי, אולטרסאונד) - צילומי רנטגן יבוצעו בעיקר על מנת לברר האם ישנם תאים סרטניים שהגיעו לריאות ויצרו גידולים גרורתיים. בדיקות הדמיה מסוג CT ו–MRI יסייעו להגדרת התפשטות הגידול ופיזורו לבלוטות הלימפה ולאיברים מרוחקים. US מהווה בדיקה מדויקת ביותר לנוכחות בלוטות לימפה חשודות בצוואר כאשר מבוצע בידיים מיומנות.
ניהול תוכנית הטיפול יהיה תלוי באזור, בשלב הגידול (גודל הגידול, התפשטות לבלוטות לימפה, גרורות מרוחקות) וסיווג היסטולוגי. בריאות כללית ובקשת המטופל חייבת להילקח בחשבון.
קביעת שלב הגידול (staging)[עריכת קוד מקור | עריכה]
על מנת לתכנן את הטיפול המיטבי לכל חולה יש לקבוע את היקף המחלה, כלומר את שלב הגידול. מחלה בשלב ראשוני יחסית צפויה להיות עם פרוגנוזה (תחזית להתפתחות המחלה) טובה יותר, בעוד שמחלה בשלב מתקדם תהיה כזו שסיכויי הריפוי שלה גבוהים פחות.
המידע נקבע באמצעות הבדיקה הגופנית, הביופסיה ובדיקות הדימות. את השלב נקבע לפי מספר משתנים בעזרת צורת סיווג מסוג TNM המדרגת את חומרת הגידול לפי גודלו (Tumer), פיזור לבלוטות לימפה (Lymph Node) ופיזור גרורתי (Metastasis). גודלו של הגידול נאמד מ-T1-4 כאשר T1 מסמן גידול קטן ביותר ו-T4 גדול ביותר. N0 מסמל מצב בו אין בלוטות לימפה מוגדלות וככל שעולה שלב ה-N כך מתרבות הבלוטות החשודות בצוואר כאשר ב-N3 ישנן בלוטות חשודות רבות בשני צידי הצוואר. M0 מתייחס לגידול ללא גרורות מרוחקות בעוד ב-M1 נמצאו אצל החולה גרורות (בדרך כלל בריאות).
טיפול[עריכת קוד מקור | עריכה]
קביעת סוג הטיפול תלויה במיקום הגידול, סוגו והשלב בו הוא נמצא. הטיפול עשוי להיות ניתוחי, כימותרפי, הקרנתי, ביולוגי או שילוב של אלו. בגידולים קטנים ובשלב מחלה התחלתי ניתן בדרך כלל לטפל בניתוח או בהקרנות כטיפול יחיד. בגידולים מתקדמים יידרש שילוב במספר שיטות.
- הקרנות - הטיפול הוא מקומי והקרינה מכוונת לגידול ולרקמות סביבו.
- טיפול ניתוחי - בגידולים ראשוניים וקטנים מבוצעת כריתה על ידי לייזר של הגידול וסביבתו. הניתוח מתבצע בהרדמה כללית דרך הפה, והחולה משתחרר בדרך כלל כעבור יממה לביתו עם הגבלות מינימליות. בגידולים מתקדמים לעיתים תידרש כריתה שלמה של הגרון עם הסרה של הבלוטות הצוואריות החשודות לגרורות מקומיות של המחלה.
- כימותרפיה - התרופות הכימותרפיות לסרטן הגרון ניתנות בדרך כלל בהזרקה ישירה למחזור הדם ומשם מגיעות אל כל הגוף. הטיפול הכימותרפי בסרטן הגרון ניתן בדרך כלל בשילוב עם הטיפול הקרינתי.
- ביולוגי - שימוש בנוגדנים מעכבי גדילה כנגד תאי הגידול הסרטני. ישנן כיום מספר תרופות המבוססות על תקיפה ביולוגית של הגידול (כגון נוגדן נגד רצפטור הגדילה של הגידול) ותרופות אלו מהוות תחליף או תוספת לטיפול הכימותרפי במחלה.
בקביעת סוג הטיפול נלקחים בחשבון גם משתנים נוספים כגון בקשות המטופל, מצבו הסוציאלי, מוכנות היענותו לסוג הטיפול, כמו גם ניסיון והעדפות המרכז הרפואי המטפל.
הטיפול האידיאלי עבור קרצינומות גרון בשלב 1–2 הוא הקרנות או טכניקות כירורגיות (אנדוסקופיה או ניתוח פתוח) המשמר פעילות לרינגיאלית תקינה. עבור קרצינומות פולשניות של הגלוטיס או של הסופרה-גלוטיס, בשלבי מחלה מוקדמים, מומלץ לטפל באמצעות הסרה כירורגית אנדוסקופית או באמצעות הקרנות (שתי השיטות יעילות באותה מידה ומניבות תוצאות דומות). טיפול בנגעים מסוימים שעדיין נמצאים בשלבים המוקדמים של המחלה עלול להיות כרוך בכריתה חלקית של מיתרי הקול.
בשלבים המאוחרים יותר של המחלה (שלבים 3–4), פרוטוקול הטיפול משלב הקרנות וטיפול כימותרפי (cisplatinum and fluorouracil). למרות שהשימוש בטיפול זה הולך וגובר, הצורך בניתוח להסרת מיתרי הקול עדיין נותר תדיר. הטיפול הראשוני היעיל ביותר בחולה במצב חמור עלול להיות כרוך בכריתה חלקית או מלאה של מיתרי הקול (laryngectomy).
אופציית הניתוח כטיפול ראשון מיועדת לחולים בהם נפח התפשטות סרטן הגרון גדול, חולים בשלב T4a, או חולים הצפויים לפתח בעיות תפקודיות כתוצאה מהמחלה.
גם אחר כריתת גרון ניתן כיום להחדיר תותב דיבור (שמתבצע בדרך כלל תוך כדי הניתוח לכריתת הגרון) שמאפשר לחולה דיבור ברמה ועוצמה מצוינים כבר עם שחרורו מהמחלקה. יש לציין שאכילה ובליעה יהיו תקינים וללא כל מגבלות אחר כריתת גרון מלאה.
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- סקירה רפואית מקיפה של המחלה באנגלית רפואית באתר eMedicine
- קביעת שלב המחלה באתר אנציקלופדיית האונקולוגיה
- סרטן הגרון באתר האגודה למלחמה בסרטן
- מניעה ואבחון מוקדם של סרטן הגרון באתר מרפאת א.ר.ם
- על אבחון וטיפול בסרטן הגרון בעקבות מותו של ספי ריבלין מהמחלה באתר דוקטורז, 05.12.13
- עופר מאיר, מותה של יהודית נאות: על סרטן הגרון, באתר ynet, 16 בדצמבר 2004
- חוקרים: מין אוראלי הוא הגורם המוביל לסרטן הלוע, באתר וואלה, 21 בפברואר 2011
- סרטן הגרון באתר בית החולים רמב"ם
- סרטן הגרון, באתר אנציקלופדיה בריטניקה (באנגלית)
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.
