אבולוציה של חיידקים – הבדלי גרסאות
| שורה 88: | שורה 88: | ||
== אבולוציה של חיידקים פתוגניים וקומנסלים == |
== אבולוציה של חיידקים פתוגניים וקומנסלים == |
||
תהליך ההסתגלות של חיידקים |
תהליך ההסתגלות של חיידקים [[פתוגניות|פתוגני]]<nowiki/>ים ו[[קומנסל|קומנסלי]]<nowiki/>ם לפונדקאי הוא תהליך אבולוציוני.<ref>{{צ-מאמר|מחבר=Kimberly A. Bliven, Anthony T. Maurelli|שם=Evolution of Bacterial Pathogens Within the Human Host|כתב עת=Microbiology Spectrum|כרך=4|שנת הוצאה=2016-01-29|doi=10.1128/microbiolspec.VMBF-0017-2015|קישור=https://journals.asm.org/doi/10.1128/microbiolspec.VMBF-0017-2015}}</ref> פונדקאות לחיידקים [[קומנסליזם|קומנסלי]]<nowiki/>ם ופתוגנים קיימים בצומח ובחי. חיידקים פתוגניים מקבוצות שונות עברו תהליכי הסתגלות מטבולית ברקמות האורגניזם, תוך פיתוח יכולות הצמדות, פולשנות והתרבות, התמודדות עם תהליכים דלקתיים והמערכת החיסונית, התמודדות עם החשיפה לתרופות אנטי-בקטריאליות ותחרותיות עם הפלורה הטבעית הקומנסלית. חיידקים פתוגניים בגוף המאחסן נחשפים למכלול תנאי מחיה סלקטיביים, תנאים המעודדים התפתחות של תכונות של היווצרות זנים אלימים {{אנג|virulence}}. לחיידקים יתרון בכך שהם יכולים לבצע העברת תכונות גנטיות רוחבית {{אנג|horizontal gene transfer}} (HGT).<ref>{{צ-מאמר|מחבר=Sandrine Borgeaud, Lisa C. Metzger, Tiziana Scrignari, Melanie Blokesch|שם=The type VI secretion system of Vibrio cholerae fosters horizontal gene transfer|כתב עת=Science|כרך=347|שנת הוצאה=2015-01-02|עמ=63–67|doi=10.1126/science.1260064|קישור=https://www.science.org/doi/10.1126/science.1260064}}</ref> חיידקים קומנסלים הבונים את הפלורה הטבעית של האורגניזם אינם מזיקים לפונדקאי. הם עוברים שינויים המאפשרים להם להתקים בסביבה ייחודיות. לדוגמא, הסתגלות חיידקי ה[[מיקרוביוטה]] של דרכי העיכול למלחי מרה<ref>{{צ-מאמר|מחבר=Verónica Urdaneta, Josep Casadesús|שם=Interactions between Bacteria and Bile Salts in the Gastrointestinal and Hepatobiliary Tracts|כתב עת=Frontiers in Medicine|כרך=4|שנת הוצאה=2017-10-03|doi=10.3389/fmed.2017.00163|קישור=http://journal.frontiersin.org/article/10.3389/fmed.2017.00163/full}}</ref> , הסתגלות של מיקרוביוטה של [[לחמית]] העינים ל[[ליזוזים]] |
||
, |
|||
== ראו גם == |
== ראו גם == |
||
גרסה מ־17:43, 21 ביוני 2023
הערך נמצא בשלבי עבודה: כדי למנוע התנגשויות עריכה ועבודה כפולה, אתם מתבקשים שלא לערוך את הערך בטרם תוסר ההודעה הזו, אלא אם כן תיאמתם זאת עם מניח התבנית.
| ||
| הערך נמצא בשלבי עבודה: כדי למנוע התנגשויות עריכה ועבודה כפולה, אתם מתבקשים שלא לערוך את הערך בטרם תוסר ההודעה הזו, אלא אם כן תיאמתם זאת עם מניח התבנית. | |

התהליך האבולוציוני של חיידקים הוא תהליך של שינויים תורשתיים באוכלוסיות במשך דורות רבים כתוצאה מברירה טבעית ומשינויים גנטיים עקב שני תהליכים: הסתגלותם של החיידקים לסביבה, ועמידותו החיסונית (אנ') של האורגניזם המאחסן.[1] התהליך האבולוציוני של חיידקים מתפרס על ציר זמן של כ-4 מיליארד שנים. החיידקים מצטיינים בשתי תכונות עיקריות המאפשרות תהליכי אבולוציה מהירים: זמני חלוקה קצרים בהתרבות אל-מינית (אנ'), ואוכלוסיות גדולות מאד.[2]
התהליך האבולוציוני החל מהתקופה הפרקמבריאנית. האב הקדמון של היצורים החיים התפצל לשלוש על-ממלכות: הארכאה (Archaea) והבקטריה (Bacteria), השייכות לפרוקריוטים. אליהם משתייכים מיקרואורגניזמים חד-תאיים, חסרי גרעין התא. החומר התורשתי
בהם מאורגן כרצועה בודדת של DNA הקרויה נוקלאואיד. העל-ממלכה השלישית בשם איקריוטים (Eukaryote)[3] התפתחה מאוחר יותר. בעלי-החיים המשתייכים לעל-ממלכה זו הם בעלי חומר תורשתי מאורגן בכרומוסומים בעלי סליל כפול. החומר התורשתי מאורגן בגרעין תא, אברון עטוף בממברנה המפרידה בינו לבין הציטופלסמה. חיידקי הארכאה והבקטריה, מאכלסים סביבות מחיה שונות ומגוונות מבחינה כימית ופיסיקלית, המעניקות הזדמנויות אבולוציוניות שונות.


תהליך האבולוציה של החיידקים התרחש משך ביליוני שנים, החל מהעידן הפרקמבריוני. ההתפצלות הראשונית בין שתי העל-ממלכות הארכאה והבקטריה התחוללה כנראה לפני 3.5 מיליארד שנים,[4] כפי שמצביעים מחקרים בשיטות ביומולקולריות של נוקלאואידים שנועדו לשחזר את המוצא הפילוגנטי של החיידקים.[5]
התאוריות הקשורות למקורות המוצא של חיידקים מתבססות על ממצאים ממקורות שונים. חוקרים מארצות הברית ויפן ביצעו בדיקות סריקה אופטיות במיקרוסקופ אלקטרונים וגילו מיקרופלנקטון על מאובנים מיקרופוסיליים (microfossil) באוסטרליה המערבית, באזור שגילו בן 3.4 מיליארד שנים המצוי ליד מקורות מים תרמיים (אנ')[6] המכילים ריכוזים גבוהים של כימיקלים מן הקרקע. ייתכן שהמים התרמיים מהווים את הסביבה הראשונית להתפתחות יצורים חיים על פני האדמה.
אנליזת איזוטופים של סלעים עתיקים מגלות שהחמצן הופיע על פני כדור הארץ כבר לפני 2.45 מיליארד שנים.[7] האבולוציה של החיידקים, בדומה לאבולוציה של אורגניזמים אחרים, מתבססת על ברירה טבעית של תכונות מעודדות חיים. רוב החיידקים מתרבים בתנאים אופטימליים בקצב של 20 עד 30 דקות לחלוקה. תהליך ההתרבות של חיידקים הוא לרוב תהליך אל-זוויגית, על ידי חלוקת תא האם לשני תאי בת הזהים בתכונותיהם הגנטיות לתא האם. בחיידקים קיימת גם רבייה זוויגית פחות נפוצה שבה מתחולל שילוב המטענים הגנטיים של של שני ההורים בתא הבת. הן ברבייה הזוויגית והן ברבייה האל-זוויגית מועבר החומר הגנטי מדור לדור בהעברה אנכית (Vertical transmission).
בעל-ממלכת הפרוקריוט קיימת גם העברה גנטית אופקית (horizontal transfer) של חומר גנטי מתא אחד לתא שני באוכלוסויות מעורבות של אורגניזמים ממוצא שונה.[8] תהליך הרבייה האופקית מתרחש בשלושה מסלולים אפשריים: התמרה, טרנספורמציה וקוניוגציה המאפשרות העברת התכונות הגנטיות לדור הבא ממקורות מרוחקים.[9] ההעברה הגנטית האופקית הינה ייחודית לפרוקריוטה.
החיידקים מסוגלים לפתח סתגלנות לתנאי קיצון המכונה אקסטרמופילית עקב חשיפה ממושכת לתנאי מחייה קיצוניים. בקצב חלוקה מהיר של חיידקים המתרחשת כל 20-30 דקות, מתאפשרת העברת חומר גנטי מהיר. באוכלוסיית חיידקים גדולה ימצאו חיידקים בעלי כושר הסתגלות משופרת לשינויים בסביבת המחיה כתוצאה משינויים גנטיים וחיידקים אלה ישרדו וישתלטו על שאר האוכלוסייה, ויהיו גם כאלה שהשינוי הגנטי יקשה על הסתגלותם והם ייעלמו.
חקר האבולוציה של החיידקים התבסס בתחילתו על מספר מאפיינים: המורפולוגיה של החיידקים ומושבותיהם על מצעי גידול מוצקים והתכונות הפיזיולוגיות. [10] הטקסונומיה המודרנית לחקר האבולוציה מתבססת על שיטות ביומולקולריות (biomelecular)[11] על ידי שימוש במקטע מוגדר של RNA ריבוזומלי המכונה (16S Ribosomal RNA) [12] המשמש לזיהוי ומיון קבוצת על-ממלכת הפרוקריוטה בסבירות של 98.5%.[13]
ההנחה הרווחת כיום היא כי בראשית האבולוציה, לפני 3.5 מיליארד שנים, האטמוספירה על פני כדור הארץ הייתה נטולת חמצן ואפשרה התפתחות חיידקים אל-אווירניים, תרמופילים(Termophiles) - חיידקים עמידים לטמפרטורות גבוהות, שהיו זקוקים למים כדי לבצע ראקציות כימיות. החיידקים הראשונים היו אוטוטרופיים (בעלי יכולת ליצור חומרים אורגניים מחומרים אי-אורגניים), גז מתאן CH4 שימשש להם כמקור לפחמן אורגני,[14] והידרותרמליים (Hydrothermal vent microbial communities)

טולרנטיות לסביבה והסתגלות לתנאי קיצון
התהליכים האבולוציונים של החיידקים על פני כדור הארץ התאפשרו הודות להיותם סתגלנים. מספר החיידקים על פני כדור הארץ עולה על זה של כל שאר היצורים גם יחד.[15] התפתחות תכונת הטולרנטיות (Tolerance)[16] המיקרוביאלית ותכונת האקסטרמופיליות (Extremophile) היא תהליך אבולוציוני הישרדותי של אוכלוסיות חיידקים שהתפתח בעקבות חשיפה ממושכת לגורמים פיזיקליים וכימיים השונים במהותם באופן קיצוני מתנאי המחיה האופטימליים. הביטוי למידת ההסתגלות לתנאים קיצוניים נעשה בשתי דרגות: דרגת הטולרנתיות (tolerance) היא דרגה שבה האורגניזם מסוגל להתקיים הן בתנאים אופטימליים למחייה והן בתנאים קיצוניים. בדרגת הסתגלות גבוהה יותר נעשה שימוש בסיומת המילה phile שפירושו בלטינית אוהב, במצב שבו המיקרואורגניזם פיתח הסתגלות פיזיולוגית לתנאי קיצון עד כדי תלות, כך שאין ביכולתו לחיות בתנאי המחיה האופטימליים הראשוניים.
ההתפתחות הטכנולוגית המואצת במאה האחרונה הובילה לחשיפה רב-גונית ממושכת של אוכלוסיות חיידקים לתנאי עקה וחשיפה לחומרים זרים לסביבה הקרויה סביבה קסנונוביוטית (Xenobiotic) בתעשייתיות שונות. שינויים טכנולוגיים מזורזים רבים גורמים לחשיפת אוכלוסיות מעורבות של חיידקים לחומרים כימיים חדשים: תעשיות המזון, הנייר, הקוסמטיקה והתרופות. בשנים האחרונות אנו עדים לפיתוח מואץ של תהליכים טכנולוגיים לטיפול במי-שתייה למיגור מיקרואורגניזמים פתוגניים,[17] טיפולים במי-שפכים ומחזור מים לחקלאות.[18][19] פיתוח שימושים נרחבים לחומרי הדברה חדשניים[20] בחקלאות המודרנית השפיעו משמעותית על הרכב אוכלוסיות המיקרואורגניזמים הפתוגניים. התפתחות הרפואה המודרנית גרמה לחשיפות אינטנסיביות של אוכלוסיות חיידקים מעורבות לחומרים אנטימיקרוביאליים במערכות שונות, כמו בתי-חולים[21], מכוני מחקר, ווטרינריה[22], תעשיית התרופות[23][24] והקוסמטיקה, החקלאות והמזון[25] המובילה לשינויים מואצים של אוכלוסיית הפלורה הטבעית וחיידקים פתוגניים.[26]
תרמוטולרנטיות ותרמופיליות
חיידקים תרמופיליים ותרמוטולרנטים שייכים מבחינה אבולוציונית לעל-ממלכת הארכאה ולעל-ממלכת הבקטריה. תרמוטולרנתיות (אנ') היא תכונה של חיידקים הגדלים באופן אופטימלי בטמפרטורות גדילה של חיידקים מזופיליים (אנ') בטווח טמפרטורות 20-45oC,[27] אך יכולים להתקיים גם בטמפרטורות גבוהות יותר שבין 45-55oC, כתוצאה מחשיפה ממושכת לטמפרטורות גבוהות ובינוניות המתבקשת בתעשיות שונות בהם מעורבים תהליכים ממושכים בהם מעורבים מים.[28][29] הוכח שכתוצאה מתהליכים ממושכים אלה, הפלורה המיקרוביאלית עוברת שינויים גנטיים המובילים לשינויים מבניים, המאפשרים תפקוד בטמפרטורות גבוהות יותר מחיידקים מזופילים.
תרמופיליות היא תכונה של חיידקים החיים באופן אופטימלי בטמפרטורות של 41-122oC.
פסיכרוטרופיות ופסיכרופיליות
80% מכדור הארץ מורכבים ממים, 70% הם מי-אוקינוס והשאר הם שטחי הקרח של הקוטב הצפוני והקוטב הדרומי. אוכלוסית החיידקים אוהבי הקור היא האוכלוסיה הנפוצה ביותר על פני כדור הארץ.[30][31] חיידקים פסיכרוטרופיים (Psychrotrofic bacteria)ופסיכרופיליים (Psychrophile) [32] הם חיידקים חובבי קור. הטמפרטורה האופטימלית לצמיחתם היא 15oC-0oC.[33] באזורי הקוטב והטונדרה נמצאו גם חיידקים שגדלים בטמפרטורה של 5oC-. רוב החיידקים הפסיכרופיליים עמידים לקיפאון. חיידקים פסיכרופילים רבים עמידים אף לטמפרטורות נמוכות יותר, ורובם משתיכים לקבוצת האקסטרמופילים בהיותם עמידים לא רק לטמפרטורות נמוכות אלא גם לקרינה רדיואקטיבית, קרני UV, יובש, לחץ אוסמוטי גבוה, pH גבוה או נמוך, מקורות מזון דלים[34]. התהליך האבולוציוני של חיידקים אלה מתבטא בהתפתחות של אנזימים פעילים בתנאי קור. בחיידקים עמידים לקור התפתחו חלבונים המגינים עליו כנגד קפיאה (Cryoprotectants), ושינויים משמעותיים במבנה קרום התא [35].
פיתוח של טכנולוגיות שונות לעיבוד מזון תוך חשיפה ממושכת לקור כגון, תעשיית החלב אפשרה התפתחותם של חיידקים פסיכרוטרופיים נפוצים מאוד בחלב קר לפני פסטור ומשתייכים לקבוצות הקוליפורמים,Micrococcus, Bacillus, Staphylococcus, Pseudomonas Flavobacterium. הם מפתחים אנזימים פרוטאוליטים וליפוליטיים (אנ') הגורמים לקלקול החלב ומוצריו גם בתנאי קור.[36]
מתאנוטרופים
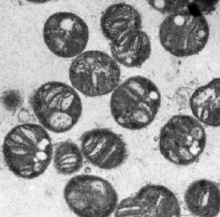

חיידקים מתאנוטרופיים הם חיידקים השייכים לעל-ממלכה Archaea ולממלכת Bacteria, המשתמשים במתאן כמקור לאנרגיה. החיידקים המתאנוטרופים מתחלקים למתאנוטרופים אובליגטורים (אנ') הזקוקים למתאן כמקור בלעדי לפחמן, ומתאנוטרופים פקולטטיביים,[37] שיכולים להשתמש גם במקורות פחמן אחרים מלבד המתאן.[38] החיידקים המתאנוטרופים נפוצים מאוד בטבע באזורים חקלאיים,[39] וגזעים רבים של חיידקים מתאנוטרופים הם גם טרמוטולרנטים (אנ'),[40] עובדה המעידה על הופעתם היחסית מוקדמת על פני כדור הארץ. חלקם הם אווירניים אובליגטורים וחלקם הם מיקרואארופילים או אל-אווירניים אובליגטורים, ומשתמשים בחומרים כימיים שונים כתורמי אלקטרונים. בנוסף להיותם אל-אווירניים, חיידקים אלה גם עמידים לטווח pH רחב, של 1–8 ותרמוטולרנתי (עד 50oC).

הלוטולרנתיות והלופיליות
ההלוטולרנתיות Halotolerance (אנ') וההלופיליות (אנ') מבטאות עמידות לריכוזי מלח גבוהים. ריכוז של 0.9% מלח בישול הקרוי גם סלין (אנ') נחשב לריכוז האופטימלי- איזוטוני לרוב החיידקים. בריכוז זה בו נשמר הלחץ האוסמוטי תקין עבור מרבית החיידקים.
חיידקים הלוטולרנתים הם חיידקים שמסוגלים להתקיים בריכוזי מלח מעל הריכוז האיזוטוני של 0.9% ועד 2.5%.
חיידקים הלופיליים בעלי יכולת גדילה בריכוז מלח בישול NaCl מעל ל-2.5%. באזורים גאוגרפיים מלוחים בצ'ילה, בודד החיידק Exiguobacterium השייך לעל-ממלכת ארכיאה, שהסתגל לסביבה עם ערך Aw- (פעילות-מים) (אנ') נמוך בגלל ריכוזי מלח גבוהים.[41] באזור צחיח זה, המצוי בגובה 3,600 מטר, יש לא רק ריכוזים גבוהים של מלח בקרקע אלא גם קרינת UV חזקה ולכן מוגדר כחיידק אקסטרמופילי.[42]
אוסמוטולרנטיות, אוסמופיליות וקסרופיליות
חיידקים הגדלים בסביבה שבה הלחץ האוסמוטי גבוה, למשל בריכוזי סוכר גבוהים, נקראים אוסמופילים (אנ'). בתא החיידק קיימים תהליכים של אוסמורגולציה (אנ'), המאפשרים לתא להסתגל לשינויים אוסמותיים סביבתיים. דופן התא מעניק לחיידק יכולת עמידה בפני שינויים אוסמוטיים כתוצאה משינוי ריכוזי חומרים מומסים בסביבה המימית החיצונית של התא, כגון, סביבה נוכחות סוכרים או מלח בישול ושינויים שינויים בריכוז המים החופשיים עקב שימוש בטכנולוגיות שונות.
קסרופילים (אנ') הם חיידקים הגדלים בסביבה דלת מים עד כדי יובש קיצוני.

אקסטרמופילים (בעברית חיידקים קיצונאיים) הם מיני חיידקים המסוגלים לשרוד בתנאים קשים במיוחד (חום גבוה, קור, חומציות גבוהה, חשיפה לקרינה, דוגמת ה-Deinococcus radiodurans, נקד גרם חיובי, בעל דופן תא עבה במיוחד, עמידה בתנאי לחץ קשים ועמידה בפני קרינה ונחשב לאקסטרמופיל-על.[43] עמידותם הרבה של חיידקים אקסטרמופילים לתנאי קיצון רבים נושאת בחובה את יכולת עמידותם לתנאים הקיצוניים, כגון, טמפרטורות גבוהות מאוד או נמוכות מאד, צחיחות וגם אוקיינוסים, סביבה מחזרת, עטירה בגאז המתאן וחסרת חמצן, ריכוזים גבוהים של יסודות ומלחים אך מחסור בחומרים אורגניים, קרינה אולטרה סגולית ורדיואקטיבית, כפי שהיה קיים על פני כדור הארץ בתקופות אבולוציוניות קדומות.
טרמוטוגאטה

הטרמוטוגטה (אנ') הם מתגים גראם שליליים, תרמופיליים, והיפרתרמופיליים (אנ') החיים בטמפרטורות בין 55-85oC ו ובין 85-113oC בהתאם. בין החיידקים היפרתרמופילים קיימים גם מינים חובבי טמפרטורות גבוהות במיוחד, חלק מהמינים התרמופילים מתרבים בצורה אידיאלית אפילו מעל 100oC ויכולים לשרוד בטמפרטורה של עד 121oC.
על פי מחקרים המבוססים על ביולוגיה מולקולרית, הטרמוטוגאטה התפתחו לפני 3.2 מיליארד שנים. הוא מיצג כיום את מרבית החיידקים ההיפתרמופילים הקיימים על פני כדור הארץ.
סידרת הטרמוטוגטה התפצלה לשני סוגים: Thermotogaceae ו-Fervidobacteriaceae. לחיידקים מקבוצה זו יש מעטפת ממברנלית ייחודית המורכבת מליפידים בשם "טוגה". הייחודיות שלה לא רק בצורתה ובהרכבה אלא גם ביכולתה להתפתח גם בפאזה הסטאציונרית (אנ') של החיידקים.[44]
ציאנובקטריה - Cyanobacteria

חוקרים מארצות הברית ויפן מומחים לחקר מיקרו מאובנים (אנ') גילו שרידים של חיידקי הציאנובקטריה על סלעים במרכז אוסטרליה.[45] המבנים המיקרוביאליים שרדו בגלל משקעי סידן פחמתי CaCO3 במבנה קפסולרי ששמר על צורת חיידקי הציאנובקטריה (הכחוליות) שהם חיידקים גראם שליליים, מכילי כלורופיל המאורגן בדיסקים הקרויים טילקואידים (אנ').[46] הם מתקיימים במימי האוקיינוסים ושייכים לקבוצת החיידקים הפוטואוטוטרופיים (אנ'), מקבעי חנקן (אנ'), דהיינו, מנצלים את אנרגיית השמש כדי להתקיים. חיידקים אלה הופיעו על פני כדור הארץ לפני 2.7-2.3 מיליארד שנה, בעת המאורע המשמעותי של העשרת האטמוספירה בריכוזי חמצן גבוהים הקרוי "אירוע החמצן הגדול"Great Oxygen Event-GOE (אנ'). האירוע זה מכונה גם "אסון החמצן" מפני שהוא הוביל להכחדה המונית של יצורים חיים אל-אווירנים שהתפתחו בתקופה שבה לא היה חמצן באטמוספירה על פני כדור הארץ, וליצירת מערכת אקולוגית חדשה ולזירוז האבולוציה לכיוון האווירני[47] הקיים עד עצם היום הזה.
מחקרים מודרניים בשיטות ביומולקולרית (אנ') מראים כי בנוסף לקבוצת הציאנובקטריה הייתה קיימת קבוצה נוספת של חיידקים בשם Melainabacteria (אנ') שתכונותיה דומות מאוד לקבוצת הציאנובקטריה, אולם ללא יכולת לבצע פוטוסינתזה. מדענים משערים ששתי הקבוצות התפתחו מקבוצת חיידקים קדומה יותר בשם Sericytochromatia.[48] הקבוצות ציאנובקטריה ומלאינבקטריה קרובות מאוד מבחינה גנטית מלבד אי היכולת לבצע פוטוסינתזה באחת הקבוצות. שתי הקבוצות נפוצות באזורים נרחבים על פני כדור הארץ בתנאי מחיה מגוונים: אזורי קרח ואזוים מדבריים, אזורי מים מתוקים ומי-אוקיינוס.
מדענים משערים שהציאנובקטריה הם המקור האבולוציוני להתהוות הכלורופלסטים בעל ממלכת האאוקריוטה באמצעות תהליך הקרוי אנדוסימביוזה,[49] תהליך שבו תאי ציאנובקטריה שהכילו טילקואידים נבלעו על ידי תאים פרוקריטים אחרים והוטמעו באופן קבוע בתאים הפרוקריוטים. צברי הטילקואידים שנבלעו היו המוצא להיווצרות הכלורופלסטים ביצורים האאוקריוטים הראשונים בעל-ממלכת הפרוטיסטה.
Pseudomonadales

עליית ריכוז החמצן באטמוספירה הובילה להתפתחות סדרת ה- הפסאודומונדלס Pseudomonadales (אנ'). בקבוצה זו כלולים חיידקים מקבעי חנקן(אנ'), כגון חיידק ה- Azotobacter,[50][51] חיידקים פתוגניים, כגון Pseudomonas aeruginosa חיידק פתוגני אופורטוניסטי (אנ'), וחיידקים כמואוטוטרופיים Chemoautotrophs ההופכים את דו-תחמוצת הפחמן לפחמן אורגני ומפיקים אנרגיה מתרכובות אי-אורגניות: ברזל, גופרית ומימן גופריתי. משערים שקבוצה זו התפתחה לפני כ-1.5 מיליארד שנים, בתקופה הפלאופרוטרוזואית.[52]

עמידות לאנטיביוטיקה
אנטיביוטיקה היא קבוצת חומרים הפוגעים במנגנונים חיוניים לקיומם של חיידקים. האנטיביוטיקה שונים פוגעים ביצירת דופן תא החיידק, מעכבים סינתזה של DNA ו-RNA, מעכבים סינתזה של חומצה פולית, וחומצה מיקולית.[53] החומר האנטיביוטי הראשון, הפניצילין התגלה בשנות העשרים של המאה הקודמת על ידי אלכסנדר פלמינג, אולם ההתפתחות המשמעותית של עמידות חיידקים לאנטיביוטיקה החלה בתקופת מלחמת העולם השנייה, כאשר השימוש בחומרים אנטיבקטריאליים נעשה נרחב יותר ויותר, הן בטיפולים אמבולטורים והן בבתי חולים. אנטיביוטיקה פועלים באופנים שונים על סוגים שונים של חיידקים. חיידקים הגורמים לדלקות יוצרים ברקמות ביופילמים המגינים על אוכלוסיות החיידקים שבתוכו. הביופילמים מקשים על חדירת האנטיביוטיקה אל החיידקים גורמי הדלקת, ועל ידי כך מאפשר להם לשגשג ועל ידי כך לעבור מוטציות לעיתים קרובות. העמידות לאנטיביוטיקה מתפתחת על שני צירים: בציר האנכי היא פועלת על ידי תהליך של ברירה טבעית של מוטנטים עמידים. בציר האופקי היא פועלת על ידי העברת גנים של עמידות לאנטיביוטיקה מחיידקים עמידים לחיידקים רגישים.
על מנת להתגבר על האבולוציה המהירה של ריבוי הזנים העמידים, הרפואה משתמשת בשיטות טיפול שונות.[54][55][56]
אבולוציה של תהליך הספורולציה (יצירת נבגים)
הספורולציה (אנ') היא תהליך של יצירת נבגים על ידי חיידקים, עובשים וצמחים. בחיידקים זהו תהליך אבולוציוני למטרות הישרדות בו הופך חיידק ממצב ווגטטיבי למצב של תרדמת פיזיולוגית המאפשר עמידות בתנאי קיצון כגון, קור, חום קרינה, יובש ומחסור במקורות פחמן וחנקן, וכן עמידות לחומרים אנטיבקטריאליים. הספורולציה נחשבת לתהליך קדום מבחינה אבולוציונית[57] ונפוצה בחיידקי קרקע, בסביבה אקולוגית המתאפינת בשינויים בתנאי מזג אוויר קיצוניים בתדירויות גבוהות במעברים בין יום ללילה ובין עונות השנה. התופעה קיימת במתגים גראם-חיוביים בעלי יכולת ליצר אנדוספורה (אנ') אחת בכל תא וגטטיבי. בתהליך הספורולציה, תא וגטטיבי שמתקשה לשרוד בתנאי מחיה קשים, בייחוד בגלל מחסור בחומרי בנין, מתחלק לשניים ורק התא הקדמי יהפוך לאנדוספורה בתהליך ביולוגי ממושך של 6–10 שעות.[58]

אנדוספורות של חיידקי קרקע, כגון חיידקים השייכים לקלוסטרידיה שהם חיידקים אל-אווירניים ובצילוס שהם חיידקים אווירניים Clostridium spp ו- Bacillus spp מכילה עד 10% חומצה די-פיקולינית (אנ'), בעלת תפקיד משמעותי בעמידותה לטמפרטורות גבוהות. מחקרים הראו שאנדוספורות מסוגלות להיכנס לתרדמת למשך תקופות ארוכות מאוד של עשרות מיליוני שנים[59] ושתהליך הספורולציה הוא תהליך רברסיבילי. האנדוספורה היא הצורה הראשונית ביותר לאפשרות של שינוי מבנה מורפולוגי ופיזיולוגי של תא, הודות לרגולטור הגנטי DNA-binding protein Spo0A (DNA-binding protein Spo0A).[60]
אבולוציה של המיקופלסמה
מיקופלסמה הם חיידקים בעלי גנום קטן שאיבדו את דופן התא, ולכן מתקיימים בתוך אורגניזמים של בעלי חיים, חסרי יכולת לחדור לרקמות, בעלי יכולת להיספח לקרום התא. קיימות תאוריות לגבי מוצאם האבולוציוני. על פי תאוריה אחת מוצאם מחיידקים גראם חיוביים.[61] מבחינה אבולוציונית ההשערה היא שהתפתחו במקביל ללקטובצילים וסטרפטוקוקים.[62]
אבולוציה של חיידקים פתוגניים וקומנסלים
תהליך ההסתגלות של חיידקים פתוגניים וקומנסלים לפונדקאי הוא תהליך אבולוציוני.[63] פונדקאות לחיידקים קומנסלים ופתוגנים קיימים בצומח ובחי. חיידקים פתוגניים מקבוצות שונות עברו תהליכי הסתגלות מטבולית ברקמות האורגניזם, תוך פיתוח יכולות הצמדות, פולשנות והתרבות, התמודדות עם תהליכים דלקתיים והמערכת החיסונית, התמודדות עם החשיפה לתרופות אנטי-בקטריאליות ותחרותיות עם הפלורה הטבעית הקומנסלית. חיידקים פתוגניים בגוף המאחסן נחשפים למכלול תנאי מחיה סלקטיביים, תנאים המעודדים התפתחות של תכונות של היווצרות זנים אלימים (virulence). לחיידקים יתרון בכך שהם יכולים לבצע העברת תכונות גנטיות רוחבית (horizontal gene transfer) (HGT).[64] חיידקים קומנסלים הבונים את הפלורה הטבעית של האורגניזם אינם מזיקים לפונדקאי. הם עוברים שינויים המאפשרים להם להתקים בסביבה ייחודיות. לדוגמא, הסתגלות חיידקי המיקרוביוטה של דרכי העיכול למלחי מרה[65] , הסתגלות של מיקרוביוטה של לחמית העינים לליזוזים
,
ראו גם
קישורים חיצוניים
- הסבר על ציאנובקטריה, באתר TheBigger (באנגלית)
- טקסונומיה של ציאנובאקטריה, באתר Cyanosite (באנגלית)
הערות שוליים
- ^ Hafiz Ishfaq Ahmad, Abdul Jabbar, Nadia Mushtaq, Zainab Javed, Immune Tolerance vs. Immune Resistance: The Interaction Between Host and Pathogens in Infectious Diseases, Frontiers in Veterinary Science 9, 2022 doi: 10.3389/fvets.2022.827407/full
- ^ Bacterial evolution - Latest research and news | Nature, www.nature.com
- ^ C R Woese, O Kandler, M L Wheelis, Towards a natural system of organisms: proposal for the domains Archaea, Bacteria, and Eucarya., Proceedings of the National Academy of Sciences of the United States of America 87, 1990-06, עמ' 4576–4579
- ^ J R Brown, W F Doolittle, Archaea and the prokaryote-to-eukaryote transition, Microbiology and Molecular Biology Reviews 61, 1997-12, עמ' 456–502 doi: 10.1128/mmbr.61.4.456-502.1997
- ^ Fabia U Battistuzzi, Andreia Feijao, S Blair Hedges, [No title found], BMC Evolutionary Biology 4, 2004, עמ' 44 doi: 10.1186/1471-2148-4-44
- ^ Natali Anderson, 3 Billion Year Old Plankton Microfossils Found in Australia | Paleontology | Sci-News.com, Sci.News: Breaking Science News, 2013-06-07 (באנגלית אמריקאית)
- ^ the new york times, [the new york times oxygen a mystery easy to take for granted], https://www.nytimes.com/2013/10/03/science/earths-oxygen-a-mystery-easy-to-take-for-granted.html.
- ^ Howard Ochman, Jeffrey G. Lawrence, Eduardo A. Groisman, Lateral gene transfer and the nature of bacterial innovation, Nature 405, 2000-05, עמ' 299–304 doi: 10.1038/35012500
- ^ Conjugation, transformation & transduction | Bacteria (article), Khan Academy (באנגלית)
- ^ Keneth Todar, [kentodar@textbookofbacteriology.net Textbook of Bacteriology. "The Good, the Bad, and the Deadly"], https://textbookofbacteriology.net/procaryotes.html, 2015
- ^ Vaibhav Bhandari, Hafiz S. Naushad, Radhey S. Gupta, Protein based molecular markers provide reliable means to understand prokaryotic phylogeny and support Darwinian mode of evolution, Frontiers in Cellular and Infection Microbiology 2, 2012 doi: 10.3389/fcimb.2012.00098
- ^ 16S Ribosomal RNA - an overview | ScienceDirect Topics, www.sciencedirect.com
- ^ Aharon Oren, George M.YR 2021 Garrity, Valid publication of the names of forty-two phyla of prokaryotes, International Journal of Systematic and Evolutionary Microbiology 71, עמ' 005056 doi: 10.1099/ijsem.0.005056
- ^ Filipa L. Sousa, Shijulal Nelson-Sathi, William F. Martin, One step beyond a ribosome: The ancient anaerobic core, Biochimica et Biophysica Acta (BBA) - Bioenergetics 1857, 2016-08, עמ' 1027–1038 doi: 10.1016/j.bbabio.2016.04.284
- ^ Nancy Merino, Heidi S. Aronson, Diana P. Bojanova, Jayme Feyhl-Buska, Michael L. Wong, Shu Zhang, Donato Giovannelli, Living at the Extremes: Extremophiles and the Limits of Life in a Planetary Context, Frontiers in Microbiology 10, 2019 doi: 10.3389/fmicb.2019.00780/full
- ^ The Procaryotes, textbookofbacteriology.net
- ^ Martins A. Adefisoye, Ademola O. Olaniran, Does Chlorination Promote Antimicrobial Resistance in Waterborne Pathogens? Mechanistic Insight into Co-Resistance and Its Implication for Public Health, Antibiotics 11, 2022-05, עמ' 564 doi: 10.3390/antibiotics11050564
- ^ Barbara Drigo, Gianluca Brunetti, Samuel C. Aleer, Jan M. Bell, Michael D. Short, Sotirios Vasileiadis, John Turnidge, Paul Monis, David Cunliffe, Erica Donner, Inactivation, removal, and regrowth potential of opportunistic pathogens and antimicrobial resistance genes in recycled water systems, Water Research 201, 2021-08-01, עמ' 117324 doi: 10.1016/j.watres.2021.117324
- ^ Benjamin Piña, Josep M. Bayona, Anastasis Christou, Despo Fatta-Kassinos, Emmanuel Guillon, Dimitra Lambropoulou, Costas Michael, Fabio Polesel, Stéphanie Sayen, On the contribution of reclaimed wastewater irrigation to the potential exposure of humans to antibiotics, antibiotic resistant bacteria and antibiotic resistance genes – NEREUS COST Action ES1403 position paper, Journal of Environmental Chemical Engineering 8, 2020-02-01, עמ' 102131 doi: 10.1016/j.jece.2018.01.011
- ^ Diederik van der Hoeven, Pesticide resistance, a growing problem, Bio Based Press, 2019-09-03 (באנגלית אמריקאית)
- ^ Teresa M. Coque, Rafael Cantón, Ana Elena Pérez-Cobas, Miguel D. Fernández-de-Bobadilla, Fernando Baquero, Antimicrobial Resistance in the Global Health Network: Known Unknowns and Challenges for Efficient Responses in the 21st Century, Microorganisms 11, 2023-04, עמ' 1050 doi: 10.3390/microorganisms11041050
- ^ Ernesto Palma, Bruno Tilocca, Paola Roncada, Antimicrobial Resistance in Veterinary Medicine: An Overview, International Journal of Molecular Sciences 21, 2020-03-11, עמ' 1914 doi: 10.3390/ijms21061914
- ^ Firzan Nainu, Andi Dian Permana, Nana Juniarti Natsir Djide, Qonita Kurnia Anjani, Rifka Nurul Utami, Nur Rahma Rumata, Jianye Zhang, Talha Bin Emran, Jesus Simal-Gandara, Pharmaceutical Approaches on Antimicrobial Resistance: Prospects and Challenges, Antibiotics 10, 2021-08-14, עמ' 981 doi: 10.3390/antibiotics10080981
- ^ Leyla Tahrani, Leila Soufi, Ines Mehri, Afef Najjari, Abdenaceur Hassan, Joris Van Loco, Tim Reyns, Ameur Cherif, Hedi Ben Mansour, Isolation and characterization of antibiotic-resistant bacteria from pharmaceutical industrial wastewaters, Microbial Pathogenesis 89, 2015-12-01, עמ' 54–61 doi: 10.1016/j.micpath.2015.09.001
- ^ Mrinal Samtiya, Karl R. Matthews, Tejpal Dhewa, Anil Kumar Puniya, Antimicrobial Resistance in the Food Chain: Trends, Mechanisms, Pathways, and Possible Regulation Strategies, Foods 11, 2022-01, עמ' 2966 doi: 10.3390/foods11192966
- ^ Department of Health & Human Services, Antibiotic resistant bacteria, www.betterhealth.vic.gov.au (באנגלית)
- ^ mesophilic bacteria, www.owp.csus.edu
- ^ Thomas Rinsoz, Silvia Hilfiker, Anne Oppliger, Quantification of Thermotolerant Campylobacter in Swiss Water Treatment Plants, by Real-Time Quantitative Polymerase Chain Reaction, Water Environment Research 81, 2009-09, עמ' 929–933 doi: 10.2175/106143009X407429
- ^ Elayse M. Hachich, Marisa Di Bari, Ana Paula G. Christ, Cláudia C. Lamparelli, Comparison of thermotolerant coliforms and Escherichia coli densities in freshwater bodies, Brazilian Journal of Microbiology 43, 2012-06, עמ' 675–681 doi: 10.1590/S1517-83822012000200032
- ^ Pieter De Maayer, Dominique Anderson, Craig Cary, Don A Cowan, Some like it cold: understanding the survival strategies of psychrophiles, EMBO reports 15, 2014-05, עמ' 508–517 doi: 10.1002/embr.201338170
- ^ Jody W Deming, Psychrophiles and polar regions, Current Opinion in Microbiology 5, 2002-06, עמ' 301–309 doi: 10.1016/s1369-5274(02)00329-6
- ^ Craig L. Moyer, R. Eric Collins, Richard Y. Morita, Psychrophiles and Psychrotrophs, Elsevier, 2017-01-01, ISBN 978-0-12-809633-8. (באנגלית)
- ^ Richard Y. Morita, Craig L. Moyer, Psychrophiles, Waltham: Academic Press, 2001-01-01, עמ' 298–303, ISBN 978-0-12-384720-1. (באנגלית)
- ^ Pieter De Maayer, Dominique Anderson, Craig Cary, Don A Cowan, Some like it cold: understanding the survival strategies of psychrophiles, EMBO reports 15, 2014-05, עמ' 508–517 doi: 10.1002/embr.201338170
- ^ S. Shivaji, M. D. Kiran, S. Chintalapati, Perception and Transduction of Low Temperature in Bacteria, Washington, DC, USA: ASM Press, 2014-04-08, עמ' 194–207
- ^ Elionora Hantsis-Zacharov, Malka Halpern, Culturable Psychrotrophic Bacterial Communities in Raw Milk and Their Proteolytic and Lipolytic Traits, Applied and Environmental Microbiology 73, 2007-11-15, עמ' 7162–7168 doi: 10.1128/AEM.00866-07
- ^ Encyclopedia of Biological Chemistry II, ScienceDirect (באנגלית)
- ^ Ivica Tamas, Angela V. Smirnova, Zhiguo He, Peter F. Dunfield, The (d)evolution of methanotrophy in the Beijerinckiaceae—a comparative genomics analysis, The ISME Journal 8, 2014-02, עמ' 369–382 doi: 10.1038/ismej.2013.145
- ^ R S Hanson, T E Hanson, Methanotrophic bacteria, Microbiological Reviews 60, 1996-06, עמ' 439–471 doi: 10.1128/mr.60.2.439-471.1996
- ^ I. Yu. Oshkin, O. V. Danilova, R. Z. Suleimanov, E. N. Tikhonova, Thermotolerant Methanotrophic Bacteria from Sediments of the River Chernaya, Crimea, and Assessment of Their Growth Characteristics, Microbiology 90, 2021-09-01, עמ' 588–597 doi: 10.1134/S0026261721050131
- ^ Francisco Remonsellez, Juan Castro-Severyn, Coral Pardo-Esté, Pablo Aguilar, Characterization and Salt Response in Recurrent Halotolerant Exiguobacterium sp. SH31 Isolated From Sediments of Salar de Huasco, Chilean Altiplano, Frontiers in Microbiology 9, 2018 doi: 10.3389/fmicb.2018.02228/full
- ^ Yutian Feng, Uri Neri, Sean Gosselin, Artemis S Louyakis, The Evolutionary Origins of Extreme Halophilic Archaeal Lineages, Genome Biology and Evolution 13, 2021-08-03, עמ' evab166 doi: 10.1093/gbe/evab166
- ^ Extremophile | Definition, Types, Examples, & Facts | Britannica, www.britannica.com (באנגלית)
- ^ Chaman Ranjit, Kenneth M. Noll, Distension of the toga of Thermotoga maritima involves continued growth of the outer envelope as cells enter the stationary phase, FEMS microbiology letters 363, 2016-10, עמ' fnw218 doi: 10.1093/femsle/fnw218
- ^ Fossil Record of the Cyanobacteria, ucmp.berkeley.edu
- ^ Thylakoid | biology | Britannica, www.britannica.com (באנגלית)
- ^ D. J. De Marais, Evolution. When did photosynthesis emerge on Earth?, Science (New York, N.Y.) 289, 2000-09-08, עמ' 1703–1705
- ^ Marie-Eve Monchamp, Piet Spaak, Francesco Pomati, Long Term Diversity and Distribution of Non-photosynthetic Cyanobacteria in Peri-Alpine Lakes, Frontiers in Microbiology 9, 2019 doi: 10.3389/fmicb.2018.03344/full
- ^ Endosymbiotic theory - Definition and Examples - Biology Online Dictionary, Biology Articles, Tutorials & Dictionary Online, 2022-06-17 (באנגלית אמריקאית)
- ^ nitrogen-fixing bacteria | Definition & Types | Britannica, www.britannica.com (באנגלית)
- ^ השותפים השקטים של הצמחים, באתר השותפים השקטים של הצמחים, 2021-11-14
- ^ Palaeos Proterozoic: The Paleoproterozoic Era, palaeos.com
- ^ Antibiotic Classification & Mechanism - Basic Science - Orthobullets, www.orthobullets.com
- ^ Devon M Fitzgerald, The road to resistance, eLife 8, 2019-10-25, עמ' e52092 doi: 10.7554/eLife.52092
- ^ Julian Davies, Dorothy Davies, Origins and Evolution of Antibiotic Resistance, Microbiology and Molecular Biology Reviews 74, 2010-09, עמ' 417–433 doi: 10.1128/MMBR.00016-10
- ^ חיים בסרט: כך החיידקים מפתחים עמידות לאנטיביוטיקה, באתר חיים בסרט: כך החיידקים מפתחים עמידות לאנטיביוטיקה, 2016-09-09
- ^ Elitza I. Tocheva, Davi R. Ortega, Grant J. Jensen, Sporulation, bacterial cell envelopes and the origin of life, Nature Reviews Microbiology 14, 2016-08, עמ' 535–542 doi: 10.1038/nrmicro.2016.85
- ^ Michiel J.L. de Hoon, Patrick Eichenberger, Dennis Vitkup, Hierarchical Evolution of the Bacterial Sporulation Network, Current Biology 20, 2010-09, עמ' R735–R745 doi: 10.1016/j.cub.2010.06.031
- ^ R. Cano, M. Borucki, Revival and identification of bacterial spores in 25- to 40-million-year-old Dominican amber, Science 268, 1995-05-19, עמ' 1060–1064 doi: 10.1126/science.7538699
- ^ Virginie Molle, Masaya Fujita, Shane T. Jensen, Patrick Eichenberger, José E. González-Pastor, Jun S. Liu, Richard Losick, The Spo0A regulon of Bacillus subtilis: The Spo0A regulon, Molecular Microbiology 50, 2003-11-11, עמ' 1683–1701 doi: 10.1046/j.1365-2958.2003.03818.x
- ^ Todd L. Sladek, A hypothesis for the mechanism of mycoplasma evolution, Journal of Theoretical Biology 120, 1986-06, עמ' 457–465 doi: 10.1016/S0022-5193(86)80039-X
- ^ M J Rogers, J Simmons, R T Walker, W G Weisburg, Construction of the mycoplasma evolutionary tree from 5S rRNA sequence data., Proceedings of the National Academy of Sciences 82, 1985-02, עמ' 1160–1164 doi: 10.1073/pnas.82.4.1160
- ^ Kimberly A. Bliven, Anthony T. Maurelli, Evolution of Bacterial Pathogens Within the Human Host, Microbiology Spectrum 4, 2016-01-29 doi: 10.1128/microbiolspec.VMBF-0017-2015
- ^ Sandrine Borgeaud, Lisa C. Metzger, Tiziana Scrignari, Melanie Blokesch, The type VI secretion system of Vibrio cholerae fosters horizontal gene transfer, Science 347, 2015-01-02, עמ' 63–67 doi: 10.1126/science.1260064
- ^ Verónica Urdaneta, Josep Casadesús, Interactions between Bacteria and Bile Salts in the Gastrointestinal and Hepatobiliary Tracts, Frontiers in Medicine 4, 2017-10-03 doi: 10.3389/fmed.2017.00163
