קולטני דופמין

קולטני דופמין (באנגלית: Dopamine Receptors או בקיצור DR) הם קולטנים מצומדים לחלבון G (המכונים GPCRs), אשר מופעלים על ידי המוליך העצבי דופמין. האיתות (Signaling) שלהם מתווך על ידי אינטראקציה ושפעול של חלבון G (המכונה GTP-binding proteins)[1][2].
קולטנים אלה מופעלים על ידי הדופמין שנמצא במרווח הסינפטי, ומעבירים את המידע לתא שעליו הם מקושרים[3]. זהו המנגנון שבאמצעותו הדופמין ששוחרר מהתא הקדם-סינפטי פועל על התאים הפוסט-סינפטיים[4].
קולטני הדופמין שכיחים במערכת העצבים המרכזית (CNS) של בעלי חוליות. הם מעורבים בתהליכים נוירולוגיים רבים, כולל מוטיבציה, הנאה, קוגניציה, זיכרון, למידה, שליטה על מוטוריקה עדינה ועוד.
העברה סינפטית של דופמין[עריכת קוד מקור | עריכה]

פעילות הדופמין במערכת העצבים היא מורכבת, כך שיכולות להיות לו השפעות שונות במקרים שונים. השפעות אלו מקושרות בין היתר לתהליכי העברה סינפטית של המוליך העצבי דופמין.
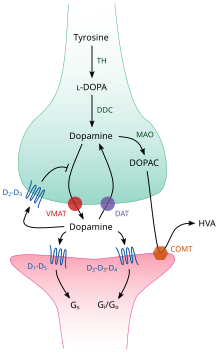
באופן כללי הדופמין מיוצר ומאוחסן בקצות הנוירונים ומשוחרר לסינפסות שלהם בעקבות דחף עצבי. כאשר הדופמין עובר את המרווח הסינפטי הוא מפעיל את הקולטנים המיוחדים לו בתא הפוסט סינפטי וכך הוא מעביר אליו את המידע[3].
הדופמין ממשיך לפעול על הקולטנים הבתר-סינפטיים כל עוד הוא נמצא במרווח הסינפטי[4]. בתום פעולת הדופמין הוא מפונה מהסינפסה במספר דרכים[3]. קולטנים קדם-סינפטיים תורמים לוויסות של כמות הפרשת הדופמין לסינפסה[2].
הדופמין יכול ליצור פוטנציאל פוסט-סינפטי מעכב או מעורר[5][6]. אופן ההשפעה של הדופמין תלוי בסוג הקולטן שאליו הוא נקשר ובתא המחובר לקולטן זה.
מעבר לקשרים בין נוירונים ספציפיים, קיימות במוח גם שלוש מערכות דופמינרגיות - מערכת הקשב, מערכת החיזוק, ומערכת קידוד הזיכרון ההצהרתי, בהן הדופמין מתפקד כהורמון לכל דבר.
סוגים של קולטני דופמין[עריכת קוד מקור | עריכה]
ישנם חמישה סוגים של קולטני דופמין[7]. סוגי הקולטנים השונים מפוזרים באזורים מוחיים שונים, כך שבאזורים מסוימים יכולים להיות יותר או פחות קולטנים מסוג מסוים בהשוואה לאזורים אחרים[3][4].
נהוג לסמן את הקולטנים באות D שאליה מצטרף המספר הרלוונטי. מספור הקולטנים נקבע על ידי סדר הגילוי שלהם[8].
DRD1 - קולטני דופמין D1[עריכת קוד מקור | עריכה]
 ערך מורחב – קולטן דופמין D1
ערך מורחב – קולטן דופמין D1
קולטני דופמין D1 (המכונים גם DRD1), הם קולטנים נפוצים יחסית. קולטני D1 הם קולטנים בתר-סינפטיים. גירוי קולטני D1 מביא לעלייה ברמת השליח השניוני cAMP בתא.
קולטני D1 נמצאים באזור הסטריאטום ובמיוחד באזורים האחראים על תנועה[2]. באזור זה יש קשר הפוך בין פעולת האצטילכולין לבין פעולת הדופמין[2].
לקולטני D1 שבקליפת המוח הקדם-מצחית יש חשיבות גדולה לזיכרון העבודה[9]. במהלך ביצוע של מטלה המתבססת על זיכרון העבודה, הדופמין פועל על קולטני D1 לצורך הפחתת יחס אות לרעש וייצוב של הדימוי המנטלי[10].
הריכוז של נשא הדופמין יכול להשפיע על אופן פעולתו של קולטן הדופמין D1[11]. זאת משום ששינויים בביטוי של נשא הדופמין יכולים לשנות באופן דרמטי את משך הזמן והעוצמה של האות הדופמינרגי בקולטנים שלו[12][13].
DRD2 - קולטני דופמין D2[עריכת קוד מקור | עריכה]

קולטני דופמין D2 (המכונים גם DRD2) הם קולטנים נפוצים יחסית. הם נמצאים באזור גרעיני הבסיס, כמו הגרעין הזנבי והפוטמן (Putamen), גרעין האקומבנס, ב-Olfactory Tubercle ובסטריאטום[2].
גירוי קולטנים אלו מפחית את רמת ה-cAMP. קולטני D2 יכולים להיות בתר-סינפטיים ויכולים להיות בעמדות קדם-סינפטיות. במקרים רבים הם משמשים כקולטנים עצמיים של התא הקדם סינפטי, אשר מווסתים את קצב ההפקה והשחרור של הדופמין[4].
קולטני D2 קשורים באופן משמעותי למערכת החיזוק[8]. עלייה בזמינות של קולטני D2 קשורה לאימפולסיביות נמוכה, יציבות רגשית, אפקט חיובי ונטייה לחוויית זרימה[14].
הזרימה מאופיינת כתחושה הוליסטית שאנשים מרגישים כאשר הם פועלים בריכוז מלא והנאה פנימית[15]. בהמשך לכך, הפעילות של קולטני D2 מקושרת גם ליכולת היצירתית של האדם[16].
ההשפעה החזקה של קולטני D2 על הסטריאטום מקושרת ליצירתיות באמצעות ההשפעה שלו על גמישות החשיבה, שהיא חלק חיוני מתהליך זה[16].
ירידה בכמות קולטני D2 מקושרת להשמנת יתר, אך לא ברור אם היא הגורם או התוצאה[17].
DRD3 - קולטני דופמין D3[עריכת קוד מקור | עריכה]
קולטני דופמין D3 (המכונים גם DRD3), נמצאים בחלק הקדמי של גרעין האקומבנס ובאזורים לימביים, כגון הגופים הממילריים ואזור הספטום[2], אך הם נפוצים יותר בסטריאטום, בהשוואה לאזורים אחרים במוח[4].
קולטנים אלו מווסתים את כמות הפרשת הדופמין אל תוך הסינפסה[2]. גירוי קולטנים אלו מפחית את רמת ה-cAMP בתא.
DRD4 - קולטני דופמין D4[עריכת קוד מקור | עריכה]
 ערך מורחב – קולטן דופמין D4
ערך מורחב – קולטן דופמין D4
קולטני דופמין D4 (המכונים גם DRD4), מבצעים תפקיד חשוב בתיווך האותות הדופמינרגיים בסינפסה[7]. גירוי קולטנים אלו מפחית את רמת ה-cAMP בתא.
הם נפוצים יותר בקליפת המוח הקדם-מצחית בהשוואה לאזורים מוחיים אחרים[4]. הגן האחראי על DRD4 נמצא בכרומוזום 11p15[18].
DRD5 - קולטני דופמין D5[עריכת קוד מקור | עריכה]
קולטני דופמין D5 (המכונים גם DRD5), נמצאים רק באזורים לטרליים של הגופים הממילריים ובאזורים ההיפוקמפיים[2].
גירוי קולטנים אלה מעלה את רמת ה-cAMP בתא. הגן של DRD5 נמצא קשור להפרעת קשב[18].
קולטנים עצמיים[עריכת קוד מקור | עריכה]
קולטנים עצמיים מצויים בדנדריטים, בגופי התא ובכפתורים הסופיים של נוירונים דופמינרגיים. הפעלתם גורמת היפר-פולריזציה ומפחיתה את הירי העצבי. הם דומים ל-D2.
קבוצות של קולטני דופמין[עריכת קוד מקור | עריכה]

חמשת קולטני הדופמין מחולקים לשתי קבוצות עיקריות: משפחת D1 ומשפחת D2[10][19]. לקולטנים שבכל אחת מה קבוצות יש מאפייני איתות (Signaling) המשותפים לקולטנים האחרים באותה הקבוצה, עם זאת ישנם גם הבדלים בין סוגי קולטנים שונים באותה הקבוצה[1]. כלומר, הקבוצות מאחדות בתוכן קולטנים שונים שחלק מהמאפיינים שלהם דומים.
לשתי המשפחות של קולטני הדופמין (משפחת D1 ומשפחת D2) יש תפקידים משלימים בשליטה הקוגניטיבית של התפקודים הניהוליים[20].
קולטני דופמין ממשפחת D1[עריכת קוד מקור | עריכה]
משפחת D1 (באנגלית: D1-like dopamine receptors), כוללת את קולטני דופמין D1 ו-D5[19][4][1][10]. קולטנים אלו מופעלים בעזרת אדניל ציקלאז (Adenyl Cyclase) על ידי חלבון G הידוע בשם Gso[2].
כל התרופות הפועלות על קולטני D1 פועלות גם על קולטני D5, על כן מחקרים פרמקולוגיים לא נוהגים להבדיל ביניהם[10]. בהתאם לכך, ניתן להתייחס לשני קולטנים אלו גם בכינוי המשותף קולטני D1/5[10].
קולטני דופמין ממשפחת D2[עריכת קוד מקור | עריכה]
משפחת D2 (באנגלית: D2-like dopamine receptors), כוללת את קולטני דופמין D3, D2 ו-D4[19][4][1][10]. קולטנים אלו אינם זקוקים לאדניל ציקלז, והם מופעלים על ידי חלבון הידוע בשם Gio[2].
קולטני דופמין ממשפחת D2 עוסקים במודולציה של אותות מוטוריים[20].
השפעות על קולטני דופמין[עריכת קוד מקור | עריכה]
הריכוז של נשא הדופמין יכול להשפיע על אופן פעולתם של קולטני הדופמין D1 ו- D2[11]. זאת משום ששינויים בביטוי של נשא הדופמין יכולים לשנות באופן דרמטי את משך הזמן והעוצמה של האות הדופמינרגי בקולטנים שלו[12].
היבטים רפואיים ונוירו-פסיכיאטריים[עריכת קוד מקור | עריכה]
האטיולוגיה של הפרעת קשב מקושרת לשונות בגנים של קולטני הדופמין[12], כמו DRD4 ו-DRD5[18]. האלל 7R של DRD4 אותר כמצביע על סיכון להפרעת קשב[7].
תרופות הפועלות על קולטני הדופמין[עריכת קוד מקור | עריכה]
משום שלקולטנים שונים ישנה השפעה שונה, אחת המטרות של הפרמקולוגיה היא לפתח תרופות שתפעלנה באופן ספציפי על סוג מסוים של קולטנים מבלי שתשפיע על הסוגים האחרים[3]. כך ניתן להעלות את יעילותה של תרופה מסוימת תוך צמצום תופעות לוואי בלתי רצויות.
התרופה מטוקלופראמיד שייכת למשפחת התרופות חוסמות קולטני דופמין. היא משמשת בעיקר לטיפול בבחילות והקאות אשר נגרמים עקב טיפולים כימותרפיים ולבעיות ושט וקיבה. כמו כן, התרופה משמשת לטיפול במיגרנה. מטוקלופראמיד ככל הנראה נקשר לקולטני דופמין מסוג D2 ופועל עליהם כאנטגוניסט. בנוסף פועל כאנטגוניסט על קולטני 5-HT3 וכאגוניסט לקולטני 5-HT4. התרופה פועלת כנוגדת בחילות והקאות בעקבות הפעילות האנטגוניסטית על קולטני הדופמין מסוג D2 הנמצאים במערכת העצבים המרכזית. במינונים גבוהים הפעילות האנטגוניסטית על קולטני 5-HT3 יכולה גם כן להקל על בחילות והקאות. פעילות מערכת העיכול מושפעת מפעילות מוסקרינית, פעילות אנטגוניסטית של קולטני D2 ופעילות אגוניסטית של קולטני 5-HT4.
אגוניסטים לדופמין[עריכת קוד מקור | עריכה]
 ערך מורחב – אגוניסטים לדופמין
ערך מורחב – אגוניסטים לדופמין
קיימות מספר תרופות המשמשות כאגוניסטים לדופמין. תרופות אלו מחקות את פעילותו של דופמין בתאים הפוסט סינפטיים וגורמים לשרשרת תהליכים תוך תאית בדומה לזה שנעשה על ידי הצמדות דופמין לקולטן.
השימוש הרפואי באגוניסטים לדופמין כולל טיפול במחלת פרקינסון[21], תסמונת הרגליים חסרות המנוחה[22], היפרפרולקטינמיה (בעיקר קברגולין)[23] והפסקת הנקה (קברגולין). למשל, פרמיפקסול פועל על הקולטנים D2, D3 ומחקה את פעילותו של המוליך העצבי דופמין. בכך מביא להקלה על התסמינים של מחלת פרקינסון[24]. באופן דומה לתרופה רופינירול יש אפיניות גבוהה לרצפטור D2 והיא מחקה את פעילותו של הדופמין. בכך מביא להקלה על התסמינים של מחלת פרקינסון.
מבחינה כימית והיסטורית, מקובל לחלק את משפחת האגוניסטים לדופמין לשתי קבוצות עיקריות:
- נגזרות של ארגוט - אלו הן תרופות שהופקו מפטריית הארגוט. הן כמעט ולא נמצאות יותר בשימוש (למעט ברומוקריפטין, שבארצות הברית משמש לטיפול בסוכרת מסוג 2 קשה), בשל תופעות לוואי הפוגעות במסתמי הלב. תרופות אלו פועלות על כל הקולטנים של דופמין.
- תרופות שאינן נגזרות של ארגוט - אלו הן תרופות חדשות יותר עם פרופיל בטיחות טוב יותר מבחינה לבבית. התרופות שהן אינן נגזרות של ארגוט (למעט רוטיגוטין) פועלות באופן ספציפי על הקולטנים D2-D3, ובכך יותר סלקטיביים בפעולתם בסינפסה.
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- "Dopamine Receptors". IUPHAR Database of Receptors and Ion Channels. International Union of Basic and Clinical Pharmacology.
- Zimmerberg, B., "Dopamine receptors: A representative family of metabotropic receptors, Multimedia Neuroscience Education Project (2002)
- Scholarpedia article on Dopamine anatomy
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ 1 2 3 4 Neve, K. A., Seamans, J. K., & Trantham-Davidson, H. (2004). Dopamine receptor signaling. Journal of receptors and signal transduction, 24(3), 165–205
- ^ 1 2 3 4 5 6 7 8 9 10 מוניץ, ח' (עורך). (2016). פרקים נבחרים בפסיכיאטריה. מהדורה שישית. תל אביב: דיונון
- ^ 1 2 3 4 5 רמי רחמימוב (2004). מהפכת המוח: תקשורת, מחלות נפש וסמים. רעננה: מכון ון ליר בירושלים הקיבוץ המאוחד
- ^ 1 2 3 4 5 6 7 8 By Vaidya, Chandan J.; Gordon, Evan M. ROLE OF DOPAMINE IN THE PATHOPHYSIOLOGY OF ATTENTION׳DEFICIT/HYPERACTIVITY DISORDER Kar, Bhoomika Rastogi (Ed), (2013). Cognition and brain development: Converging evidence from various methodologies. APA human brain development series., (pp. 105-125). Washington, DC, US: American Psychological Association, xiii, 328 pp
- ^ Neil R. Carlson, (2013). Physiology of Behavior. Boston: Pearson.
- ^ Kroener, S., Chandler, L., Phillips, P. M., & Seamans, J. K. (2009). Dopamine Modulates Persistent Synaptic Activity and Enhances the Signal-to-Noise Ratio in the Prefrontal Cortex. Plos ONE, 4(8), 1–14
- ^ 1 2 3 Mayseless, N., Uzefovsky, F., Shalev, I., Ebstein, R. P., & Shamay-Tsoory, S. G. (2013). The association between creativity and 7R polymorphism in the dopamine receptor D4 gene (DRD4). Frontiers in human neuroscience, 7
- ^ 1 2 Mark R. Rosenzweig, Arnold L. Leiman, S. Marc Breedlove (1999). Biological psychology: an introduction to behavioral, cognitive, and clinical neuroscience. 2nd ed. Sunderland, Massachusetts: Sinauer Associates
- ^ Floresco, S. B., & Magyar, O. (2006). Mesocortical dopamine modulation of executive functions: Beyond working memory.Psychopharmacology, 188(4), 567-85
- ^ 1 2 3 4 5 6 Arnsten, A. F. (2011). Catecholamine influences on dorsolateral prefrontal cortical networks. Biological psychiatry, 69(12), e89-e99
- ^ 1 2 Söderqvist, S., Nutley, S. B., Peyrard-Janvid, M., Matsson, H., Humphreys, K., Kere, J., & Klingberg, T. (2012). Dopamine, working memory, and training induced plasticity: Implications for developmental research. Developmental psychology, 48(3), 836
- ^ 1 2 3 Tripp, G., & Wickens, J. R. (2009). Neurobiology of ADHD. Neuropharmacology,57(7), 579-589
- ^ Binder, M. D., Hirokawa, N., Windhorst, U., & Hirsch, M. C. (2009). Encyclopedia of Neuroscience. Springer
- ^ de Manzano, Ö., Cervenka, S., Jucaite, A., Hellenäs, O., Farde, L., & Ullén, F. (2012). Individual differences in the proneness to have flow experiences are linked to dopamine D2-receptor availability in the dorsal striatum. NeuroImage 67, 1-6
- ^ Teng, C. I. (2011). Who are likely to experience flow? Impact of temperament and character on flow. Personality and Individual Differences, 50(6), 863–868
- ^ 1 2 Boot, N., Baas, M., van Gaal, S., Cools, R., & De Dreu, C. K. (2017). Creative cognition and dopaminergic modulation of fronto-striatal networks: Integrative review and research agenda. Neuroscience & Biobehavioral Reviews, 78, 13–23
- ^ Wang, G. J., Volkow, N. D., Logan, J., Pappas, N. R., Wong, C. T., Zhu, W., ... & Fowler, J. S. (2001). Brain dopamine and obesity. The Lancet, 357(9253), 354–357
- ^ 1 2 3 Berger, Andrea, (2011). Self-regulation: Brain, cognition, and development. Human brain development series., (pp. 61-90). Washington, DC, US: American Psychological Association
- ^ 1 2 3 Ranganath, A., & Jacob, S. N. (2016). Doping the mind: dopaminergic modulation of prefrontal cortical cognition. The Neuroscientist, 22(6), 593-603
- ^ 1 2 Ott, T., & Nieder, A. (2019). Dopamine and cognitive control in prefrontal cortex. Trends in cognitive sciences
- ^ Bonuccelli U and Pavese N. Role of dopamine agonists in Parkinson's disease: an update. Expert Rev Neurother. 2007 Oct;7(10):1391-9.
- ^ Zak RS and Walters AS. Dopaminergic Therapy for Restless Legs Syndrome/Willis-Ekbom Disease. Sleep Med Clin. 2015 Sep;10(3):279-85
- ^ Majumdar A and Mangal. Hyperprolactinemia. J Hum Reprod Sci. 2013 Jul-Sep; 6(3): 168–175.
- ^ Dooley M and Markham A. Pramipexole. A review of its use in the management of early and advanced Parkinson's disease. Drugs Aging. 1998 Jun;12(6):495–514
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.
