טומוגרפיית פליטת פוזיטרונים

טומוגרפיית פליטת פוזיטרונים (באנגלית: Positron Emission Tomography, ובראשי תיבות: PET)[1] היא טכניקת דימות ברפואה גרעינית, המשמשת להתבוננות בתהליכים מטבוליים בגוף האדם. המערכת מזהה זוגות של קרני גאמא, הנפלטות כתוצאה מדעיכתו של חומר רדיואקטיבי (טרייסר), שהוחדר לגוף על פני מולקולה פעילה ביולוגית. לאחר מכן, נבנות תמונות תלת-ממדיות של ריכוז הטרייסר בתוך הגוף.
רוב סריקות PET (כ-90% מהסריקות) משמשות לדימות ריכוז הגלוקוז ברקמות הגוף, מידע המאפשר זיהוי גידולים ממאירים וגרורות שלהם, ואבחון מחלות מוח.
אחד החסרונות העיקריים של סריקות PET הוא העלות הגבוהה שלהן,[2] הנובעת מעלות מכשיר הסריקה, מעלות הכנת החומרים הרדיואקטיביים הדרושים לסריקה ומשלוחם, ומהזמן והמיומנות הנדרשים לניתוח הסריקה.
כיום, סורקי PET-CT מאפשרים לשלב את טכניקת PET עם טכניקת CT על מנת לתת תמונה מלאה יותר של המטופל. סריקות ה-CT מבוצעות על החולה באותו המכשיר כמו סריקות הPET.
שימושים
[עריכת קוד מקור | עריכה]
ל- PET שימוש נרחב באונקולוגיה קלינית (דימות של גידולים, וחיפוש אחר גרורות) ובאבחון של מחלות מוח, כגון אלה הגורמות לסוגים שונים של שיטיון. בנוסף, PET היא כלי מחקרי חשוב למיפוי פעילות תקינה של המוח והלב האנושיים ולפיתוח תרופות. חשיבותה של PET מתבטאת בכך שמאפשרת להתמקד רק בחומרים מסוימים, המשמשים בגוף לפעולה הנחקרת.
PET משמשת גם במחקרים טרום קליניים על בעלי חיים, בהם היא מאפשרת חקירות חוזרות ונשנות על אותם הפרטים. יתרון זה גורם לעלייה באיכות הסטטיסטית של הנתונים, כיוון שהפרטים יכולים לשמש כקבוצת הבקרה של עצמם, ולירידה משמעותית במספר בעלי החיים הנחוצים לכל מחקר.
שיטות חלופיות של סריקה כוללות טומוגרפיה ממוחשבת באמצעות קרני רנטגן (CT), דימות תהודה מגנטית (MRI), דימות תהודה מגנטית תפקודי (fMRI), אולטרה סאונד (US) וטומוגרפיית פליטת פוטון בודד (SPECT).
בעוד חלק משיטות הסריקה, כמו CT ו-MRI, מדגימות שינויים אנטומיים בגוף, PET ו-SPECT מסוגלות לאתר אזורים בהם יש פעילות ביולוגית מולקולרית מסוימת, אפילו לפני שינוי אנטומי. סריקת ה-PET עושה זאת באמצעות שימוש בגששים מולקוריים מסומנים רדיואקטיבית, אשר נספגים במידה שונה בהתאם לסוג הרקמה המעורבת ותפקידה. סריקת ה-PET מסוגלת לכמת וליצור הדמיות של שינויים בזרימת הדם המקומית במבנים אנטומיים שונים.
דימות ה-PET היעיל ביותר נעשה באמצעות שימוש בסורק PET המיועד לכך. למרות זאת, ניתן לבצע דימות PET בעזרת מצלמת קרני גאמא דו-ראשית, מצוידת בגלאי אשר מסוגל לזהות אירועים סמוכים מאוד זה לזה בזמן (coincidence detector). איכות ה-PET המבוצע בעזרת מצלמת הגאמא נמוכה משמעותית מהשיטה המקובלת, והפקת הנתונים ממנה איטית. למרות זאת, שיטה זו מאפשרת דימות במוסדות עם ביקוש נמוך לבדיקות PET, ומונע הפנייתם של חולים למרכזים אחרים, או הסתמכות על סורקים ניידים.
אונקולוגיה
[עריכת קוד מקור | עריכה]סריקות PET משתמשות באיזוטופ רדיואקטיבי של פלואור (18F) המחובר למולקולת גלוקוז. החומר שמתקבל כתוצאה מכך הוא פלואורודיאוקסיגלוקוז (FDG), הנקרא גם FDG-PET. במנה טיפוסית של FDG בסריקה אונקולוגית יש מנת קרינה אפקטיבית של 14 מיליסיוורט.[3] טרייסר זה הוא אנלוג כימי של גלוקוז. הוא נספג על ידי תאים המשתמשים בגלוקוז ועובר זרחון על ידי הקסוקינאז (אנזים שריכוזו גבוה בתאים ממאירים). אטום החמצן של הגלוקוז, המוחלף בפלואור-18 בעת ייצור FDG מגלוקוז, נחוץ עבור השלב הבא של מטבוליזם של גלוקוז, ולכן FDG, שאטום זה חסר לו, לא משתתף בתגובות נוספות. בנוסף, רוב הרקמות (פרט לכבד ולכליות) אינן מסוגלות להסיר את הזרחן שנוסף למולקולות ה-FDG על ידי הקסוקינאז. משמעות הדבר היא שהמולקולה כלואה בכל תא שסופג אותה, עד דעיכתה, משום שסוכרים מזורחנים אינם יכולים לצאת מהתא, הודות למטענם היוני. כליאה זו מובילה למעשה לסימון רדיואקטיבי של רקמות עם ספיגת גלוקוז גבוהה, כמו המוח, הכבד, ומרבית הגידולים הסרטניים. כתוצאה מכך, סריקות FDG-PET יכולות לשמש לאבחון גידולים סרטניים, קביעת שלב המחלה ומעקב אחרי הטיפול בה, במיוחד במחלות מסוג לימפומת הודג'קין, לימפומה שאינה הודג'קין, וסרטן הריאות.
כיום, נכנסים בהדרגה גם איזוטופים ורדיוטרייסרים אחרים לשימוש בתחום האונקולוגיה. החומר 11C-metomidate, לדוגמה, יכול לשמש לזיהוי גידולים שמקורם בקליפת בלוטת יותרת הכליה (קליפת האדרנל).[4][5] דוגמה נוספת היא סריקת FDOPA PET-CT, שהוכיחה עצמה כשיטה רגישה יותר לזיהוי ואיתור פאוכרומוציטומה מאשר סריקת MIBG.[6][7][8]
דימות מוחי
[עריכת קוד מקור | עריכה]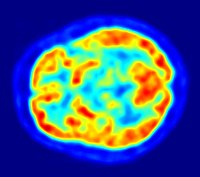
דימות נוירולוגי
[עריכת קוד מקור | עריכה]דימות מוחי בעזרת PET מבוסס על ההנחה, לפיה אזורים פעילים רדיואקטיבית הם אזורים בהם מתרחשת פעילות מוחית. הערך הנמדד בעקיפין בסריקות אלה, על ידי הטרייסר חמצן-15, הוא זרימת הדם לאזורים שונים במוח. אך מדידה שכזו היא קשה לביצוע, כיוון שחמצן-15 הוא אטום רדיואקטיבי בעל זמן חיים של שתי דקות בלבד, ולכן על מנת להשתמש בו בסריקה יש להזרים אותו ישירות מציקלוטרון רפואי.
בפועל, סריקת FDG-PET סטנדרטית של המוח, שמודדת שימוש מקומי בגלוקוז, יכולה גם היא לשמש להבחנה בין מחלת אלצהיימר לבין תהליכי שיטיון מוחי אחרים, וגם לאבחון מוקדם של אלצהיימר. זאת משום שהמוח לרוב צורך כמויות גדולות של גלוקוז, ופתולוגיות מוחיות כמו מחלת אלצהיימר מפחיתות מאוד את המטבוליזם של גלוקוז ושל חמצן במוח. היתרון של סריקת FDG-PET על פני סריקות אחרות בנושא זה הוא נגישותו הגבוהה.
דימות PET בעזרת FDG יכול לשמש גם לאיתור מוקד של התקף אפילפטי, שכן המוקד יופיע בסריקות בין-התקפיות כאזור היפומטבולי. בנוסף, פותחו עבור שימוש בסריקות PET רדיוטרייסרים שהם ליגנדים, הנקשרים לסוגי קולטנים עצביים מסוימים. למשל:
- 11C] raclopride]
- [18F] fallypride]
- 18F] desmethoxyfallypride]
נקשרים לקולטני דופמין D2/D3;
- 11C] McN 5652]
- [11C] DASB]
נקשרים לטרנספורטרים של סרטונין;
18F] Mefway]
נקשר לקולטני סרטונין 5HT1A;
ו-18F] Nifene]
נקשר לקולטנים ניקוטיניים או למצעי אנזימים.
חומרים אלו מאפשרים לחזות בקבוצות של קולטנים עצביים מסוימים בהקשר למספר רב של מחלות נוירולוגיות ונוירופסיכיאטריות.
דימות עמילואידים נמצא כיום על סף שימוש קליני, הודות לפיתוחם של מספר גששים חדשניים עבור דימות לא פולשני של משקעים במוח האדם. הגששים המוקדמים ביותר לדימות עמילואידים היו:
[9]שפותח באוניברסיטת קליפורניה, לוס אנג'לס, ו-
[10] הנקרא גם תרכובת פיטסבורג B, שפותח באוניברסיטת פיטסבורג. גששי דימות עמילואידים אלו מאפשרים לחזות בלוחיות עמילואידים במוחותיהם של חולי אלצהיימר, ויכולים לסייע לקליניקאים לאבחן אלצהיימר ולפתח טיפולים חדשניים נגד עמילואידים. המולקולה 11C]PMP] היא תרכובת רדיואקטיבית פורצת דרך המשמשת ב-PET על מנת לבחון את הפעילות של מערכת המוליכים העצביים האצטילכוליניים, בכך שהיא משמשת מצע לאצטילכולין אסטראז. ניתוחים לאחר המוות של חולי אלצהיימר מצביעים על רמות נמוכות של אצטילכולין אסטראז. 11C]PMP] משמשת למיפוי פעילות האצטילכולין אסטראז במוח, ולכן יכולה לסייע באבחון מחלת אלצהיימר ובמעקב אחרי הטיפול בה.[11] חברת Avid Radiopharmaceuticals מפילדלפיה פיתחה חומר בשם 18F-AV-45 שמשתמש ברדיונוקליד ארוך-החיים פלואור-18 על מנת לזהות לוחיות עמילואידים בעזרת סריקות PET.[12]
נוירופסיכולוגיה / נוירולוגיה קוגניטיבית
[עריכת קוד מקור | עריכה]בחינת הקשר בין תהליכים פסיכולוגיים או הפרעות לבין פעילות מוחית.
פסיכיאטריה
[עריכת קוד מקור | עריכה]מספר תרכובות הנקשרות באופן בררני לקולטנים עצביים מסוימים, יכולות להיות מסומנות רדיואקטיבית בעזרת C-11 או F-18. רדיוליגנדים הנקשרים לקולטני דופמין (D1,[13] D2[14][15]), קולטני סרטונין (5HT1A, 5HT2A), קולטני אופיואיד ועוד, שימשו בהצלחה במחקרים על בני אדם. ישנם מחקרים הבוחנים את מצבם של קולטנים אלו בחולים בסכיזופרניה, מכורים לסמים, בעלי הפרעות אפקטיביות ועוד, ביחס לקבוצות בקרה בריאות.
כירורגיה סטריאוטקטית ורידוכירורגיה
[עריכת קוד מקור | עריכה]כירורגיה המונחית באמצעות דימות PET מאפשרת טיפול בגידולים תוך-גולגולתיים, במלפורמציה עורקית-ורידית ובמצבים אחרים הניתנים לטיפול כירורגי.[16]
קרדיולוגיה
[עריכת קוד מקור | עריכה]בקרדיולוגיה קלינית, סריקות FDG-PET מסוגלות לזהות לקויות בהתכווצותם של חלקי שריר הלב (hibernating myocardium), אבל התועלת של סריקה זו ביחס לעלותה אינה ברורה לעומת יעילותה של בדיקת SPECT.
דימות FDG-PET של טרשת עורקים, לאיתור חולים עם סכנה לשבץ, יכול לסייע לבחון את יעילות הטיפולים החדשניים בטרשת עורקים.[17]
מחלות זיהומיות
[עריכת קוד מקור | עריכה]הדמיית זיהומים עם טכנולוגיות דימות מולקולריות יכולה לשפר את האבחון ואת טיפולי ההמשך. בעבר, סריקות PET שימשו להדמיית זיהומים בקטריאליים רפואיים תוך שימוש ב-FDG לזיהוי תגובה דלקתית הקשורה לזיהום.
לאחרונה, שלושה סוגים שונים של חומרי ניגוד פותחו עבור PET להדמיית זיהומים בקטריאליים:
FDS הוא בעל ערך מוסף בדמות יכולת להתמקד בחיידקים ממשפחת Enterobacteriaceae.
פרמקוקינטיקה
[עריכת קוד מקור | עריכה]בניסויים טרום-קליניים, ניתן לסמן רדיואקטיבית תרופה חדשה ולהזריק אותה לבעלי חיים. סריקות כאלו מכונות מחקר פיזור ביולוגי (biodistribution). באמצעות שיטה זו, ניתן לפקח באופן אפקטיבי ומהיר יותר על ספיגת התרופה, הרקמות בהן היא מתרכזת, והיעלמותה בסופו של דבר. לעומתה, שיטות ישנות יותר כללו הרג וניתוח בעלי החיים על מנת להשיג ולגלות מידע זהה.
אולם, בדרך כלל, ניתן להסיק בדרך עקיפה את מידת הימצאות התרופה במקום מסוים על ידי מחקר תחרותי בין תרופה שאינה מסומנת לבין תרכובת מסומנת רדיואקטיבית הידועה כתרכובת הנקשרת לאתר הנחקר. רדיוליגנד בודד יכול לבחון בצורה זו מספר רב של תרופות פוטנציאליות למטרה אחת. שיטה דומה מערבת סריקה באמצעות רדיוליגנד שמתחרה עם חומר טבעי בקולטן מסוים על מנת להדגים שהתרופה גורמת לשחרור החומר הטבעי.
להלן קטע מתוך מאמר של הכותב פיטר ראואל מאוניברסיטת הרווארד, שפורסם באתר HarvardScience: "תהליך כימי חדש, יכול להרחיב את האפשרויות של טומוגרפיית פליטת הפוזיטרונים (PET) על ידי יצירת תמונה תלת־ממדית (3D) בזמן אמת של הפעילות הכימית שמתרחשת בתוך הגוף. היכולת החדשה הזאת, מעלה אפשרות מפתה של שימוש בסריקות PET על מנת להתבונן במספר תהליכים המתרחשים בתוך בעלי חיים ובני אדם על ידי פישוט תהליך השימוש בגלאים מולקולריים לצורך יצירת תמונה תלת־ממדית." (מחקר זה יוכל לשמש לפיתוח תרופות).[20]
דימות בעלי חיים קטנים
[עריכת קוד מקור | עריכה]לצורך מטרה זו, נבנה סורק PET מיניאטורי, שניתן להלבשה על ראשה של חולדה הנמצאת בהכרה מלאה, בעת שהיא נעה בחופשיות.[21] סורק זה, הקרוי RatCAP, מאפשר סריקת בעלי חיים ללא תופעות הלוואי של הרדמה. סורקי PET, המכונים microPET, שעוצבו במיוחד לדימות מכרסמים, וכן סורקים המיועדים ליונקים קטנים, משווקים כיום למחקר אקדמאי ותרופתי. הסורקים מבוססים על חומרים פולטי אור (scintillators) מיניאטוריים ודיודות מפולת (APDs). בנוסף, מערכת שהומצאה לאחרונה משתמשת במכפילור סיליקון.
דימות שלד ושרירים
[עריכת קוד מקור | עריכה]סריקות PET הוכיחו את עצמן גם כשיטה לחקר שרירי השלד במהלך פעילות, כגון הליכה.[22] יתרון מרכזי בשימוש בPET הוא שסריקה זו יכולה לספק מידע אודות שרירים פנימיים, כגון שריר העכוז הקטן, לעומת שיטות מחקר אחרות כמו אלקטרומיוגרפיה, שמאפשרות התבוננות בשרירים הקרובים לעור בלבד. עם זאת, חיסרון מובהק של סריקת PET בעניין זה הוא שאינה מספקת מידע לגבי תזמון פעילות השריר, מכיוון שהיא נמדדת לאחר שהפעילות נגמרה, וזאת בשל פרק הזמן שלוקח למולקולה FDG להצטבר בשרירים הפעילים.
בטיחות
[עריכת קוד מקור | עריכה]סריקת PET אינה פולשנית, אך היא כוללת חשיפה לקרינה מייננת.[2]
הרדיוטרייסר הסטנדרטי כיום בדימות מוחי וטיפול בחולי סרטן הוא 18F-FDG,[23] והוא בעל מנת חשיפה לקרינה של 14 mSv.[3]
מנת קרינה זו דומה למנת הקרינה שנחשפים אליה בשהייה במשך שנה שלמה בעיר האמריקאית דנוור, קולורדו (12.4 mSv/year).[24] לשם השוואה, מנת הקרינה של סוגי סריקות אחרות נעה בין 0.02 mSv עבור צילום רנטגן של בית החזה, עד 6.5-8 mSv לסריקת CT של בית החזה.[25][26]
צוות הטיסה האזרחי הממוצע נחשף בשנה לכ-3 mSv.[27] המגבלה לעובדים בתחום האנרגיה הגרעינית בארצות הברית היא 50 mSv בשנה.[28] להמשך קריאה בנושא סדרי גודל בקרינה, ראה Orders of magnitude (radiation).
עבור סריקת PET-CT' החשיפה לקרינה נעה בין 23–26 mSv לאדם השוקל 70 ק"ג, כאשר מנת הקרינה עלולה לעלות ככל שמשקל האדם עולה.[29]
פעולה
[עריכת קוד מקור | עריכה]
רדיונוקלידים ורדיוטרייסרים
[עריכת קוד מקור | עריכה]הרדיונוקלידים המשמשים לסריקות PET הם לרוב איזוטופים בעלי זמן מחצית חיים קצר,[30] כמו:
- פחמן-11 - זמן מחצית חיים של כ-20 דקות.
- חנקן-13 - זמן מחצית חיים של כ-10 דקות.
- חמצן-15 - זמן מחצית חיים של כ-2 דקות.
- פלואור-18 - זמן מחצית חיים של כ-110 דקות.
- גאליום-68 זמן מחצית חיים של כ-67 דקות.
- זירקוניום-89 זמן מחצית חיים של כ-78.41 שעות.
- רובידיום-82 זמן מחצית חיים של כ-1.27 דקות.
רדיונוקלידים (רדיואיזוטופים) אלה משולבים במולקולות בעלות שימוש רב בגוף, כמו גלוקוז (או אנלוגיות לגלוקוז), מים או אמוניה. הם יכולים להיות משולבים גם במולקולות הנקשרות לקולטנים או אתרים אחרים בהם ישנה פעילות של תרופה. מולקולות מסומנות אלה נקראות רדיוטרייסרים. טכנולוגיית PET יכולה לשמש על מנת לעקוב אחרי המסלול הביולוגי של כל תרכובת בבני אדם חיים (ובמינים רבים אחרים), בהנחה שתרכובת זו נתונה לסימון באמצעות איזוטופ PET. בכך, התהליכים הספציפיים הנתונים למחקר באמצעות PET הם כמעט בלתי מוגבלים, וסינתזה של רדיוטרייסרים עבור מולקולות ותהליכים חדשים מתרחשת כל הזמן. כיום, עשרות רדיוטרייסרים נמצאים בשימוש קליני, ומאות בשימוש מחקרי. הרדיוטרייסר הנפוץ ביותר בסריקות PET קליניות הוא פלואורדאוקסיגלוקוז (FDG), אנלוג כימי של גלוקוז שמסומן באמצעות פלואור-18. רדיוטרייסר זה משמש בכמעט כל הסריקות האונקולוגיות וברוב הסריקות הנוירולוגיות, ולכן מהווה הרדיוטרייסר העיקרי (מעל 95%) המשמש בסריקות PET ו-PET-CT.
הודות לזמני מחצית החיים הקצרים של רוב הרדיואיזוטופים פולטי הפוזיטרונים, הרדיוטרסיירים מיוצרים לרוב בעזרת ציקלוטרון הנמצא בסמוך למתקן דימות ה-PET. זמן מחצית החיים של פלואור-18 ארוך מספיק על מנת לאפשר ייצורו מחוץ למתקן והעברתו למרכזי הדימות. לאחרונה, מייצרי רובידיום-82 הפכו נגישים בשוק הרחב.[31] אלה מכילים סטרונציום-82, הדועך באמצעות לכידת אלקטרון לרובידיום-82, הפולט פוזיטרונים.
תהליך הפליטה
[עריכת קוד מקור | עריכה]על מנת לבצע את הסריקה, טרייסר רדיואקטיבי קצר חיים מוזרק לתוך הנבדק (בדרך כלל לזרם הדם שלו). כל אטום של הטרייסר משולב בצורה כימית במולקולה פעילה ביולוגית. ישנו זמן המתנה בזמן שריכוז המולקולה הפעילה ברקמות הנבדקות עולה. זמן ההמתנה עבור הרדיוטרייסר הנפוץ ביותר, FDG, הוא לרוב כשעה. לאחר מכן הנבדק נכנס לסורק. בזמן הסריקה, רישומים של הריכוזים ברקמות נשמרים בזמן שהטרייסר דועך.

כשהרדיוטרייסר עובר דעיכת פליטת פוזיטרון (הידועה גם כדעיכת בטא חיובית), הוא פולט פוזיטרון, אנטי חלקיק של אלקטרון בעל המטען החשמלי ההפוך לו. הפוזיטרון הנפלט נע ברקמות למרחק קצר (לרוב פחות ממילימטר אחד, אבל מרחק זה תלוי באיזוטופ המסוים[32]). בזמן זה הפוזיטרון מאבד אנרגיה קנטית, ומאט עד לנקודה שהוא מסוגל לבצע אינטראקציה עם אלקטרון (קביעה זו היא ניסויית בלבד נכון לעכשיו, וקורה כתוצאה מתנועה בקרבת לוח אלומיניום.[33][34] המפגש ביניהם (איון פוזיטרון-אלקטרון) משמיד את האלקטרון וגם את הפוזיטרון, ויוצר זוג פוטונים (קרני גאמא) הנעים בקירוב בכיוונים הפוכים. אלה מתגלים כאשר הם פוגעים בחומר המפיץ אור (scintillator), שמתיינן עקב פגיעתם. אור זה ניתן לזהות באמצעות מכפילור או דיודת מפולת עשויה סיליקון (APD). הטכניקה תלויה בגילוי סימולטני של זוג הפוטונים. פוטונים שאינם מגיעים ב"זוגות" - כלומר בהפרש של ננו-שניות בודדות זה מזה - אינם נלקחים בחשבון.
זיהוי אירוע איון פוזיטרונים
[עריכת קוד מקור | עריכה]תוצאתם של האירועים המשמעותיים ביותר של איון אלטרון-פוזיטרון היא פליטת שני פוטוני גאמא 511 KeV בזווית של כמעט 180 מעלות ביניהם. לכן, ניתן לאתר את מקור ההתרחשות לאורך הקו הישר של ההתנגשות (LOR). בפועל, מכיוון שהפוטונים נפלטים בזווית שאינה בדיוק 180 מעלות, לLOR רוחב שונה באפס. מרווח הזמן הקטן ביותר שמסוגלים רוב הגלאים הנפוצים כיום לזהות הוא כ-10 ננו-שניות. לאחר זיהוי זוג הפוטונים, ניתן לאתר את מיקום האירוע על מיתר שאורכו נקבע לפי רזולוציית עיתוי הגלאי. במערכות מתקדמות יותר, כאשר רזולוציית העיתוי משתפרת ומרווח הזמן קטן, יחס האות לרעש (SNR) של התמונה משתפר, וכך ניתן להגיע לאותה איכות דימות, עם פחות אירועי התנגשות. סורקים בעלי דיוק גבוה במיוחד אינם נפוצים עדיין.[35]
שחזור תמונה
[עריכת קוד מקור | עריכה]הנתונים הגולמיים שנאספים על ידי סורק PET הם רשימה של אירועי התנגשות המייצגים זיהוי על ידי שני גלאים של פוטונים שנפלטו מההתנגשות, בזמנים כמעט זהים. כל אירוע התנגשות מייצג קו במרחב שמחבר את שני הגלאים שלאורכם התרחשה פליטת הפוזיטרונים, הקרוי LOR. מערכות מודרניות בעלות רזולוציות זמן גבוהה (בערך 3 ננו-שניות) משתמשות בשיטה (הקרויה "Time-of-flight") בה הם קובעים בצורה מדויקת יותר את הבדלי הזמן בין איתורם של שני הפוטונים ובכך ממקמים בצורה מדויקת יותר את נקודת המוצא של אירוע האיון.
ניתן לקבץ את אירועי ההתנגשות לתמונות הקרויות סינוגרם (sinogram). הסינוגרם ממויין לפי הזווית וההטייה של כל תמונה (על מנת להשיג תמונה תלת־ממדית). תמונות הסינוגרם דומות לתצלומים של סורקי CT, וניתן לשחזר אותן בוצרה דומה. עם זאת, סטטיסטיקת הנתונים של PET גרועה בהרבה, מה שגורם ל"רעש תמונה" גדול יותר בתצלומי PET.
שני גורמים מרכזיים לרעש ב-PET הם:
- פיזור - הקצאת זוג פוטונים מזוהים ל-LOR לא נכון. נובע מסטייתו של לפחות אחד מהפוטונים ממסלולו המקורי בעקבות אינטראקציה של הפוטון עם חומר כלשהו.
- אירועים אקראיים - פוטונים שנרשמו כאירועי התנגשות בעקבות הגעתם לגלאים באותו חלון זמן, אך מקורם בשני אירועי איון שונים.
בפועל, נחוץ עיבוד נתונים מראש הכולל תיקון עבור אירועים אקראיים, אומדן והתעלמות מפוטונים מפוזרים, תיקון זמן-מת של הגלאי (לאחר זיהוי פוטון, הגלאי חייב להתקרר) ותיקון רגישות הגלאי (הן רגישות הגלאי עצמו, והן הבדלים ברגישות בעקבות הבדלים בזווית הפגיעה).
שיטת FBP) Filtered Back Projection) משמשת לעיתים קרובות לשחזור תמונות מתוך הסינוגרמים. לאלגוריתם זה יתרון בכך שהוא פשוט ואינו זקוק למשאבי מחשוב רבים. עם זאת, רעש שוט בנתונים הגולמיים בולט מאוד בתמונה המשוחזרת ואזורי ספיגת גלאים גבוהה יותר נוטים ליצור פסים לאורך התמונה. בנוסף, FBP מטפל בנתונים בצורה דטרמיניסטית, כלומר הוא אינו לוקח בחשבון את האקראיות שנקשרת לנתוני הPET, ולכן טרם השחזור ישנו צורך בתיקונים השונים שהוזכרו.
באמצעות נתונים סטטיסטיים שנאספים מעשרות אלפי אירועי התנגשות, מספר משוואות סימולטניות עבור הפעילות של רקמות לאורך LOR יכולות להפתר במספר שיטות. כך יכולה להיבנות מפה של הפעילות הרדיואקטיבית כפונקציה של מיקום הרקמות. המפה שנוצרת מראה את הרקמות בהן הגלאים המולקולריים התרכזו, והיא מפוענחת על ידי מומחה לרפואה גרעינית או רדיולוג לפי האבחון ותוכנית הטיפול של המטופל.
גישות סטטיסטיות המבוססות על הסתברות
[עריכת קוד מקור | עריכה]אלגוריתמי מיקסום תוחלת איטרטיביים סטטיסטיים המבוססים על הסתברות כמו אלגוריתם שייפ-ווארדי[36] הם השיטה המועדפת כיום לשחזור. אלגוריתמים אלו אומדים את הפיזור האפשרי שנוצר מאירועי האיון לפי עקרונות סטטיסטיים.[37][38] היתרון הוא שיפור במצב הרעש בתמונה וירידה בתופעת הפסים שנפוצים עם FBP. החיסרון הוא דרישות גבוהות יותר במשאבי מחשב.
מחקרים הוכיחו כי שיטות הסתברות בייסיאניות שכוללים את פונקציית הסתברות פואסון והסתברות פריורית, יכולים להניב תוצאות יותר טובות מהשיטות המבוססות על מיקסום התוחלת אשר כוללות הסתברות פואסון, אך לא כוללות הסתברות פריורית.[39]
תיקון הדללה
[עריכת קוד מקור | עריכה]הדללה מתרחשת כאשר הפוטונים הנפלטים מהרדיוטרייסר שבתוך הגוף נספגים ברקמות שבין פליטת הפוטון לבין הגלאי. משום שLOR-ים שונים עוברים ברקמות שונות בעלי עובי שונה, הפוטונים מדוללים בצורה שונה. משמעות הדבר היא שמבנים הנמצאים עמוק בתוך הגוף משוחזרים כאילו יש להם ספיגת טרייסר נמוכה יותר מן הספיגה האמיתית. סורקים מודרניים מסוגלים להעריך את ההדללה באמצעות ציוד CT מובנה המשתמש בקרני רנטגן, אך סורקים מוקדמים יותר השתמשו בצורה גסה של CT בעזרת קרני גאמא ובעזרת גלאי ה-PET.
בעוד שהדמיות שעברו תיקון הדללה הן לרוב אמינות יותר, תהליך התיקון עצמו נתון לטעויות. כתוצאה מכך, התמונה המתוקנת והתמונה הלא מתוקנת משוחזרת שתיהן ונקראות יחדיו.
שחזור 2D/3D
[עריכת קוד מקור | עריכה]בסורקי PET ראשוניים הייתה רק טבעת אחת של גלאים, לכן איסוף הנתונים והשחזור הוגבלו למישור דו-ממדי יחיד. סורקים חדשניים יותר כוללים מספר טבעות, והם יוצרים גליל של גלאים.
ישנן שתי גישות של שחזור התמונה מהמידע בסורק כזה:
- שחזור דו-ממדי - התייחסות לכל אחת מהטבעות כמערכת נפרדת, כך שאירועי התנגשות שמתרחשים בכל אחת מהטבעות מזוהים, והתמונה משוחזרת מכל אחת בנפרד.
- שחזור תלת-ממדי - זיהוי התנגשויות בין הטבעות בנוסף לאלו בתוך הטבעות, ולאחר מכן שחזור כל הנתונים בבת אחת.
לשיטות תלת־ממדיות יש רגישות גבוהה יותר (מכיוון שהן מזהות יותר התנגשויות), ולכן יש פחות רעש, אך הן רגישות יותר לתופעות פיזור ואירועים אקראיים, וכן דורשים משאבי מחשב גדולים יותר בהתאמה. הופעתם של גלאים בעלי רזולוציית עיתוי של פחות מננו שנייה מאפשרים התעלמות גבוהה יותר מאירועים אקראיים, ובכך נותנת העדפה לשחזור תלת־ממדי.


שילוב של PET עם CT וMRI
[עריכת קוד מקור | עריכה]כיום, הולך וגובר השימוש בסריקות PET לצד סריקות CT ו-MRI, צירוף המשלב מידע אנטומי ומטבולי. מכיוון שדימות PET שימושי ביותר בשילוב עם דימות אנטומי, כגון CT, סורקי PET מודרניים משולבים כעת עם סורקי CT high-end multi-detector-row. סורקים משולבים אלה נקראים סורקי PET-CT. כיוון שהמטופל יכול לבצע את שתי הסריקות באותו הביקור, ללא שינוי אפילו בתנוחה בה הוא נמצא. רישום שתי התמונות המתקבלות מתבצע בדיוק רב יותר, מכיוון שהאזורים החריגים בPET מקושרים לאנטומיה המתקבלת בתמונת הCT. שיטה זו שימושית מאוד בדימות איברים נעים או מבנים בעלי גיוון אנטומי רב.
באפריל 2009 החל לפעול במכון למדעי למוח וביופיזיקה ביוליך מכשיר הPET-MRI הגדול בעולם, שכלל טומוגרפיית תהודה מגנטית (MRT) של 9.4 טסלה בשילוב עם טומוגרפיית פליטת פוזיטרונים (PET). כיום, ניתן לבצע בשדות מגנטיים חזקים אלו דימות של הראש והמוח בלבד.[40]
מגבלות
[עריכת קוד מקור | עריכה]השימוש ברדיונוקלידים קצרי חיים אטרקטיבי מאוד הודות למינימליזציה של מנת הקרינה לנבדק. למרות זאת, מעבר לתפקידן המבוסס כטכניקת אבחון, לסריקות PET תפקיד הולך וגובר כשיטה לבחון את תגובת הנבדק לטיפול, בפרט טיפול בסרטן,[41] שבו הסיכון לחולה הנובע מחוסר מודעות להתקדמות המחלה גובר בהרבה על הסיכון הנובע מהקרינה שבסריקה.
ישנן מגבלות לשימוש נרחב בסריקות PET, והן נובעות מהעלויות הגבוהות של הציקלוטרונים הנדרשים על מנת לייצר את הרדיונוקלידים קצרי החיים, ומהצורך לציוד ייחודי לסינתוז כימי על מנת ליצור את התרכובות הכימיות לאחר ייצור הרדיואיזוטופים. לא ניתן לייצר את הרדיוטרייסרים האורגניים, העתידים להכיל רדיואיזוטופ פולט פוזיטרונים, לפני הרדיואיזוטופ, מפני שההפצצה באמצעות הציקלוטרון הנדרשת עבור ייצור האיזוטופ משמידה כל נשא אורגני שלו. לכן, יש לייצר ראשית את האיזוטופ, ורק לאחר מכן לייצר את הרדיוטרייסר האורגני (כגון FDG) במהרה, לפני שהאיזוטופ דועך. מעטים בתי החולים והאוניברסיטאות המסוגלים לתחזק מערכות כאלה, ומשום כך רוב מתקני ה-PET הקליניים מקבלים את הרדיוטרייסים שלהם מספקים חיצוניים המציידים מספר רב של מתקנים. מאפיין זו מגביל את ה-PET הקליני לשימוש בעיקר בטרייסרים המסומנים בפלואור-18, שהוא בעל זמן מחצית חיים של 110 דקות ולכן יכול להישלח למרחק סביר לפני השימוש. האפשרות הסבירה השנייה היא סימון ברובידיום-82 (נמצא בשימוש כרובידיום-82 כלוריד), בעל זמן מחצית חיים של 1.27 דקות, המיוצר בגנרטור נייד ומשמש לבדיקות מיפוי לב. למרות זאת, בשנים האחרונות נכנסו לשימוש בבתי חולים מרוחקים ציקלוטרונים מקומיים בעלי הגנות מובנות מקרינה ו"מעבדות חמות" (מעבדות כימיה אוטומטיות העובדות עם רדיואיזוטופים). נוכחותם של הציקלוטרונים המקומיים הקטנים ככל הנראה תתרחב בעתיד, והציקלוטרונים יקטנו בתגובה לעלות הגבוהה של משלוח איזוטופים למכונות PET מרוחקות.[42] בשנים האחרונות המחסור בסריקות PET בארצות הברית הוקל, בעקבות הגידול בייצוא הרדיואיזוטופים מטעם בתי המרקחת בכ-30% בשנה.
משום שזמן מחצית החיים של פלואור 18 הוא כשעתיים, התרכובת הרדיואקטיבית הנושאת אותו תעבור מספר דעיכות במהלך יום עבודה. תכונה זו מחייבת כיול מחדש תכוף של המנה הנותרת, ותכנון קפדני הלוקח בחשבון את לוחות הזמנים של הבדיקות.[43]
היסטוריה
[עריכת קוד מקור | עריכה]המושג טומוגרפיית פליטת פוזיטרונים הוצג לראשונה על ידי דוד אדמונד קחל (David E. Kuhl), לוק צ'פמן (Luke Chapman) ורועי אדוורדס (Roy Edwards) בשנות ה-50 המאוחרות. עבודתם הובילה לעיצוב ובניית מספר מכשירים טומוגרפיים באוניברסיטת פנסילבניה. בשנת 1985 שיטות דימות טומוגרפי פותחו על ידי מייקל טר-פוגוסיאן (Michel Ter-Pogossian), מיכאל אדוורד פלפס (Michael E. Phelps), אדוורד יוסף הופמן (Edward J. Hoffman) ואחרים בבית הספר לרפואה של אוניברסיטת וושינגטון.[44][45]
עבודתם של גורדון ברוול (Gordon Brownell), צ'ארלס ביירהם (Charles Burnham) ושותפיהם בבית החולים של מסצ'וסטס בתחילת שנות ה-50, תרמה רבות לפיתוח טכנולוגיית ה-PET וכללה שימוש ראשוני בקרינת איון עבור דימות רפואי.[46] חידושיהם כללו שימוש בצינורות אור וטיטור, ופיתחו מאוד את התחום. בשנת 1961, ג'יימס רוברטסון (James Robertson) ושותפיו במעבדה הלאומית ברוקהייבן בנו את סורק הPET הראשון, שכונה "מכווץ הראשים" ("head-shrinker").[47]
אחד הגורמים המשפיעים ביותר לכניסת דימות הפוזיטרון לתוך עולם הרפואה היה הפיתוח בייצור חומרים רדיואקטיביים. בפרט, פיתוחה של המולקולה 2FDG על ידי קבוצה מברוקהייבן תחת ניהולם של אל וולף (Al Wolf) וג'והנה פוולר (Johanna Fowler) היוותה גורם מרכזי בהרחבת תחום הדימות באמצעות PET.[48] התרכובת יושמה לראשונה על שני מתנדבים בעלי מוח נורמטיבי על ידי אבאס אלווי (Abass Alavi) באוגוסט 1976 באוניברסיטת פנסילבניה. תמונות המוח האנושי שהתקבלו בסורק גרעיני רגיל (שאינו PET) הדגימו את ריכוז ה-FDG באיבר. מאוחר יותר, השתמשו בחומר זה בסורקי PET ייעודיים, וכך נוצרה פרוצדורת ה-PET המודרנית.
ההרחבה ההגיונית ביותר למכשור פוזיטרונים הייתה שימוש בשני מערכים דו־ממדיים של גלאים. המכשיר PC-I, שתוכנן ב-1968, סיים להיבנות ב-1969 ופורסם ב-1972, היה המכשיר הראשון שהשתמש בשיטה זו. היישומים הראשונים של הPC-I במצב טומוגרפי שצוינו והובדלו מהטומוגרפיה הממוחשבת דווחו ב-1970.[49] במהרה, אלו שהשתתפו בפיתוח PET הבינו כי מערך עגול או גלילי של גלאים הוא הצעד הבא בטכנולוגיית PET. למרות שחוקרים רבים פעלו לפי גישה זו, ג'יימס רוברטסון (James Robertson)[50] וזאנג-הי צ'או (Zang-Hee Cho)[51] היו הראשונים להציע מערכת טבעות שהפכה לאב-טיפוס של PET המוכר לנו כיום.
סורק ה-PET-CT, המיוחס לד"ר דוד טוונסנד (David Townsend) ולד"ר רונאלד נאט (Ronald Nutt), כונה על ידי מגזין TIME כהמצאה הרפואית של שנת 2000.[52]
מחיר
[עריכת קוד מקור | עריכה]החל מחודש אוגוסט 2008, וועדת הטיפול בסרטן של אונטריו מדווחת כי המחיר הממוצע לסריקת PET במחוז הוא כ-1000$-1200$. מחיר זה כולל את עלות התרכובת הרדיואקטיבית וניתוח הסריקה.[53]
בקרת איכות
[עריכת קוד מקור | עריכה]ביצועיה המלאים של מערכות PET יכולות להבדק על ידי מכשירי בקרת איכות כמו Jaszczak phantom.[54]
קישורים חיצוניים
[עריכת קוד מקור | עריכה]- טומוגרפיית פליטת פוזיטרונים, באתר אנציקלופדיה בריטניקה (באנגלית)
הערות שוליים
[עריכת קוד מקור | עריכה]- ^ Bailey, D.L; D.W. Townsend; P.E. Valk; M.N. Maisey (2005). Positron Emission Tomography: Basic Sciences. Secaucus, NJ: Springer-Verlag. ISBN 1-85233-798-2.
- ^ 1 2 Carlson, Neil (22 בינואר 2012). Physiology of Behavior. Methods and Strategies of Research. Vol. 11th edition. Pearson. p. 151. ISBN 0205239390.
{{cite book}}: (עזרה) - ^ 1 2 Exposure fact sheet Health Physics Society
- ^ Khan TS; Sundin A; Juhlin C; Långström B; et al. (2003). "11C-metomidate PET imaging of adrenocortical cancer". European Journal of Nuclear Medicine and Molecular Imaging. 30 (3): 403–410. doi:10.1007/s00259-002-1025-9. PMID 12634969.
- ^ Minn H; Salonen A; Friberg J; Roivainen A; et al. (ביוני 2004). "Imaging of adrenal incidentalomas with PET using (11)C-metomidate and (18)F-FDG". J. Nucl. Med. 45 (6): 972–9. PMID 15181132.
{{cite journal}}: (עזרה) - ^ full text of early article on FDOPA PET for pheochromocytoma
- ^ imaging overview
- ^ Luster M; Karges W; Zeich K; Pauls S; et al. (2010). "Clinical value of 18F-fluorodihydroxyphenylalanine positron emission tomography/computed tomography (18F-DOPA PET/CT) for detecting pheochromocytoma". Eur. J. Nucl. Med. Mol. Imaging. 37 (3): 484–93. doi:10.1007/s00259-009-1294-7. PMID 19862519.
- ^ Agdeppa ED; Kepe V; Liu J; Flores-Torres S; et al. (2001). "Binding characteristics of radiofluorinated 6-dialkylamino-2-naphthylethylidene derivatives as positron emission tomography imaging probes for beta-amyloid plaques in Alzheimer's disease" (PDF). J Neurosci. 21 (24): RC189(1–5). PMID 11734604.
- ^ Mathis CA; Bacskai BJ; Kajdasz ST; McLellan ME; et al. (2002). "A lipophilic thioflavin-T derivative for positron emission tomography (PET) imaging of amyloid in brain". Bioorg. Med. Chem. Lett. 12 (3): 295–8. doi:10.1016/S0960-894X(01)00734-X. PMID 11814781.
- ^ Kuhl DE; Koeppe RA; Minoshima S; Snyder SE; et al. (במרץ 1999). "In vivo mapping of cerebral acetylcholinesterase activity in aging and Alzheimer's disease". Neurology. 52 (4): 691–9. doi:10.1212/wnl.52.4.691. PMID 10078712.
{{cite journal}}: (עזרה) - ^ Kolata, Gina. "Promise Seen for Detection of Alzheimer’s", הניו יורק טיימס, June 23, 2010. Accessed June 23, 2010.
- ^ Catafau AM; Searle GE; Bullich S; Gunn RN; et al. (2010). "Imaging cortical dopamine D1 receptors using 11C NNC112 and ketanserin blockade of the 5-HT 2A receptors". J Cereb Blood Flow Metab. 30 (5): 985–93. doi:10.1038/jcbfm.2009.269. PMC 2949183. PMID 20029452.
- ^ Mukherjee J; Christian BT; Dunigan KA; Shi B; et al. (2002). "Brain imaging of 18F-fallypride in normal volunteers: Blood analysis, distribution, test-retest studies, and preliminary assessment of sensitivity to aging effects on dopamine D-2/D-3 receptors". Synapse. 46 (3): 170–88. doi:10.1002/syn.10128. PMID 12325044.
- ^ Buchsbaum MS; Christian BT; Lehrer DS; Narayanan TK; et al. (2006). "D2/D3 dopamine receptor binding with F-18fallypride in thalamus and cortex of patients with schizophrenia". Schizophrenia Research. 85 (1–3): 232–44. doi:10.1016/j.schres.2006.03.042. PMID 16713185.
- ^ Levivier M; Massager N; Wikler D; Lorenzoni J; et al. (2004). "Use of stereotactic PET images in dosimetry planning of radiosurgery for brain tumors: clinical experience and proposed classification". Journal of Nuclear Medicine. 45 (7): 1146–1154. PMID 15235060.
- ^ Rudd JH; Warburton EA; Fryer TD; Jones HA; et al. (2002). "Imaging atherosclerotic plaque inflammation with [18F]-fluorodeoxyglucose positron emission tomography". Circulation. 105 (23): 2708–11. doi:10.1161/01.CIR.0000020548.60110.76. PMID 12057982.
- ^ Gowrishankar, G.; Namavari, M.; Jouannot, E. B.; Hoehne, A.; et al. (2014). "Investigation of 6-[18F]-fluoromaltose as a novel PET tracer for imaging bacterial infection". PLoS ONE. 9 (9): e107951. doi:10.1371/journal.pone.0107951. PMC 4171493. PMID 25243851.
- ^ Weinstein EA; Ordonez AA; DeMarco VP; Murawski AM; et al. (2014). "Imaging Enterobacteriaceae infection in vivo with 18F-fluorodeoxysorbitol positron emission tomography". Science Translational Medicine. 6 (259): 259ra146. doi:10.1126/scitranslmed.3009815. PMC 4327834. PMID 25338757.
- ^ "Tracing biological pathways | Harvard Gazette". News.harvard.edu. נבדק ב-2012-08-13.
- ^ Rat Conscious Animal PET
- ^ Oi N; Iwaya T; Itoh M; Yamaguchi K; et al. (2003). "FDG-PET imaging of lower extremity muscular activity during level walking". J Orthop Sci. 8 (1): 55–61. doi:10.1007/s007760300009. PMID 12560887.
- ^ Kelloff GJ; Hoffman JM; Johnson B; Scher HI; et al. (אפר' 2005). "Progress and promise of FDG-PET imaging for cancer patient management and oncologic drug development". Clin. Cancer Res. 11 (8): 2785–808. doi:10.1158/1078-0432.CCR-04-2626. PMID 15837727.
{{cite journal}}: (עזרה) - ^ Background Radiation in Denver, Institute for Science and International Security
- ^ Managing Patient Does, ICRP, 30 October 2009.
- ^ de Jong PA; Tiddens HA; Lequin MH; Robinson TE; et al. (במאי 2008). "Estimation of the radiation dose from CT in cystic fibrosis". Chest. 133 (5): 1289–91, author6 reply 1290–1. doi:10.1378/chest.07-2840. PMID 18460535.
{{cite journal}}: (עזרה) - ^ Chapter 9 Occupational Exposure to Radiation, IAEA
- ^ Information for Radiation Workers, Nuclear Regulatory Commission
- ^ Brix G; Lechel U; Glatting G; Ziegler SI; et al. (באפריל 2005). "Radiation exposure of patients undergoing whole-body dual-modality 18F-FDG PET/CT examinations". J. Nucl. Med. 46 (4): 608–13. PMID 15809483.
{{cite journal}}: (עזרה) - ^ Neil Carlson, Physiology of Behavior, 11th edition, Pearson, January 22, 2012, Methods and Strategies of Research, עמ' 151
- ^ Bracco Diagnostics, CardioGen-82, 2000
- ^ Michael E. Phelps (2006). PET: physics, instrumentation, and scanners. Springer. pp. 8–10. ISBN 0-387-34946-4.
- ^ https://www.princeton.edu/~romalis/PHYS312/Positron.pdf
- ^ "PET Imaging". GE Healthcare. אורכב מ-המקור ב-2012-05-04.
- ^ "Invitation to Cover: Advancements in "Time-of-Flight" Technology Make New PET/CT Scanner at Penn a First in the World". University of Pennsylvania. 2006-06-15. אורכב מ-המקור ב-2006-06-28. נבדק ב-2010-02-22.
- ^ Shepp, L.; Vardi, Y. (1982). "Maximum likelihood reconstruction for emission tomography". IEEE Transactions Medical Imaging. 1 (2): 113–122. doi:10.1109/TMI.1982.4307558. PMID 18238264.
- ^ Carson, Lange; Richard Carson (1984). "EM reconstruction algorithm for emission and transmission tomography". Journal of Computer Assisted Tomography. 8 (2): 306–316. PMID 6608535.
- ^ Vardi, Y.; L. A. Shepp; L. Kaufman (1985). "A statistical model for positron emission tomography". Journal of the American Statistical Association. 80 (389): 8–37. doi:10.1080/01621459.1985.10477119.
- ^ Qi, J.; R. Leahy (2006). "Iterative reconstruction techniques in emission computed tomography". Physics in Medicine and Biology. 51 (15): R541–R578. doi:10.1088/0031-9155/51/15/R01.
- ^ "A Close Look Into the Brain". Jülich Research Centre. 7 במרץ 2014. נבדק ב-2015-04-14.
{{cite news}}: (עזרה) - ^ Young H; Baum R; Cremerius U; Herholz K; et al. (1999). "Measurement of clinical and subclinical tumour response using [18F]-fluorodeoxyglucose and positron emission tomography: review and 1999 EORTC recommendations". European Journal of Cancer. 35 (13): 1773–1782. doi:10.1016/S0959-8049(99)00229-4. PMID 10673991.
- ^ July 2003: Trends in MRI | Medical Imaging
- ^ Michael Phelps Talk on PET Scans
- ^ Ter-Pogossian MM; Phelps ME; Hoffman EJ; Mullani NA (1975). "A positron-emission transaxial tomograph for nuclear imaging (PET)". Radiology. 114 (1): 89–98. doi:10.1148/114.1.89. OSTI 4251398. PMID 1208874.
- ^ Phelps ME; Hoffman EJ; Mullani NA; Ter-Pogossian MM (1 במרץ 1975). "Application of annihilation coincidence detection to transaxial reconstruction tomography". Journal of Nuclear Medicine. 16 (3): 210–224. PMID 1113170.
{{cite journal}}: (עזרה) - ^ Sweet, W.H.; G.L. Brownell (1953). "Localization of brain tumors with positron emitters". Nucleonics. 11: 40–45.
- ^ A Vital Legacy: Biological and Environmental Research in the Atomic Age, U.S. Department of Energy, The Office of Biological and Environmental Research, September 2010, p 25–26
- ^ Ido T; Wan CN; Casella V; Fowler JS; et al. (1978). "Labeled 2-deoxy-D-glucose analogs. 18F-labeled 2-deoxy-2-fluoro-D-glucose, 2-deoxy-2-fluoro-D-mannose and 14C-2-deoxy-2-fluoro-D-glucose". Journal of Labelled Compounds and Radiopharmaceuticals. 14 (2): 175–183. doi:10.1002/jlcr.2580140204.
- ^ BROWNELL G.L., Dave Marcum, B. HOOP JR., and D.E. BOHNING, "Quantitative dynamic studies using short-lived radioisotopes and positron detection" in proceedings of the Symposium on Dynamic Studies with Radioisotopes in Medicine, Rotterdam. August 31–September 4, 1945. IAEA. Vienna. 194824. pp. 161–172.
- ^ ROBERTSON J.S., MARR R.B., ROSENBLUM M., RADEKA V., and YAMAMOTO Y.L., ``32-Crystal positron transverse section detector, in Tomographic Imaging in Nuclear Medicine, Freedman GS, Editor. 1983, The Society of Nuclear Medicine: New York. pp. 142–153.
- ^ CHO, Z. H., ERIKSSON L., and CHAN J.K., ``A circular ring transverse axial positron camera in Reconstruction Tomography in Diagnostic Radiology and Nuclear Medicine, Ed. Ter-Pogossian MM., University Park Press: Baltimore, 1975.
- ^ "PET Scan: PET/CT History". Petscaninfo.com. אורכב מ-המקור ב-14 באפריל 2012. נבדק ב-2012-08-13.
{{cite web}}: (עזרה) - ^ Ontario PET Steering Committee (31 באוגוסט 2008), PET SCAN PRIMER, A Guide to the Implementation of Positron Emission Tomography Imaging in Ontario, Executive Summary, pp. iii
{{citation}}: (עזרה) - ^ Jennifer Prekeges. Nuclear Medicine Instrumentation. Jones & Bartlett Publishers. 2012. ISBN 1449645372 p.189
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.

![{\displaystyle {\ce {2-(1-{6-[(2-[18F]fluoroethyl)(methyl)amino]-2-naphthyl}ethylidene)malononitrile ([18F]FDDNP)}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/84835c85f68c3bac721791d0df02b3fa66b4b9af)

![{\displaystyle {\ce {N-methyl-[11C]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/481dbf14a6c7aeef6a3fc6262a207eafcf1fcdc2)