אמוניה
 | |||
| |||
| שם סיסטמטי | Azane NH3 | ||
|---|---|---|---|
| שמות נוספים |
נַשְׁדּוּר אמונייק Hydrogen nitride Nitro-Sil Vaporole | ||
| כתיב כימי |
NH₃ | ||
| מסה מולרית | 17.0306 גרם/מול | ||
| מראה | גז חסר צבע בעל ריח חריף | ||
| מספר CAS | 7664-41-7 | ||
| צפיפות | 0.0006942[דרושה הבהרה] גרם/סמ"ק | ||
| מצב צבירה | גז | ||
| מסיסות |
במים[1] 47% (0 °C) 31% (25 °C) 18% (50 °C) | ||
| טמפרטורת היתוך |
-77.73 °C 195.42 K | ||
| טמפרטורת רתיחה |
-33.34 °C 239.81 K | ||
| חומציות | 9.21±0.01 | ||
| בסיסיות | 4.75 (בתגובה עם H2O) pKb | ||
| אנתלפיית התהוות סטנדרטית | −45.94 קילוג'ול למול | ||
| אנטרופיה מולרית תקנית | 192.5±0.05 ג'ול למול־קלווין | ||
| LD50 | 7±1 gram per cubic metre, 4,600±1 milligram per cubic metre, 4,500±1 חלקים למיליון, 4,230±1 חלקים למיליון, 21,430±1 חלקים למיליון, 7±1 gram per cubic metre, 18,600±1 milligram per cubic metre, 7,040±1 milligram per cubic metre, 2,000±1 חלקים למיליון, 17,401±1 חלקים למיליון, 9,500±1 חלקים למיליון, 40,300±1 חלקים למיליון, 28,595±1 חלקים למיליון, 20,300±1 חלקים למיליון, 11,590±1 חלקים למיליון, 7,338±1 חלקים למיליון, 4,837±1 חלקים למיליון, 9,859±1 חלקים למיליון, 2,000±1 חלקים למיליון | ||



אָמוֹנְיָה (Ammonia; נקראת גם נַשְׁדּוּר, בעבר גם אמונייק) היא תרכובת חנקן ומימן, ונוסחתה NH3. האמוניה היא אחד הכימיקלים התעשייתיים הנפוצים והחשובים בעולם. שימושה העיקרי הוא כחומר גלם בתעשיית הדשנים, ובייצור תרכובות חנקן. בביולוגיה משמשת האמוניה כחומר ראשוני ליצירת בסיסים חנקניים (המרכיבים את הנוקלאוטידים) וחומצות אמינו.
האמוניה מופיעה בטבע בכמות קטנה כחלק ממחזור החנקן בקרקע, וכתוצר פירוק של השתנן שבשתן, ועל כן ריחה מזוהה עם ריח משתנות לא נקיות. בתעשייה מיוצרת האמוניה מחנקן, שמקורו באוויר, וממימן, שמקורו בגז טבעי, בתהליך הבר-בוש.
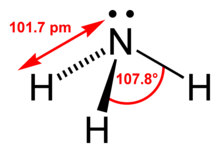
בתנאי לחץ וטמפרטורה תקניים, האמוניה היא גז חסר צבע ובעל ריח חריף. גז האמוניה קל מהאוויר, והוא בעל מסיסות גבוהה מאוד במים. מולקולת האמוניה מתפקדת כבסיס בשל נטייתה לקלוט פרוטון ולהפוך ליון אמוניום (NH4+), ולכן תמיסות מימיות של אמוניה הן בסיסיות.
האמוניה רעילה לבני אדם ובעלי חיים, ועלולה אף לגרום למוות, ועל כן נדרשים כללי בטיחות מחמירים בעת ייצור, הובלה, אחסון ושימוש באמוניה.
היסטוריה
[עריכת קוד מקור | עריכה]מראשית המאה ה-19 עקב הגידול באוכלוסיית העולם והתיעוש ההולך וגדל של מדינות המערב גבר הצורך למצוא מקורות חדשים לאספקת חנקן לקרקע החקלאית בצורה של דשנים. בתחילה נפתרה הבעיה בעזרת גילוי של מינרלים חנקתיים בצ'ילה (בעיקר NaNO3). המסחר במלחת צ'ילה הלך וגדל במהירות החל מ-1830. כבר בתחילת המאה ה-20 היה ברור, כי לא ניתן יהיה לספק באמצעות מינרל טבעי זה את כל תצרוכת תרכובות החנקן של העולם המודרני הדרושה הן למטרות חקלאיות, כדי לספק מזון לאוכלוסייה ההולכת וגדלה בקצב אדיר, והן לצורכי התעשייה המתפתחת בצעדי ענק.
בתחילת המאה ה-20 ניתן היה להשיג חלק מהאמוניה או תרכובותיה כתוצר לוואי של תהליכים תעשייתיים שונים, אך גם באלה לא היה די כדי לספק את כל צורכי השוק.
תהליך הבר-בוש
[עריכת קוד מקור | עריכה] ערך מורחב – תהליך הבר-בוש
ערך מורחב – תהליך הבר-בוש
בראשית המאה ה-20 החלו המדענים הגרמניים פריץ הבר וקארל בּוֹש בפיתוח של שיטה סינתטית לייצור של אמוניה. האבר ובוש ביקשו להשתמש בשני חומרי גלם זולים ונפוצים לייצור אמוניה (חנקן - שמקורו מהאוויר ומימן - שמקורו מהמים או ממקורות פחמניים כגון גז טבעי, נפט ופחם). הקושי הגדול בייצור האמוניה היה באדישות הכימית הגבוהה של החנקן שנובע מקיומם של שלושה קשרים קוולנטים המחברים בין שני אטומי חנקן. הבר ובוש הבינו שעל מנת להתגבר על בעיה זו ועל מנת להשיג שליטה מלאה על קינטיקת התגובה לייצור האמוניה, יש צורך בתכנון ריאקטור כימי בו יופעלו תנאי לחץ וטמפרטורה אידיאליים להתרחשות התגובה ובמציאת זרז כימי מתאים שיאפשר את הורדת אנרגיות השפעול הגבוהה הנדרשת להתרחשות התגובה.
הבר היה זה אשר הגה את הרעיון ויצר את התשתית המדעית והמעבדתית לתהליך זה, אך קארל בוש היה זה אשר פיתח את התהליך מבחינה טכנולוגית והביא להגשמתו כתהליך כלכלי בקנה מידה תעשייתי.
הבר בחן שורה ארוכה של זרזים החל מאורניום ואסמיום ששימשו בשלבי הניסוי הראשונים ועד ניקל, סידן, מנגן, ברזל ועד רבים (סה"כ נבחנו אלפי זרזים שונים). לבסוף נבחרה תחמוצת הברזל, והחומר משמש גם בימנו כזרז בתהליך. למעשה תהליך הייצור שפיתחו הבר ובוש משמש עד היום לייצור אמוניה, כמעט ללא שינוי. הלחץ שנבחר אז לביצוע התהליך היה 200 אטמוספירות, שהוא הלחץ המרבי שניתן היה להשיג אז (כיום הלחץ המשמש הוא כ-300 אטמוספירות), והטמפרטורה שנבחרה הייתה כ-500 מעלות צלזיוס.
על תהליך ייצור האמוניה קיבל פריץ הבר את פרס נובל לכימיה לשנת 1918. כ-13 שנים אחר כך, בשנת 1931, קיבל שותפו, קארל בוש את פרס נובל בכימיה, על תרומתו בפיתוח שיטות לעבודה בתנאי לחץ גבוה בעת שלבי התיעוש של תהליך ייצור האמוניה.
ייצור עולמי
[עריכת קוד מקור | עריכה]נכון ל־2020, הייצור העולמי של אמוניה עומד על כ־150 מיליון טון[2], כאשר סין היא היצרן הגדול ביותר (כרבע מכלל הייצור העולמי). ישנו עודף כושר ייצור של אמוניה בעולם, בהשוואה לביקוש. מחיר האמוניה רגיש בעיקר לשינויים במחיר גז טבעי, שהוא חומר הגלם העיקרי כיום ליצור אמוניה, ובמחירי האנרגיה.
שימושים באמוניה
[עריכת קוד מקור | עריכה]האמוניה חיונית ליצור תעשייתי כחומר גלם וכאמצעי לקירור בבתי קירור ומחסני מזון. השימושים העיקריים באמוניה הם:
- דשנים: כ-80% מכלל ייצור האמוניה בעולם מיועד לתעשיית הדשנים. האמוניה מהווה חומר גלם עיקרי בייצור של דשנים חשובים, כגון אמוניום חנקתי (NH4NO3) ואשלגן חנקתי (KNO3). האמוניה משמשת כשלעצמה כדשן להעשרת קרקעות עניות בחנקן, עת היא מומסת בריכוז נמוך במים ומסופקת לקרקע בצורה ישירה.
- ייצור חומצה חנקתית: התהליך התעשייתי החשוב ביותר שנעשה בו שימוש באמוניה הוא הפקת חומצה חנקתית. האמוניה מוזרמת ביחס של חלק אחד של אמוניה לתשעה חלקים של אוויר מעל זרז פלטינה בטמפרטורה של כאלף מעלות צלזיוס, ומחומצנת לחד-תחמוצת החנקן ולמים. הזרז חשוב ביותר, שכן התוצרים היציבים יותר בחמצון של אמוניה הם חנקן ומים. החומצה החנקתית חשובה ביותר לייצור דשנים וחומרי נפץ.
- ייצור סיבים סינתטיים (כגון ניילון).
- ייצור חומרי צבע המבוססים על תרכובות אורגניות.
- ייצור תרופות.
- גז קירור: לפני גילוי הפריאון, הייתה האמוניה חומר פופולרי במערכות קירור. השימוש למטרה זו הופסק בשל רעילות, ובשל יצירת קורוזיה במגע עם נחושת, הנפוצה כחומר גלם לצינורות במערכות קירור. עם זאת, במכונות גדולות לייצור קרח ולעיבוד מזון בהקפאה, עדיין נעשה שימוש באמוניה כקרר, בשל תכונותיה התרמודינמיות העדיפות. גם במקרר של איינשטיין נעשה שימוש באמוניה כקרר.
- דלק[3]: מטוסי רקטה כ-X-15 הופעלו באמוניה. בשנת 1981 הסבה חברה קנדית מכונית שברולט אימפלה רגילה לתדלוק באמוניה. אמוניה היא חומר הגלם העיקרי בייצור של אוריאה (שתנן) המשמשת כתוסף דלק למנועי דיזל.
בטיחות
[עריכת קוד מקור | עריכה]במצבה הגזי, האמוניה חסרת צבע ובעלת ריח חריף. בשל ריחה החריף, קל לזהותה באוויר אפילו בריכוזים נמוכים של כ-5 ppm. כמויות קטנות של אמוניה אינן בעלות השפעה מזיקה על האדם, אך בכמויות גדולות היא עלולה להיות מסוכנת ביותר. האמוניה היא חומר רעיל, המגרה את אברי הנשימה, ועלול לגרום לכוויות בעור ובעיניים. גירוי הלחמית וריריות דרכי הנשימה נגרם בריכוז נמוך יחסית, של 50 ppm, בעוד שתסמינים ריאתיים ניכרים בריכוזים העולים על 1000 ppm, עד להסתמנות קטלנית בריכוזים של כ-1500 ppm. הכווייה מאמוניה שבריכוזים גבוהים גורמת לנמק נוזלי (Liquefaction necrosis) ברקמות הפגועות[4].
האמוניה גורמת לקורוזיה במתכות מסוימות, כגון נחושת, ועל כן אין לאחסן או להעביר אמוניה בצנרת או במכלי נחושת. בשל הסיכון הסביבתי והביטחוני הנשקף מהאמוניה, מכלי אמוניה בעולם נדרשים לעמידה בתקני בטיחות שונים למניעת דליפות.
השפעה ביולוגית
[עריכת קוד מקור | עריכה]האמוניה נוצרת באופן נורמלי בגוף חי בתהליך חילוף החומרים של חומצות אמינו. בריכוזים גבוהים האמוניה רעילה ולכן היא מפורקת על ידי הכבד בתהליך מורכב לשתנן, המסולק באמצעות הכליות אל השתן. הצטברות של אמוניה בדם בשל הפרעה לתהליך זה נקראת היפראמונמיה והיא תופעה מסוכנת שעשויה לגרום אף למוות.
בנוסף, היווצרות אמוניה היא תופעת לוואי באקווריומים בהם מגדלים דגים. האמוניה נוצרת על ידי ההפרשות של דגי הנוי.
שאיפת אמוניה בכמויות קטנות הייתה בעבר שיטה מקובלת להעיר אנשים מעלפונם. שאיפת אמוניה בריכוזים העולים על 25–35 חלקים למיליון עשויה לגרום לנזק חמור לריאות ואף למוות.
בישראל
[עריכת קוד מקור | עריכה]בעבר היה ייצור אמוניה בישראל, אך זה הופסק במהלך שנות ה־80, ומאז מיובאת האמוניה ממדינות אחרות. האמוניה המיובאת לישראל עוברת דרך מסוף הכימיקלים בנמל הקישון במפרץ חיפה, שלצידו הוקם מכל אחסון גדול המכיל עד 12,000 טון. מכל אחסון זה קרוב יחסית לריכוזי אוכלוסייה במטרופולין חיפה, ומאוים ביטחונית עקב קרבה יחסית לגבול לבנון. עם זאת, ועדה ציבורית שבדקה את נושא אחסון החומרים הרעילים במפרץ חיפה בעקבות מלחמת לבנון השנייה, הגיעה למסקנה כי אמצעי המיגון במכל מספקים.
נכון לשנת 2017, צריכת האמוניה בישראל היא כ־120,000 טון לשנה[5]. אחסון האמוניה נעשה במכל במפרץ חיפה, ובמכלים קטנים יותר בשטחי מפעלים הצורכים את החומר. השימוש העיקרי (כ־80%) באמוניה בישראל הוא לייצור דשן ובהיקפים קטנים יותר לייצור חומצה חנקתית (כ־8%), וניילון (כ־5%). שאר הכמות (כ-7%) משמשת למגוון שימושים, כדוגמת ייצור חומרי נפץ, תרופות, קירור ועוד.
הייבוא לישראל נעשה על ידי מפעל חיפה כימיקלים, שבבעלותו גם מכל האחסון במפרץ חיפה, ממנו נמשכת צנרת הובלה למפעל חיפה כימיקלים במפרץ חיפה ולמפעל דשנים וחומרים כימיים הסמוך. היבוא נעשה באמצעות משלוח חודשי של כ־10,000 טון אמוניה הנאגר במכל, ומוזרם בהדרגה בצנרת אל המפעלים. חיפה כימיקלים צורך כ־70% מהכמות המיובאת לישראל בשני מפעליו במפרץ חיפה ובנגב, כאשר אל המפעל בנגב מובלת האמוניה באמצעות מכליות כביש. יתר הכמות מגיעה למפעל דשנים המשתמש ברובו, ומשווק כ־4% מסך הכמות המיובאת לארץ (כ־5,000 טון) לצרכנים קטנים יחסית באמצעות מכליות כביש ומכלי אחסון קטנים.
ב-6 בנובמבר 2014 אירעה דליפת גז מסוג אמוניה במפעל באזור עמק חפר עקב חיתוך שגוי של צינור במהלך עבודות שנעשו על ידי קבלן חיצוני. במהלך הטיפול באירוע נהרג כבאי ונפצעו 21 אנשים עקב חשיפה לאמוניה[6].
ב-1 ביוני 2015 בית המשפט העליון קבע כי על הממשלה להודיע עד תום תקופה של 45 ימים, על התאריך בו יפונה מיכל האמוניה.
בפברואר 2016 הודיע חסן נסראללה כי בכוונתו לשלוח טילים ולכוונם למיכל האמוניה בחיפה, שיש בו 15,000 טון של גז, והדבר יגרום להרג של עשרות אלפי אנשים. למעשה, טען, מאוימים באזור 800,000 אזרחים. במלחמת לבנון השנייה החליט שלא לפגוע בהם, ועתה, אם ישראל תתקוף יפעיל כוחו זה[7].
ביולי 2017 רוקן מיכל האמוניה ונסגר מפעל חיפה כימיקלים[8]. במרץ 2019 הודיעה הממשלה כי יבוא האמוניה לא יעבור יותר בצפון המדינה[9].
קיים תכנון להקמת לצורך אספקת הביקוש המקומי, בעקבות מציאת מאגרי גז טבעי גדולים בסמוך לישראל. הקמת מפעל זה תאפשר להשבית את מכל האחסון במפרץ חיפה.
בדצמבר 2020 התפרסם כי קבוצת חיפה חתמה על חוזה מול חברת SAIPEM האיטלקית במסגרתו תקים החברה מפעל לייצור אמוניה במישור רותם בנגב. המפעל צפוי להיות בעל תפוקה של כ-100,000 טון אמוניה בשנה וישמש את קבוצת חיפה לשיווק בישראל ובחו"ל. ההשקעה של קבוצת חיפה בפרויקט נאמדת בכ-200 מיליון דולר.[10]
קישורים חיצוניים
[עריכת קוד מקור | עריכה]- הערך "אמוניה - Ammonia", באתר ויקירפואה
 תהליך הבר-בוש לייצור אמוניה, Royal Society of Chemistry, סרטון באתר יוטיוב
תהליך הבר-בוש לייצור אמוניה, Royal Society of Chemistry, סרטון באתר יוטיוב- אבני דרך, עשר ההמצאות הטכנולוגיות הגדולות, באתר ifeel
- הכל על האמוניה באתר הידען
- בחינת חלופות למערך היבוא, האחסון, הניפוק והשינוע של אמוניה במפרץ חיפה, דו"ח שהוגש למשרד להגנת הסביבה, 2010.
- לביא ביגמן, אמוניה: לא רק חומר מסוכן, במדור "מדע במבט-על" באתר של מכון דוידסון לחינוך מדעי, 12 באפריל 2017
- אמוניה, באתר אנציקלופדיה בריטניקה (באנגלית)
 אמוניה, דף שער בספרייה הלאומית
אמוניה, דף שער בספרייה הלאומית
הערות שוליים
[עריכת קוד מקור | עריכה]- ^ Budavari, Susan, ed. (1996). The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (12th ed.). Merck. ISBN 0-911910-12-3.
- ^ US Gelogical Survey, Mineral Commodits Summary 2015
- ^ אמוניה "ירוקה" תוכל לשמש כדלק עתידי, באתר הידען, 5 במרץ 2020
- ^ "אמוניה ומלחי אמוניום – תרופה ורעל?", באתר האיגוד הישראלי לנוירוטוקסיקולוגיה
- ^ חלופות יישומיות למשק האנרגיה, פברואר 2017
- ^ שלומי גבאי, אבי אשכנזי ודנה ירקצי, דליפת אמוניה בשרון: כבאי נהרג ו-21 נפגעו, באתר וואלה, 7 בנובמבר 2014
- ^ נסראללה מאיים: "מיכל האמוניה בחיפה הוא הפצצה הגרעינית שלי", באתר כיכר השבת, 17 בפברואר 2016
- ^ מיכל פעילן, אחרי כ-30 שנה: מכל האמוניה ריק, באתר מאקו, 19 בספטמבר 2017
- ^ יבוא האמוניה לא יעבור יותר בצפון המדינה
- ^ ליאור גוטמן, SAIPEM האיטלקית תקים ל"קבוצת חיפה" מתקן לייצור אמוניה במישור רותם, באתר כלכליסט, 23.12.2020


