אפיגנטיקה
ערך ללא מקורות
| ||
| ערך ללא מקורות | |
אפיגנטיקה (באנגלית: Epigenetics) הוא התחום בביולוגיה העוסק בשינויים בתפקוד הגנים שאינם כרוכים בשינוי רצף ה-DNA עצמו. אפי-(מיוונית: ἐπι - מעל, מחוץ) מרמז שאין כלל שינוי ברצף הגנטי של ה-DNA, אלא רק בעיצוב ביטוים של גנים מסוימים, החלשה או חיזוק של גנים, וכדומה. המונח מתייחס לרוב לשינויים ברמת הכרומוזום המשפיעים על הפעילות והביטוי של גנים, אך ניתן להרחיב את המונח לכל פנוטיפ תורשתי שאינו נובע משינוי ברצף ה-DNA, כגון פריונים. שינויים אלו יכולים לנבוע כתוצאה משלבי התפתחות טבעיים, וכן ממשובים חיצוניים מהסביבה ומהעולם (כדוגמת דיאטה, לחץ נפשי ועוד).
שינויים בעלי השפעה על תפקוד הגנום, שאינם כרוכים בשינוי רצף ה-DNA, יכולים להתרחש כתוצאה ממספר רב של מנגנונים. לדוגמה, מתילציה של רצף ה-DNA וקוד היסטונים, אשר משפיעים על ביטוי הגנים בלי שהרצף עצמו משתנה. שינויים כאלה ניתנים להורשה דרך שלבי מחזור החיים של התא. דוגמה לתהליך כזה הוא תהליך התמיינות התאים. בתהליך המורפוגנזה, תא גזע פלוריפוטנטי מתחלק ויוצר תאי גזע מולטיפוטנטיים, אשר שמתחלקים ויוצרים סוג מסוים של תאים. כלומר, מתא אחד מופרה, הזיגוטה, מתקבלים תאי בת עם אותו רצף DNA, אך עם תפקידים שונים, כגון תאי עצב, תאי שריר, כלי דם וכדומה, הנבדלים זה מזה במגוון הגנים המבוטאים. מצב זה מתקבל בעזרת שינויים אפיגנטיים אשר מפעילים ומחזקים גנים מסוימים ומדכאים אחרים.
מבחינה היסטורית, המונח שימש לתיאור תופעות שהן לא בהכרח תורשתיות, אך נכללו במונח מכיוון שאינן גורמות לשינוי ברצף ה-DNA עצמו. לדוגמה, כל שינוי של כרומוזומים, בייחוד על היסטונים, בין אם זהו שינוי תורשתי ובין אם לא, בין אם זה משפיע על הפנוטיפ ובין אם לא, הוגדר כשינוי אפיגנטי. כיום מקובל כי התופעה חייבת להיות ניתנת להורשה כדי להיכנס להגדרה של אפיגנטיקה. שימוש בלתי תקין במונח על ידי אנשים שאינם בקיאים גרם לכך שהתקבעה בתודעה הציבורית הגדרה שגויה של המושג ולמחלוקות ציבוריות.
הגדרת המושג[עריכת קוד מקור | עריכה]
המונח כפי שאנו מכירים אותו כיום הופיע בשנות ה-90, אז נעשה שימוש בו בכמה משמעויות שונות. ההגדרה המוסכמת כיום של המושג אפיגנטיקה כפנוטיפ יציב, תורשתי, הנובע משינוי בכרומוזום ללא שינוי ברצף ה-DNA. הגדרה זו התקבלה בכנס של ה-Cold Spring Harbor בשנת 2008, אם כי יש אחרים המשתמשים בהגדרות אשר כוללות תופעות שאינן מורָשות.
מקור המונח[עריכת קוד מקור | עריכה]
מבחינה היסטורית, משמעות המונח אפיגנזיס הוא צמיחה נוספת, והוא נמצא בשימוש באנגלית מהמאה ה-17. משמעות הקידומת היוונית אפי היא בין השאר "בנוסף", ואכן האפיגנטיקה עוסקת בשינויים הנוספים אשר מתרחשים בנוסף לשינויים הגנטיים ה"רגילים" ב-DNA. את השימוש המודרני הראשון במושג אפיגנטיקה מייחסים לקונרד הל וודינגטון (Conard Hal Waddington), שבשנת 1942 הגדיר את האפיגנזה כתהליך שבו תאי גזע מתמיינים לסוג תא מסוים במהלך ההתפתחות העוברית. באותה תקופה לא היה קיים ידע רב על הגנים ותפקידם בתורשה; וודינגטון השתמש בו כמודל רעיוני כדי להסביר כיצד גנים יוצרים יחסי גומלין עם סביבתם כדי להוביל לפנוטיפ. הוא השתמש במונח נוף אפיגנטי (epigenetic landscape) כמטאפורה להתפתחות עוברית. וודינגטון סבר כי גורלו של תא מסוים נקבע בצורה דומה לזו של כדור המתגלגל מראש הר אל הנקודה הנמוכה ביותר בסביבה (ידוע כתאוריית התיעול של וודינגטון). הוא הציע לראות את תהליך ההתמיינות הבלתי הפיך של התא כסביבה של רכסים ועמקים, שביניהם מתגלגל כדור (המדמה את התא). כיום מודל זה משמש בתחומי מחקר של התמיינות תאים, בגישה החוקרת את דינמיות המערכות הקובעות את גורל התא. לפי גישה זו ישנה דינמיות מסוימת בגורלם של התאים המתחלקים, התלוי בגורמי משיכה מסוימים (כגון נקודת שיווי משקל והגבלת מחזור התא) או תנודות.
פסיכולוגיה התפתחותית[עריכת קוד מקור | עריכה]
בפסיכולוגיה התפתחותית שימש המונח אפיגנטיקה לתיאור התפתחות פסיכולוגית הנובעת מהשפעה מתמשכת, דו כיוונית, בין התורשה לסביבה. מספר תאוריות התפתחותיות נדונו בצורות שונות ובשמות שונים במאות ה-19 וה-20. תאוריה מוקדמת, הוצעה, כחלק מהצהרות היסוד של האמבריולוגיה על ידי קארל ארנסט פון בר, אשר הפכה נפוצה בזכות ארנסט הקל. תאוריה אפיגנטית רדיקלית (אפיגנזה פיזיולוגית) פותחה על ידי פול וינטרברט. תאוריה נוספת, אפיגנזה הסתברותית, הוצגה על ידי גילברט גוטליב בשנת 2003. השקפה זו כוללת את כל הגורמים ההתפתחותיים המשפיעים על האורגניזם, כיצד הם משפיעים זה על זה, וכיצד האורגניזם משפיע על ההתפתחות העצמית שלו.
ההגדרה הביולוגית כיום[עריכת קוד מקור | עריכה]
ישנן הגדרות רבות למונח, כאשר נקודת מחלוקת בין החוקרים היא האם לכלול את הדרישה שהשינוי יהיה תורשתי. לדוגמה, רובין הולידיי הגדיר את המונח כ"מחקר של מנגנוני הבקרה התלויים בזמן ובמרחב אשר מבקרים את הפעילות של גנים במהלך ההתפתחות של יצורים מורכבים", ואדריאן בירד הגדיר את המונח כ"התאמה מבנית של אזורים כרומוזומליים כדי לרשום, לאותת או להנציח מצבי פעילות שהשתנו". הגדרה זו כוללת בתוכה שינויים זמניים הקשורים למנגנוני תיקון נזקי DNA או למחזור התא בנוסף לשינויים מורָשים אחרים, ולא כוללת שינויים הקשורים למבנה הקרום או פריונים, במידה והם לא פגעו בתפקוד הכרומוזום. הגדרות אלו לא מקובלות בקרב החוקרים. מקובל להשתמש בהגדרה מחמירה יותר, כמו זו שנוסחה על ידי ארתור ריגס ועמיתיו, "המחקר של שינויים מורָשים בפעילות גנים – שינויים שעוברים בתורשה בתהליך המיטוזה ו/או המיוזה – שאינם יכולים להיות מוסברים על ידי שינויים ברצף ה-DNA". מיזם מפת הדרכים האפיגנומית של ה-NIH משתמש בהגדרה זו: "שינויים תורשתיים בפעילות וביטוי גנים (בצאצאי התא או הפרט), וכן שינויים יציבים לאורך זמן של הפוטנציאל השיעתוקי של התא, שלא בהכרח תורשתיים".
הדמיון בין המונח אפיגנטיקה לגנטיקה יצר שימושים רבים מקבילים. לדוגמה, המונח אפיגנום מקביל למונח גנום, ומתייחס למצב האפיגנטי הכללי של התא. בעוד הגנום בכל התאים באורגניזם הוא זהה (פרט למוטציות בתאים סומטיים), האפיגנום שונה בין סוגי תאים מסוימים, ולעיתים אף בין תאים מאותו הסוג. אפיגנומיקה מקבילה לגנומיקה, ומתייחסת לתחום החוקר שינויים אפיגנטיים גלובליים ברחבי הגנום. הקוד האפיגנטי מקביל לקוד הגנטי, ומתאר את התכונות האפיגנטיות היוצרות פנוטיפים שונים בתאים שונים המכילים את אותו רצף DNA (לדוגמה, ישנו קוד אפיגנטי שונה המבדיל בין תא עצב לתא T). ניתן להרחיב את משמעות המונח 'הקוד האפיגנטי' באופן קיצוני ולכלול בו את מלוא מצבו של התא, אך בדרך כלל המונח מתייחס למאמצים שיטתיים למדוד צורות ספציפיות ורלוונטיות של מידע אפיגנטי.
פסאודו-מדע[עריכת קוד מקור | עריכה]
היות שהאפיגנטיקה נמצאת בשלבים מוקדמים של התפתחותה כמדע, והדיווח עליה מושפע מנטיית התקשורת לחפש סנסציות, מספר מדענים הזהירו מפני הפצה של מסקנות שגויות ופסאודו-מדעיות על ידי כותבים מתחום העידן החדש, המעלים השערות בלתי מבוססות שניתן לשלוט בפעילות הגנים ובבריאות של אדם באמצעות שטיפת מוח. שימוש שגוי במונח על ידי שרלטנים רפואיים הביא להפצת מידע שגוי בציבור.
הבסיס המולקולרי[עריכת קוד מקור | עריכה]
שינויים אפיגנטיים משפיעים על רמות הפעילות והביטוי של גנים, אך לא על רצף ה-DNA עצמו. הארגון של ה-DNA (לא הקוד) יכול להשתנות, וכן החלבונים הקשורים בכרומטין, ודברים אלו יכולים לגרום לביטוי או לדיכוי פעילות גנים. דבר זה מאפשר לתאים שונים בתוך אותו יצור לבטא מערכת שונה של גנים כתלות בצורכי התא הייחודיים. השינויים האפיגנטיים נשמרים כאשר תאים מתחלקים. רוב השינויים האפיגנטיים מתרחשים במהלך חיי היצור, אך ישנה גם אפשרות של העברת שינויים אלו לצאצאים, בתהליך הנקרא תורשה אפיגנטית בין דורית.
ישנם תהליכים אפיגנטיים רבים, בהם פאראמוטציות, סימון גנים, החתמה גנומית, השתקת גנים, השתקה של כרומוזום X, השפעת המיקום, מתילציות על ה-DNA, טרנסבקציה, השפעות אימהיות, תהליכים קרצינוגניים, תהליכים טרטולוגיים, בקרת שינויים בהיסטונים, בקרת רצפי הטרוכרומטין ועוד.
נזקי DNA יכולים גם להשפיע על האפיגנטיקה של התא. DNA ניזוק באופן תדיר, כ-60,000 פגיעות ביום בתא באדם. רוב הנזקים האלו מתוקנים על ידי מנגנוני התיקון של התא רק ברמת רצף ה-DNA, ולא בהכרח ברמת האפיגנטיקה. באופן ספציפי, שבר דו גדילי ב-DNA עלול להוביל להשתקה של הגן על ידי מתילציה של ה-DNA המתוקן או לגרום לשינוי בהיסטונים. בנוסף, האנזים Parp1 (poly(ADP)-ribose polymerase) והתוצר שלו PAR (poly(ADP)-ribose) מצטברים באזור השבר כחלק ממנגנון התיקון. ההצטברות שלהם גורמת לגיוס והפעלה של מעצב כרומטין בשם ALC1 שיכול להזיז את הנוקליאוזומים בסביבה ולגרום להשתקת הגן. לתוצאה דומה יכולים גם להוביל כימיקלים שונים הפוגעים ב-DNA, כגון בנזן, סטירן וטריכלורואתילן, שגורמים לירידה ברמת המתילציה של גנים, לעיתים דרך הפעלה של מסלולי תגובה לעקת חמצון.
סוגי מזון שונים משפיעים על המצב האפיגנטי של חולדות. מרכיבי מזון מסוימים מגבירים את הביטוי של חלבוני תיקון DNA שונים. מרכיבים אחרים מונעים נזקי DNA, כגון אנתוציאנינים מאוכמניות ואיזופלבונים מסויה.
המחקר האפיגנטי משתמש במגוון רחב של טכניקות ביולוגיות מולקולריות כדי לקדם את הבנתנו את תופעות האפיגנטיקה, ובהם מיצוי נוגדני של כרומטין (והשיטות הנגזרות ממנה – ChIP on chip, ChIP-seq), נגישות כרומטין, מיקום נוקליאוזומים, היברידיזציה פלואורסצנטית באתר, אנזימי הגבלה הרגישים למתילציות וריצוף ביסולפט. השימוש בשיטות מתחום הביואינפורמטיקה הולך וגובר, ויוצר תחום של אפיגנטיקה חישובית.
מנגנונים אפיגנטיים[עריכת קוד מקור | עריכה]
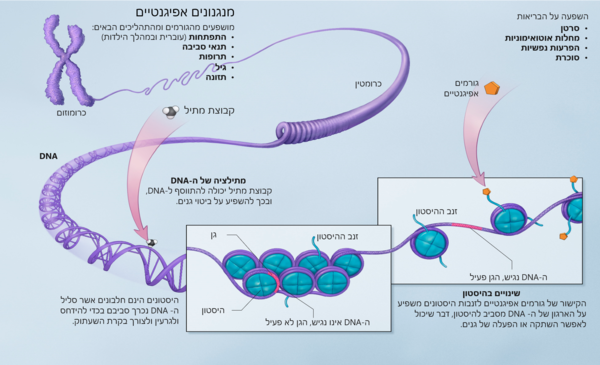
מספר תהליכים תאיים נופלים תחת הקטגוריה של תהליכים אפיגנטיים:
- תהליכים הקשורים ב-DNA – שינויים קוולנטיים של ה-DNA (כגון מתילציה של ה-DNA) ושל ההיסטונים (כגון אצטיליציה של ליזין, מתילציה של ליזין וארגינין זרחון של סרין ותריאונין) מעורבים בתהליכים רבים של תורשה אפיגנטית.
סליל ה-DNA נכרך סביב חלבוני ההיסטונים כדי ליצור כרומטין. הפנוטיפ של יצורים מושפע מהגנים שמבוטאים, וישנו קשר בין הקיפול של גנים לבין רמת הביטוי שלהם. לפיכך, צורת הכריכה של סליל ה-DNA סביב ההיסטונים משפיעה על הפנוטיפ של התא. מצב זה הוא דינמי, ויכול להשתנות באמצעות חלבונים מעצבי כרומטין, אשר פועלים בשני מנגנונים עיקריים:
1. שינויים לאחר תרגום על חומצות האמינו של ההיסטונים. לחלבוני ההיסטונים יש שיירים ארוכים המורכבים מחומצות אמינו, ושינויים בהם יכולים להשפיע על צורת ההיסטון עצמו, וגם על אופן כריכת ה-DNA. במהלך תהליך השכפול, ההיסטונים אינם משתנים, ובכך יכולים להשפיע על אופן כריכת ה-DNA החדש. היסטונים אלה משמשים גם כתבניות עבור היסטונים חדשים המיוצרים כדי לשמור על השינויים הללו, שמוודאים שאופן כריכת ה-DNA מתאים לסוג התא הרצוי.
2. מתילציה של ה-DNA – לרוב באתרי CpG, כך שהציטוזין נהיה 5-מתיל-ציטוזין, אשר לרוב מתנהג כמו ציטוזין שאינו ממותל. אך כאשר ישנה כמות גבוהה של מתילציה באזור מסוים, הוא לרוב פחות מבוטא. תבנית המתילציה של ההורים יכולה להיות מועברת לזיגוטה, המסמנת איזה אלל יבוטא בצאצא (ראו החתמה גנומית). מנגנון הפעולה של המתילציה על ה-DNA נחקר היטב, ותלוי באנזימים אשר יודעים לזהות מצב בו בגדיל אחד של ה-DNA יש מתילציה, ולעשות מתילציה על הגדיל המשלים.
- תהליכים התלויים בתעתיקי RNA – לעיתים, גן משעתק מקטע RNA המבקר את פעילות הגן בצורה ישירה או עקיפה, באמצעות גיוס ספציפי של קומפלקסים המשנים את הכרומטין. ישנם שינויים נוספים המתווכים באמצעות קטעי RNA קצרים או באמצעות יצירת RNA Interference. כאשר תא מתחלק, גם ה-RNA יתחלק בין תאי הבת, גם אם הגירוי המקורי ליצירת ה-RNA לא קיים בתאי הבת. ה-RNA יכול גם לעבור בין תאים סמוכים באמצעות דיפוזיה. אֵם מעבירה לזיגוטה כמות גדולה של RNA וחלבונים במהלך האואוגנזה, דבר המוביל להשפעות אימהיות. לאחרונה התגלה כי גם האב מעביר כמות מועטה של RNA שיכולה להשפיע בצורה אפיגנטית על מספר דורות.
- תהליכים התלויים במיקרו רנ"א – מיקרו RNA הם חלק ממשפחת ה-RNA שאיננו מקודד, ובאורך שבין 17 ל-25 נוקילאוטידים, אשר מבקרים מספר רב של תהליכים ביצורים רבים. כל רצף קצר כזה יכול לבקר מאות רבות של מרנ"א ולשלוח אותם לפירוק. מחקרים מראים כי כ-60% מהגנים האנושיים מבוקרים על ידי מיקרו רנ"א. רבים מהמיקרו רנ"א מבוקרים בצורה אפיגנטית. בכ-50% מהגנים של המיקרו רנ"א ישנם איי CpG, שיכולים לדכא שעתוק כאשר הם עוברים מתילציה. שעתוק מאזורים שעברו מתילציה על איי CpG מדוכא ומורש. מיקרו רנ"א יכול להיות מבוקר על ידי מתילציה על ה-DNA וכן על ידי שינוי ההיסטונים.
- תהליכים הקשורים במרנ"א – המרנ"א עצמו יכול לעבור מתילציה, ובכך מושפע ביטויו.
- תהליכים התלויים ב-Small RNA – sRNA הן מולקולות רנ"א שאינו מקודד קטנות, מובְנות מאוד המצויות בחיידקים. הן שולטות על ביטוי גנים, וממלאות תפקידים חשובים בתהליכים ביולוגיים רבים על ידי קישור למולקולות המרנ"א בפרוקריוטים.
- פריונים – זוהי הצורה הזיהומית של חלבון. באופן כללי, חלבונים מתקפלים ליחידות נפרדות המבצעות תפקידים תאיים מסוימים. חלבונים מסוימים יכולים להפוך להיות פריונים, על ידי קיפול החלבון לצורה זיהומית מסוימת, ואף לגרום לחלבונים אחרים לעבור למצב של פריון. על אף שהפריונים נחקרים בתחום המחלות הזיהומיות, ניתן לראות תהליך הדבקה על ידי פריון כתהליך אפיגנטי, כי הפריונים מובילים לשינויים פנוטיפיים מבלי לשנות את רצף ה-DNA עצמו. פריונים פטרייתיים נחשבים אפיגנטיים מכיוון שהם עוברים בתורשה.
- תורשה מבנית – בריסניות, כגון סנדלית וטטרהימנה, תאים זהים מבחינה גנטית מראים הבדלים תורשתיים בסידור הריסים על פני התא. חוקרים שינו את דפוס הביטוי והראו שהסדר החדש מועבר לתאי הבת, וטענו כי המבנה הקיים משמש כתבנית ליצירת המבנה לדור הבא. המנגנון של צורת תורשה כזאת אינו ברור דיו, אך קיימות סיבות להניח שגם אורגניזמים רב תאיים משתמשים במבני תאים קיימים כדי להרכיב תאים חדשים.
- מיקום נוקליאוזומים – הגנום של יצורים איקריוטיים מסודר סביבי אינספור נוקליאוזומים. המיקום שלהם ברחבי הגנום אינו אקראי, וקובע את מידת הנגישות של ה-DNA לחלבוני בקרה, המבקרים את רמות ביטוי הגנים וחלוקת התא. הוכח כי לפחות חלק מהנוקליאוזומים נשמרים בתאי הזרע (כאשר רוב ההיסטונים מוחלפים על ידי פרוטמינים) אך לא כל ההיסטונים, ולכן מיקום הנוקליאוזומים הוא תורשתי במידה מסוימת. מחקרים מראים כי ישנו קשר בין מיקום נוקליאוזומים לבין מאפיינים גנטיים נוספים, כגון מתילציה של DNA. עם זאת, לא כל עיצוב כרומטין מורש, ולא כל תורשה אפיגנטית מערבת את עיצוב הכרומטין.
אפיגנטיקה ונטייה מינית[עריכת קוד מקור | עריכה]
מחקר מצביע על כך שהומוסקסואליות מועברת דרך מנגנון אפיגנטי.[1][2]
אפיגנטיקה ורפואה[עריכת קוד מקור | עריכה]
לאפיגנטיקה ישנם יישומים רבים ומגוונים ברפואה. חוקרים אחדים, כמו ד"ר רנדי ג'ירטל מהמרכז הרפואי של אוניברסיטת דיוק, סוברים כי ייתכן והאפיגנטיקה עשויה להיות משמעותית יותר במחלות מסוימות מאשר הגנטיקה. בשנת 2008, ה-NIH הכריזו על הענקת תקציב מחקר של 190 מיליון דולר למחקר אפיגנטיקה במהלך חמש השנים הבאות, מתוך מחשבה שלאפיגנטיקה יש פוטנציאל להסביר מנגנונים של הזדקנות, התפתחות האדם, מקורות מחלת הסרטן, מחלות לב, מחלות נפש ועוד.
תאומים[עריכת קוד מקור | עריכה]
 ערך מורחב – תאומים
ערך מורחב – תאומים
מחקר של תאומים זהים הוא מודל אופטימלי למחקר אפיגנטיקה סביבתית. בעוד תאומים זהים בשנות הילדות זהים מבחינה אפיגנטית, תאומים זהים מבוגרים נבדלים זה מזה בצורה ניכרת ברמות ובמיקום של המתילציות על ה-DNA והאצטילציות על היסטונים. זוגות התאומים עם ההבדלים הניכרים ביותר הם אלו אשר חיו בנפרד זמן רב ויותר, ואלו שההיסטוריה הרפואית שלהם שונה זה מזה.
החתמה גנומית[עריכת קוד מקור | עריכה]
 ערך מורחב – החתמה גנומית
ערך מורחב – החתמה גנומית
החתמה גנומית היא תופעה שבה האב והאם תורמים תבנית אפיגנטית שונה לאזור מסוים ב-DNA של הצאצא. ישנן מחלות שונות הקשורות בתופעה זו, כגון תסמונת אנגלמן ותסמונת פראדר וילי. אלו מחלות גנטיות רגילות אשר נגרמות עקב מחיקה או השתקה של גנים, אך הן נפוצות באופן חריג מכיוון שנוצר מצב מעין המיזיגוטי בגלל החתמה גנומית, ולכן מספיקה פגיעה בעותק אחד של הגן ולא בשני העותקים כפי שנדרש להיווצרות של מחלות רבות. התסמונת הנוצרת – אנגלמן או פראדר וילי – תלויה בעותק ה-DNA (האבהי או האימהי) העובר החתמה גנומית. דוגמה נוספת היא תסמונת Beckwith–Wiedemann, אשר עלולה להיגרם עקב פגם בהחתמה הגנומית האימהית באזור מסוים על כרומוזום 11.
בשוודיה נערך מחקר על צאצאים של גברים שוודים שנחשפו למצב של רעב בשנות ההתבגרות שלהם במאה ה-19 ובו התגלה כי נכדים אבהיים (אך לא אימהיים) היו בסיכון יותר נמוך למות ממחלות לב וכלי דם. לעומת זאת, במצב שבו הסבים לא סבלו מרעב, התמותה מסוכרת אצל הנכדים גדלה, מה שיכול לרמז על תורשה גנטית למשך מספר דורות. תופעה הפוכה נצפתה אצל הנשים – הנכדות האבהיות (אך לא האימהיות) של נשים שחוו רעב בעודן ברחם (כלומר, כאשר ביציותיהן נוצרו) חיו חיים קצרים יותר בממוצע.
סרטן[עריכת קוד מקור | עריכה]
 ערך מורחב – סרטן (מחלה)
ערך מורחב – סרטן (מחלה)
מגוון של מנגנונים אפיגנטיים מעורבים בסוגי סרטן רבים. שינויים אפיגנטיים בגנים המתקנים נזקי DNA ובגנים הקשורים למחזור התא שכיחים מאוד בסרטן המתפתח באופן אקראי לעומת אותו סוג סרטן הנגרם עקב סיבות תורשתיות. שינויים אפיגנטיים חשובים לתהליך ההתמרה הסרטנית, ולכן מחקר בתחום זה מהווה פוטנציאל לזיהוי, טיפול ומניעה של סרטנים אלו. כיום ישנן תרופות בעלות השפעה אפיגנטית ידועה, ותחום המחקר העוסק בכך הוא אפיגנטיקה של סרטן.
אפיגנטיקה בחיידקים[עריכת קוד מקור | עריכה]
אפיגנטיקה קיימת גם בחיידקים, אך בעוד באיקריוטים בכלל וביצורים רב תאיים בפרט האפיגנטיקה משמשת בעיקר כמנגנון בקרה בסיסי לביטוי גנים, שימוש זה אצל חיידקים הוא מצומצם. השימוש הנרחב של חיידקים באפיגנטיקה הוא במתילציה של ה-DNA לאחר שכפולו כדי לשלוט אפיגנטית על האינטראקציות של חלבונים עם ה-DNA. בעוד האיקריוטים ממתלים את הנוקליאוטיד ציטוזין ב-DNA, החיידקים ממתלים את האדנין כאות אפיגנטי. מתילציה של אדנין ב-DNA של חיידקים רבים חיונית לאלימות שלהם, לדוגמה אצל Escherichia coli, סלמונלה, Vibrio, Yersinia, Haemophilus, ו-Brucella. בסוגי חיידקים מסוימים, כגון Alphaproteobacteria, מתילציית האדנין מבקרת את מחזור התא, ומצמדת בין תהליכי ביטוי גנים לתהליך שכפול ה-DNA. באחרים, כגון Gammaproteobacteria, מתילציית האדנין מאותתת לתהליכים רבים, ובהם שכפול DNA, הפרדה של כרומוזומים, תיקון אי התאמה בזיווג בסיסים, אריזה של בקטריופאג'ים, פעילות טרנספוזונית ובקרת ביטוי גנים.
בפסיכולוגיה ובפסיכיאטריה[עריכת קוד מקור | עריכה]
מקובל לטעון כי תורשה של אפימוטציה לדור הבא יכולה לנבוע מגורמים סביבתיים רבים, כמו תזונת ההורים, חשיפת העובר לעקה של האם וגיל ההורים. דברים אלו ואחרים יכולים לגרום לשינוי שאינו ברצף ה-DNA עצמו בצאצא, ואף בדורות הבאים.
התמכרות הוא מצב בו מנגנון התגמול במוח נפגם, ונובעת משינויים ברמת השעתוק ומנגנונים נוירו-אפיגנטיים. תהליכים אלה מתעצמים במהלך חשיפה כרונית לגירוי הממכר (כגון מורפין, קוקאין, יחסי מין, הימורים וכדומה). במחקרים פרה-קליניים הראו כי ישנה תורשה של הפנוטיפים של מכורים לצאצאים.
במחקר פרה-קליני שנערך בעכברים הראו כי ישנה תורשה אפיגנטית של פנוטיפים הקשורים בחרדה. במחקר זה, תורשה של תכונות הנובעות מיצירת מצב עקה אצל האב עבר בתורשה דרך RNA לא מקודד לצאצאים. דבר דומה נמצא גם בפנוטיפים הקשורים לדיכאון. בנוסף, מחקרים בעכברים הראו כי פחדים מותנים מסוימים יכול לעבור בתורשה על ידי אחד ההורים. לדוגמה, נערך ניסוי בו החוקרים הצמידו ריח מסוים לשוק חשמלי, כך שהעכברים למדו לפחד מהריח. נמצא כי הפחד הזה נוכח גם אצל הצאצאים, על אף שהם לא חוו שוק חשמלי כלל. החוקרים טוענים כי מתילציה ספציפית של ה-DNA מוּרשת לפחות במשך שני דורות, כך שהעכברים פוחדים מהריח בלי חשיפה לשוק החשמלי.
ראו גם[עריכת קוד מקור | עריכה]
לקריאה נוספת[עריכת קוד מקור | עריכה]
- The Changing Concept of Epigenetics, EVA JABLONKA AND MARION J. LAMB, Annals of the New York Academy of Sciences 981:82-96 (2002)
- ד"ר שרון מועלם, דווקא החלשים שורדים, הוצאת אריה ניר, 2009.
- פרופ' חוה יבלונקה ומריון ג' למב, אבולוציה בארבעה ממדים, הוצאת עם עובד, 2008.
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- התורשה שמעבר לדנ"א, חלק א', חלק ב', חלק ג' דינה צפרירי, גליליאו, ynet
- רנן נצר, 40 השבועות שביליתם בבטן אמכם - ישפיעו על בריאותכם כל חייכם, באתר גלובס, 17 במאי 2012
- אופיר דור, טראומה זה בגנים, באתר כלכליסט, 11 בדצמבר 2014
- מחקר על אפשרות לתורשה אפיגנטית בעכברים, באתר מכון דוידסון לחינוך מדעי, של מכון ויצמן
- יעל (פרוינד) אברהם, תעביר את זה הלאה, בעיתון מקור ראשון, 29 באפריל 2019
- הורשת פעילות מוחית מדור לדור שלא דרך DNA באתר הידען
- רוח הרפאים בגנים שלכם Horizon. את הסרט בארבעה חלקים אפשר למצוא כאן (באנגלית)
- אפיגנטיקה, באתר אנציקלופדיה בריטניקה (באנגלית)
