הפריה חוץ-גופית
יש לערוך ערך זה. הסיבה היא: שגיאות כתיב, חלוקה לנושאים, פסקאות וסעיפים לקויה, חוסר במקורות.
| ||
| יש לערוך ערך זה. הסיבה היא: שגיאות כתיב, חלוקה לנושאים, פסקאות וסעיפים לקויה, חוסר במקורות. | |

הפריה חוץ-גופית או הח"ג (בלשון הדיבור: הפריית מבחנה, באנגלית: In vitro fertilisation ובקיצור IVF) היא אחד הכלים העיקריים לטיפול בעקרות בקרב נשים וגברים. בהפריה כזו, לבורנט מפרה זרע עם תא ביצית במבחנה, כלומר מחוץ לגוף האישה, ולאחר מכן, הביצית המופרית מועברת לרחם, שם מתפתח ההיריון כרגיל.
היסטוריה[עריכת קוד מקור | עריכה]
טכניקת ההפריה החוץ-גופית פותחה בבריטניה על ידי ד"ר פטריק סְטֶפְּטוֹ וד"ר רוברט אדוארדס. "תינוקת המבחנה" הראשונה בעולם הייתה לואיז בראון, שנולדה ב-25 ביולי 1978 בבית החולים הכללי אולדהם בהליך של ניתוח קיסרי. הוריה ניסו להרות במשך כתשע שנים ללא הצלחה בשל חסימה בחצוצרות של אמה. גם אחותה הקטנה, נטלי, נולדה באמצעות הפריה חוץ-גופית, וב-1999 הייתה לאם הראשונה שנולדה בהליך זה[1]. בתחילה היו שפקפקו באמיתות ההצלחה של סטפטו ואדוארדס[2], אך בהמשך הוכרה ההצלחה על ידי כולם.
ישראל היא המדינה החמישית בעולם שבה בוצעה הפריית מבחנה, ובעקבות הפריה זו נולדה בשנת 1982 העיתונאית והמגישה רומי נוימרק[3]. שנה אחר כך נולד אלעד קליינר, ילד המבחנה (הזכר) הראשון. ביוני 1985 נולדה בבית החולים רמב"ם התינוקת הראשונה שנולדה לאם ערבייה מהפריה חוץ-גופית[4]. בינואר 1986 נולדה בישראל שלישייה לאם שעברה דילול עוברים בצרפת לאחר הפריה חוץ-גופית[5]. מאז יש גידול רב בשימוש בהפריה חוץ-גופית, וקרוב לאחוז אחד מכל הלידות כיום בעולם המערבי הן כתוצאה מהפריה חוץ-גופית.
התוויה[עריכת קוד מקור | עריכה]
מטרתה המקורית של ההפריה החוץ-גופית הייתה לטפל באי-פוריות מכנית או חסימתית כתוצאה מבעיה בחצוצרות, אך שיטת הטיפול התבררה כיעילה גם במקרה של בעיות פוריות אחרות. פיתוח שיטת ICSI (הזרקת זרע ציטופלזמטית) נותנת מענה יעיל ביותר להפרעות בפוריות הגבר, כל עוד ניתן להפיק זרע.
הפריה חוץ-גופית היא פעולה התערבותית ויקרה יחסית, ועל כן השימוש בה נעשה לאחר שנוסו שיטות אחרות לטיפול באי-פוריות שהן פולשניות פחות, תלוי ברמת בעיית הפוריות של הגבר או האישה.
מאז השימוש הראשון בהפריה חוץ-גופית ובשל היעילות הרבה של השיטה, התרחבו מאוד ההתוויות לשימוש בהפריה חוץ-גופית:
- אי-פיריון לא מוסבר
- רזרבה שחלתית נמוכה
- בעיות זרע (בבעיות זרע קלות קו הטיפול הראשוני בדרך כלל יהיה על ידי הזרעה תוך רחמית. בבעיות זרע קשות ייתכן שיפנו ישירות ל-IVF)
ישנם טיפולים שניתן לבצע אך ורק בעזרת טיפולי הפריה חוץ-גופית אף שלא קיימת בעיית פוריות:
- אבחון טרום עוברי, משמש למניעת העברת מחלות גנטיות
- בחירת מין הילוד
- פונדקאות
- תרומת ביצית
- שימור פריון והקפאת ביציות
- אבות נשאי HIV
השיטה[עריכת קוד מקור | עריכה]
בדיקות מקדימות[עריכת קוד מקור | עריכה]
לפני טיפולי הפריה חוץ-גופית מקובל לבצע בדיקות מקדימות רבות, תלוי בהחלטת הרופא המטפל:
- בדיקות כלליות לאישה לפני כניסה להיריון
- בדיקות גנטיות לשלילת מחלות תורשתיות הניתנות למניעה באבחון טרום-עוברי
- בדיקות לאיתור מחלות מין
- בדיקת זרע
- הדגמה של חלל הרחם באחת מהשיטות הקיימות (US תלת־ממד, היסטרוסקופיה או צילום רחם)
- הערכה של הרזרבה השחלתית על ידי אחת מהבדיקות האלה: FSH, AFC, בדיקת זקיקים קטנים או AMH.
עקרונות ושלבי הטיפול[עריכת קוד מקור | עריכה]
טיפול הפריה חוץ-גופית מבוסס על כמה עקרונות ושלבים:
- מתן גירוי שחלתי להגדלת כמות הביציות
- דיכוי ביוץ ספונטני
- גרימת ביוץ יזום ומתוזמן
- שאיבת ביציות
- הפריה במעבדה
- גידול העוברים
- החזרת עוברים או הקפאה
- מתן תמיכות הורמונליות
גירוי השחלות[עריכת קוד מקור | עריכה]
מחזור הטיפול מתחיל על פי רוב ביום השני לווסת, וכולל מתן תרופות המגרות את השחלות לייצר מספר רב של זקיקים. ברוב המקרים מוזרקים גונדוטרופינים מסוג FSH או נגזרותיו. במהלך מתן ההורמונים יש צורך במעקב אחרי רמת האסטרדיול ובדיקות אולטרסאונד למעקב אחרי גדילת הזקיקים. לרוב יש צורך בכעשרה ימי טיפול. בזמן זה ניתנות תרופות לעיכוב הביוץ.
באופן כללי, רוב הפרוטוקולים בטיפולי פריון מתבססים על עיקרון של סופר-אובולציה (super ovulation) כדי לגרות ייצור של כמה ביציות ולשפר את תזמון שאיבתן. הטכניקות הקיימות כיום כוללות את התרופות האלה:
- מתן FSH – סינתטי או אורינרי/הומני (מיוצר משתן אנושי).
- LH – סינתטי או אורינרי/הומני.
- ניתן להתחיל את הטיפול עם איקקלומין או לטרזול אך תרופות אלה מקובלות פחות בישראל.
תרופות אלה נלקחות על בסיס יומי ומגדילות את מספר הזקיקים בשחלה. לאחר מתן תרופות אלה יש לעקוב באופן קפדני על ידי אולטרסאונד כדי לוודא שאין מספר רב מדי של ביציות ולוודא שהן גדלות לגודל אופטימלי לצורך שאיבתן.
- רמות האסטרדיול נבדקות גם הן לצורך הערכת הגדילה. מצופה שכל זקיק יגרום להפרשה של 200 פיקוגרם למ"ל של אסטרדיול. קיימת הוכחה לכך שאופן ההתנהגות של רמות האסטרדיול בדם מנבאות את הצלחת הטיפול – ירידה ברמות האסטרדיול טרם מתן HCG המביא לביוץ עצמו מקושרת לשיעורי היריון נמוכים יותר.
- כאשר שני זקיקים מובילים מגיעים לגודל של 18–19 מ"מ באולטראסאונד, יש להשרות ביוץ על ידי HCG, הפועל בדומה להורמון LH ומביא לביוץ בתוך 38–40 שעות. יש לשאוב את הביציות לפני טווח זמן זה. אם הזקיקים יישאבו מאוחר מדי, הם לא יכללו ביציות שכבר בייצו.
- הטיפול במדכאי ביוץ GNRH אגוניסטים או אנטגוניסטים בנוסף לטיפולים המתוארים לעיל הביא לירידה דרסטית בסיכוי של עלייה מוקדמת מדי ב-LH, ובמילים אחרות הביא לירידה דרסטית ביכולת של ביצית לפרוץ החוצה טרם שאיבתה. כתוצאה מכך, משמשים היום תכשירים אלו ברוב המוחלט של טיפולי ההפריה החוץ-גופית.
פרוטוקולים[עריכת קוד מקור | עריכה]
ישנם פרוטוקולים רבים לגירוי שחלתי, אך שני הפרוטוקולים השכיחים הם:
- פרוטוקול ה-GNRH agonist. ניתנים לרוב ביום ה-21 של המחזור הקודם (פרוטוקול ארוך) או בתחילת הווסת של המחזור הנוכחי יחד עם מתן של גונדוטרופינים. הם ניתנים עד ליום שבו ניתן HCG.
- מחזור GNRH antagonist (קצר), מתחיל במתן גונדוטרופינים ביום השני למחזור, ומתן GNRH antagonist חמישה-שישה ימים לאחר מתן הגונדוטרופינים, או כאשר הזקיק המוביל הוא בגודל של 13 מ"מ.
הבדלים בין המחזורים:
- ב-GNRH antagonist (קצר) יש פחות זריקות ומינונים נמוכים יותר של גונדוטרופינים (SOFT PROTOCOL).
- ב-GNRH antagonist (קצר) יש פחות גירוי יתר שחלתי ואפשרות לגרום לביוץ בעזרת GNRH agonist ובכך לבטל לחלוטין את האפשרות של גירוי יתר שחלתי באותו מחזור.
- ב-GNRH agonist שיעור ההריונות גבוה יותר.
שאיבת הביציות[עריכת קוד מקור | עריכה]
שאיבת הביציות נעשית בערך 34–36 שעות לאחר מתן הזרקת HCG, ונעשית כיום בגישה טרנס-וגינלית ובסיוע אולטראסאונד. טכניקת השאיבה מבוססת על מחט מונחית-אולטראסאונד החודרת דרך דופן הנרתיק ומגיעה לשחלות. מחט זו שואבת את הנוזל מתוך הזקיקים והוא מועבר למעבדה כדי לזהות את הביציות. תהליך השאיבה נמשך כ-20 דקות והוא מתבצע לרוב תחת טשטוש או בהרדמה כללית.
טכניקת ICSI[עריכת קוד מקור | עריכה]
 ערך מורחב – הזרקת זרע ציטופלזמטית
ערך מורחב – הזרקת זרע ציטופלזמטית
באופן כללי, זרע טרי לאחר השפיכה אינו יכול להפרות ביצית בתנאי מעבדה, ועליו לעבור קפסיטציה – זהו תהליך פשוט הכולל אינקובציה קצרה בתוך תרבית. לאור תהליך שאיבת הביציות, ניתן לצפות כי הביציות עצמן יהיו בשלבי גדילה שונים. לאחר שאיבתן מתבצעת חלוקה שלהן לביציות בשלות וביציות לא בשלות. ביציות בשלות מכילות שכבה עבה ורחבה של קומולוס אופורוס, הן השלימו את החלוקה המיוטית הראשונה שלהן וניתן לראות בתוכן את הגופיף הפולארי הראשון. הן מופרות על ידי זרע לרוב תוך חמש שעות ממועד שאיבתן. אם זרע וביצית מעורבבים מוקדם מדי, לא תתרחש הפריה. בין 50,000 ל-150,000 זרעונים מושמים ליד כל ביצית. ביציות שאינן בשלות מכילות שכבה קומפקטית בלבד של אופורוס קומולוס, ועדיין לא ניתן לראות בהן גופיף פולארי. הן מושמות באינקובציה עד ל-36 שעות טרם הפרייתן.
האינדיקציה העיקרית להפריה בשיטת ה-ICSI היא אי-פריון גברי – פחות מחמישה מ"ל זרע נורמלי ומוטילי למ"ל, עבור זרע שהוצא מהאשך באופן כירורגי כגון מצבים של אזוספרמיה. עם זמן הלכו והתרחבו האינדקציות לשימוש ב-ICSI. האינדקציות המקובלות היום:
- הפריית ביציות שהופשרו
- בטיפולי PGD – אבחון טרום-השרשתי
- אי-פריון לא מוסבר – מקובל לבצע למחצית מהביציות הפריה ב-ICSI
- מיעוט ביציות (בחלק מהמכונים)
- נשאי HIV
בתהליך זה נבחר זרעון אחד לכל ביצית בשלה. ישנו ניסיון לבחור את הזרעון התקין ביותר מבחינה מורפולוגית מתוך ההנחה שהתקינות המורפולוגית מצביעה גם על תקינות הזרעון וסיכויי ההפריה. הוא מוזרק ישירות לתוך הציטופלזמה ורחוק מהגופיף הפולארי.
לאחר תהליך ההפריה העוברים נמצאים באינקובציה באטמוספירה המכילה פחות מחמישה אחוזים של carbon dioxide. העוברים נבחנים בפרמטרים שונים, לרבות האם נוצר בהם pronuclei המוודא שאכן הייתה הפריה.
החזרת עוברים[עריכת קוד מקור | עריכה]
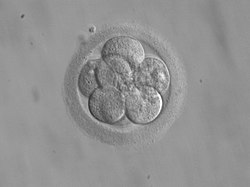
שלושה-חמישה ימים לאחר גדילה בתנאי מעבדה העוברים מוחזרים לרחם בתהליך הנקרא החזרת עוברים. קודם להחזרה העוברים מדורגים מ-A ל-D לפי הופעתם ורמת הפרגמנטציה בהם. אם ההעברה מתרחשת ביום החמישי או השישי, העוברים מוחזרים בשלב הבלסטוציסט. ההחלטה אם להחזיר ביום השלישי או ביום החמישי תלויה במידת ההצלחה של המעבדה ושל הרופא. בהחלטה כמה עוברים להחזיר מעורבים שני שיקולים: מצד אחד, רוצים להגדיל את הסיכוי שלפחות עובר אחד ייקלט ברחם, ומצד שני, רוצים להימנע מהיריון של מספר גדול מדי של עוברים, על הסיכונים הנובעים מכך. מכיוון שסיכויי קליטת העוברים קטנים ככל שגיל האם גבוה יותר, ההמלצות הנוכחיות הן להחזיר מספר גדול יותר של עוברים ככל שגיל האם גבוה יותר.
המלצות הוועדה האמריקנית לפריון (ASRM) הן:
- אישה מתחת לגיל 35 – החזרת שני עוברים (יש לשקול החזרת עובר אחד בלבד, אם זהו מחזור הטיפול הראשון ב-IVF, אם היה מחזור טיפול מוצלח קודם ב-IVF, או כאשר העובר במצב מצוין).
- אישה בת 35–37 – החזרת בין שניים לשלושה עוברים.
- אישה בת 38–40 – החזרת שלושה-ארבעה עוברים.
- מעל גיל 40 – החזרת חמישה עוברים.
במצבים מסוימים, כמו טיפולי IVF קודמים שלא הצליחו או פרוגנוזה לא טובה, יש הממליצים על החזרת עוברים רבים יותר (מסלול שאינו תלוי גיל). שיקול נוסף בהחלטה לגבי מספר העוברים המוחזרים נוגע לסיכויי ההצלחה של דילול עוברים והסכמת האם לדילול עוברים אם מספר גבוה של עוברים ייקלט.
רוב ההחזרות מתבצעות תחת הנחיית אולטראסאונד. על המטופלת לשתות מים על מנת למלא את שלפוחית השתן, כדי "לחזק" את הרחם ולהגביר את יכולת הצפייה באולטראסאונד. העוברים הטובים ביותר נשאבים לתוך קתטר, ולאחר שהרופא מכין את צוואר הרחם ושואב ריר צווארי, העוברים מוחדרים לתוך חלל הרחם. הסיכוי להיריון מושפע מגיל האם, מסיבת האי-פריון, מעובי האנדומטריום ומהדירוג הממוצע של העוברים שהוכנסו. אצל חלק מהמטופלות, בעיקר מטופלות מעל גיל 38, יש פתיחה של ה-zona pellucida (תהליך של assisted hatching) בביצית, כדי לשפר את ההשרשה. זה לא נעשה באופן רוטיני.
מתן תמיכה לוטאלית[עריכת קוד מקור | עריכה]
לאחר שמתבצעת החזרת העוברים ניתן פרוגסטרון למשך כשבעה שבועות לצורך תמיכה לוטאלית. הפרוגסטרון יכול להינתן בהזרקה, בג'ל ואמצעים נוספים.
סיבוכים וחסרונות הקשורים להפריה חוץ-גופית[עריכת קוד מקור | עריכה]
- היריון מרובה עוברים – כיום נעשה ניסיון להקטין את מספר העוברים המוכנסים לרחם כפי שצוין לעיל. העברת עוברים רבים יותר לרחם לא בהכרח מגדילה את שיעורי ההצלחה. אם נשארו עוברים שלא הועברו לרחם, ניתן להקפיא אותם לצורך שימוש בשלב מאוחר יותר. נהוג לציין כי הסיכוי של השרשה מוצלחת של עובר מוקפא הוא מחצית מהסיכוי עבור עובר טרי, אולם ישנן מספר מעבדות המתארות שיעורי היריון דומים בשני המקרים.
- היריון חוץ-רחמי והיריון הטרוטופי – הפריית מבחנה מגדילה פי שניים את הסיכויים להיווצרות היריון חוץ-רחמי. היריון הטרוטופי הוא היריון המכיל עובר אחד בתוך הרחם ועובר אחד שהשתרש מחוץ לרחם. מקרים אלה נדירים בהיריון רגיל, אך בהפריית מבחנה שיעורם מגיע לכאחוז אחד.
- לידה מוקדמת ותינוקות שנולדים במשקל נמוך יותר מהממוצע – הפריית מבחנה מגדילה את הסיכויים לכך.
- תסמונת גירוי יתר שחלתי – תסמונת זו מאופיינת על ידי הגדלה בשחלות, מיימת, והמו-קונסנטרציה. הפרוגנוזה לרוב גרועה יותר אצל נשים שהרו תוך כדי היווצרות התסמונת. מטופלות אלו הן בסיכון מוגבר להיווצרות קרישי דם.
- מומים מולדים – בחלק מן המקרים דווח על סיכון מוגבר יותר למומים מולדים אצל תינוקות שנולדו בהפריית מבחנה, אך מידע זה שנוי במחלוקת. אם בוצעה טכניקת ICSI, הסיכון למומים גנטיים הקשורים להחתמה גנטית עלול לעלות (לדוגמה, תסמונת אנגלמן או תסמונת בקווית'-ויידמן (אנ')).
טכניקות נוספות הקשורות להפריית מבחנה[עריכת קוד מקור | עריכה]
- תרומת ביציות – תרומת ביציות יכולה להיעשות בכמה מצבים. מצב אחד הוא שאישה עם בעיות פריון בוחרת לתרום חלק מהביציות במסגרת תהליך הפריית המבחנה לאישה אחרת שאינה מסוגלת לייצר ביציות. מצב אחר הוא שאישה עוברת תהליך של סופר-אובולציה למטרת תרומת ביציות בלבד. בשני המקרים, טרם העברת הביציות או העוברים עצמם, יש לדאוג למתן אסטרוגן ופרוגסטרון לרחם האישה הקולטת, ויש להמשיך במתן אסטרוגן ופרוגסטרון למשך עשרה שבועות לפחות. מספר העוברים המוחזרים הוא בהתאם לגיל התורמת ולא לגיל המקבלת.
- העברת גמטה לחצוצרה (באנגלית: GIFT) (אנ') – שיטה דומה ל-IVF, שבעבר שימשה רבות בטיפולי הפריה, אולם לאור עלייה בהצלחת הטיפול ב-IVF היא כמעט שאינה מבוצעת כיום. אינדיקציות לביצוע GIFT כוללות כיום בעיקר מטופלים המעוניינים שההפריה תתבצע בגוף האישה ולא בתנאי מעבדה, למשל מסיבות דתיות. במנגנון זה מתבצעת סופר-אובולציה כמו ב-IVF רגיל ונשאבות ביציות. לאחר מכן, הזרע נאסף ועובר קפסיטציה, ואז מתבצעת לפרוסקופיה, ובמהלכה הזרעונים והביציות מעורבבים ומוכנסים לתוך קתטר. הקתטר מכניס אותם באופן לפרוסקופי לחצוצרה, ושם מתרחשת ההפריה עצמה. בשיטה זו דווחו כ-20–30 אחוזים שיעורי הצלחה פר מחזור. השיטה מבוצעת בנשים שאין להן בעיה בחצוצרה וגילן אינו מבוגר, אך מכיוון שהשיטה מצריכה ביצוע הרדמה כללית ולפרוסקופיה, כמעט שאין מבצעים אותה כיום.
- ZIFT או zygote intrafallopian transfer – טכניקה המשלבת בין GIFT לבין IVF. לאחר שהביציות נשאבות הן עוברות הפריה בתנאי מעבדה, ומייד לאחר מכן הן מוחזרות לחצוצרה כשהן בשלב הזיגוטה בטכניקה הדומה ל-GIFT (לפרוסקופיה). כיום כמעט שלא משתמשים בטכניקה זו.
- אבחון טרום-השרשה (PGD) – החל משנת 1990. בטכניקה זו ניתן לאבחן מגוון רב של מחלות לפני החזרת העובר לרחם, בטכניקות של FISH ושל PCR. כיום ניתן להוציא תא אחד או שניים (בלסטומר) מעובר המכיל 8 תאים בלבד, ללא פגיעה בעובר. ניתן גם לערוך ביופסיה לגופיף הפולארי הראשון או השני באותו האופן, כדי לבחון פגמים בגנים. בדיקה זו מבוצעת להורים שהם נשאים או חולים במחלות גנטיות מסוימות, המעוניינים לוודא שהעובר אינו חולה במחלה, או במקרים שבהם קיימות הפלות חוזרות, מספר מחזורי טיפול ב-IVF שלא הצליחו וסיבות נוספות.
לאחר ההעברה[עריכת קוד מקור | עריכה]

בעבר היה מקובל להמליץ על מנוחה לאחר החזרת עוברים, אך כיום לאחר מחקרים בתחום מקובל כי אין צורך כלל במנוחה במיטה לאחר החזרת עוברים. כעבור שבועיים על האישה לבצע בדיקת היריון, ועד אז עליה לקחת תמיכות הורמונליות בפרוגסטרון ולעיתים גם באסטרוגן. אך במקרה שמתבצעת החזרה של עוברים מוקפאים, תוך שימוש במחזור הטבעי של האישה, לעיתים אין צורך בתמיכות הורמונליות.
היריון[עריכת קוד מקור | עריכה]
שיעור ההצלחה הוא בין 20 ל-30 אחוז עבור כל מחזור הפריה. הגורמים המשפיעים על שיעור ההצלחה כוללים את גיל האישה, איכות הביציות ותאי הזרע, משך האי-פוריות, בריאות הרחם ומומחיות הרופאים. בתוכניות הפריה רבות מקובל מאוד להעביר לרחם מספר גדול של עוברים כדי להגדיל את סיכויי הקליטה. נוהל זה מגדיל את הסיכוי להיריון מרובה-עוברים, שעלול לגרום בעצמו לסיבוכים. בכמה מדינות חל איסור על העברת יותר משני עוברים לרחם.
קְרִיוֹפְּרֶזֶרְוָוצְיָה (הקפאה)[עריכת קוד מקור | עריכה]
הקפאה היא תהליך שבו עוברים או ביציות מוקפאים לצורך שימוש בעתיד. הקפאת עוברים נמצאה יעילה מאוד והשתפרה משמעותית עם השנים, כאשר שיעורי ההישמרות של עוברים מוקפאים דווחו בין 50% ל-90%. לפני החזרת העוברים יש לבצע סינכרוניזציה של מחזור המטופלת כך שהעוברים יוחזרו במהלך ההשרשה ברחם, ועל כן מומלץ מתן אסטרוגן ופרוגסטרון. הקפאת ביציות החלה לצבור תאוצה בעשור האחרון, אולם טרם צברה נתונים מספריים, שלא כמו הקפאת עוברים.
הקפאת עוברים[עריכת קוד מקור | עריכה]
 ערך מורחב – הקפאת עוברים
ערך מורחב – הקפאת עוברים
אם נוצר מספר רב של עוברים, המטופלים יכולים לבחור להקפיא עוברים שלא הועברו לרחם. עוברים אלו נשמרים בחנקן נוזלי ויכולים להישמר כך זמן רב. היתרון בכך הוא שאפשר להיכנס שוב להיריון מבלי לעבור מחדש את כל מחזור שאיבת הביציות.
הקפאת ביציות[עריכת קוד מקור | עריכה]
 ערך מורחב – הקפאת ביציות
ערך מורחב – הקפאת ביציות
עד לפני כמה שנים הקפאת ביציות כמעט לא הייתה אפשרית בשל קושי טכני להקפיא ביציות בשיטת ההקפאה האיטית. עם כניסתה של שיטת הווטריפיקציה (זיגוג) התאפשר להקפיא ביציות עם סיכויי הישרדות של עד 90 אחוזים. שימור פריון היה מיועד בתחילה לנשים לפני טיפולים אונקולוגיים כימותרפיים או כריתת שחלות. כיום ניתן לשמור ביציות גם לצורך "שימור פריון סוציאלי". נשים מעל גיל 30 שטרם מצאו בן זוג או מעוניינות בדחיית הילודה יכולות לשמור ביציות ובכך לשמור על פוטנציאל הפוריות שלהן לשנים.
הקפאת רקמת שחלה[עריכת קוד מקור | עריכה]
 ערך מורחב – שימור שחלות
ערך מורחב – שימור שחלות
הקפאת רקמת שחלה נועדה לנשים המעוניינות להאריך את תקופת הפוריות שלהן מעבר לגבולה הטבעי, או נשים לפני טיפול בסרטן, העלול לפגוע בשחלות שלהן.
בעיות אתיות[עריכת קוד מקור | עריכה]
נושאים שנויים במחלוקת[עריכת קוד מקור | עריכה]
מאז הופעת ההפריה החוץ-גופית היא עוררה מחלוקת גם בציבור וגם באקדמיה, במיוחד בתחילת דרכה. כמה מן הנושאים האתיים מעוררי המחלוקת:
- עקיפת הדרך הטבעית להפריה.
- יצירת חיים במעבדה.
- יצירת יותר עוברים מכפי הצורך.
- השמדת עוברים לא נחוצים.
- שימוש בטכנולוגיה לא-בדוקה.
- הליך יקר שרבים אינם יכולים להרשות לעצמם.
- בזבוז משאבים רפואיים על טיפולים שאינם חיוניים להצלת חיים.
- הקפאת עוברים ב"לימבו".
- השמדת עוברים כחלק מתהליך המחקר.
- אפשרות לברור מבין העוברים על פי תכונותיהם הגנטיות, או (בעתיד) להכניס בהם שינויים גנטיים. ראו גם: בחירת מין היילוד.
- התייחסות לעוברים ולהיריון כאל מוצר צריכה.
- הפריה והולדה לאחר מות האב[6].
פגיעה בתפקידי ההורים המסורתיים[עריכת קוד מקור | עריכה]
הפריה חוץ-גופית מטשטשת את מושג ההורות הביולוגית – אישה יכולה ללדת תינוק מביציות של אישה אחרת ומזרע של גבר שאינו בעלה. עובדה זו מעלה שאלות אתיות ומשפטיות חדשות. השימוש בהפריה חוץ-גופית מקל על רווקים, רווקות וזוגות חד-מיניים להקים משפחה, נושא שמעורר התנגדות או אי-נוחות בקרב רבים (ראו גם: הורות להט"בית).
כמה מקרים זכו לפרסום נרחב:
- ב-2001 התפרסם מקרה של אישה צרפתייה שהעמידה פנים שהיא נשואה לאחיה, וכך ילדה תינוק מזרעו ומביצית שנתרמה. היו שראו בכך מעין גילוי עריות; אחרים טענו שיכול להיגרם נזק נפשי לילד כשיגדל וישמע על הדרך שבה נוצר. אחרים לא ראו בכך כל בעיה.
- בכמה מקרים של טעויות מעבדה הרו נשים וילדו תינוקות שנוצרו מגמטות של אחרים, מה שגרם לבעיות משפטיות סבוכות.
היריון בגיל הפסקת הווסת[עריכת קוד מקור | עריכה]
בעוד גיל הפסקת הווסת מהווה גבול טבעי שאחריו אי-אפשר להיכנס להיריון, הפריה חוץ-גופית מאפשרת לנשים להרות גם בשנות החמישים והשישים לחייהן. טיפול הורמונלי מכין את הרחם שלהן לקליטת היריון, ועוברים נוצרים מביציות של תורמות. האישה המבוגרת ביותר שילדה היא אדריאנה אלייסקו מרומניה, שילדה בגיל 66.
שיקולי דת[עריכת קוד מקור | עריכה]
ביהדות, נושא ההפריה החוץ-גופית מעלה סוגיות הלכתיות סבוכות, ויש מחלוקת בין פוסקי הלכה בשאלה אם מותר להשתמש בהליך זה, ובאילו מגבלות. בין השאר עולה בעיה של הוצאת זרע לבטלה, וכן שאלות בנושא זהות ההורים המדויקת (במיוחד כאשר היולדת אינה האם הביולוגית), ממזרות, והאם התהליך הוא בגדר פרייה ורבייה. באופן כללי ניתן לומר כי מרבית הפוסקים נוטים להתיר הפריה חוץ-גופית, במיוחד כאשר מדובר בזוג נשוי שאינו נזקק לזרע, לביצית או לפונדקאות של צד שלישי.
הכנסייה הקתולית מתנגדת להפריה חוץ-גופית באופן גורף, ורואה בעקרות קריאה מצד האל לאמץ ילדים. מלבד זאת, הכנסייה הקתולית רואה בעוברים בני-אדם לכל דבר, ומתנגדת להשמדתם.
מגבלות חוקיות[עריכת קוד מקור | עריכה]
מדינות רבות הטילו מגבלות חוקיות על הפריה חוץ-גופית בתחומים שונים, בהם מספר הביציות המופרות, מספר העוברים המועברים לרחם, האפשרות להשתמש בתרומת ביציות או תאי זרע, והאפשרות להקפיא ביציות ועוברים. בישראל היה נהוג לאשר רק לנשים נשואות לקבל תרומת ביצית[7], אולם ביוני 2011 פסק בית המשפט המחוזי בירושלים כי בית חולים חייב לאפשר הליכי הפריה חוץ-גופית באישה שאיננה נשואה, מזרע של גבר שנשוי לאישה אחרת, מבלי ליידע את אשתו של הגבר הנשוי או לבקש את התייחסותה[8]. עוברים שנוצרו מזרע ומביצית של זוג שהתגרש אפשר להשתיל רק בהסכמת הבעל[9]. אין להקפיא ביציות למשך יותר מעשר שנים[10].
ישראל תומכת בילודה באמצעות הפריית מבחנה שכן גם בני זוג שאינם נשואים רשאים לקבל טיפול בהפריית מבחנה, ובתנאי שיחתמו על הסכם מיוחד שתוכנו מוכתב על ידי משרד הבריאות, וכולל בעיקר הסכמות מראש מה ייעשה בחומר הגנטי המשותף במקרה שאחד הצדדים משנה את דעתו ואינו מעוניין עוד להמשיך בתהליך, או נפטר.
ראו גם[עריכת קוד מקור | עריכה]
לקריאה נוספת[עריכת קוד מקור | עריכה]
- שרית מגן, ילד משלָךְ - מאחורי הפרגוד של טיפולי ההפריה בישראל, כנרת זמורה ביתן, 2017.
- יהל שלום ויעל השילוני-דולב, עמדותיהן של מטופלות בדבר המעמד המוסרי והשימוש הראוי בעוברים מוקפאים, משפט רפואי וביו אתיקה, כרך 3 עמוד 175, 2010
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- אברהם שטינברג, הערך "הפריה חוץ-גופית", מתוך אנציקלופדיה הלכתית רפואית, באתר מכון שלזינגר
- דנ"א 2401/95 רותי נחמני נגד דניאל נחמני ואח'. פ"ד נ(4) 661. פסק דין תקדימי של בית המשפט העליון בישראל הדן בזכויות הנוגדות של בני זוג שנפרדו להולדת ילדים מביציות שהופרו בהפריה חוץ-גופית.
- הפריה חוץ-גופית, מאמר באתר "דעת", 1995
- ד"ר אלי גבע, בעקבות החוק החדש: איך מקפיאים ביציות ומה העלות, באתר ynet, 20 בינואר 2011
- שבח פרידלר, כיצד אפשר להגביר סיכויים לקליטת עוברים, 27 בדצמבר 2013
 פרופ' פואד עאזם על טיפולי פוריות, סרטון באתר יוטיוב, 17 בדצמבר 2016
פרופ' פואד עאזם על טיפולי פוריות, סרטון באתר יוטיוב, 17 בדצמבר 2016 רותי לוי, אשליית הפריון: מה לא מספרים לנשים על טיפולי ההפריה - ומי משלם את החשבון?, באתר TheMarker, 18 בספטמבר 2017
רותי לוי, אשליית הפריון: מה לא מספרים לנשים על טיפולי ההפריה - ומי משלם את החשבון?, באתר TheMarker, 18 בספטמבר 2017- אדיר ינקו, המחדל הבא בפתח: מעצמת הפריות המבחנה נותרה עם נהלים מלפני עשור, באתר ynet, 20 במרץ 2024
 הפריה חוץ גופית של האדם, דף שער בספרייה הלאומית
הפריה חוץ גופית של האדם, דף שער בספרייה הלאומית- הפריה חוץ-גופית, באתר אנציקלופדיה בריטניקה (באנגלית)
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ אתי הרמתי, ילדת המבחנה הראשונה בעולם, במדור "היום לפני במדע" באתר של מכון דוידסון לחינוך מדעי, 25 ביולי 2016
- ^ אם תינוקת המבחנה הרתה בשיטה המקובלת - טוען ארגון בארה"ב, מעריב, 6 בנובמבר 1978
- ^ מיטל יסעור וליאת רותם, רומי נוימרק, ילדת המבחנה הראשונה: "יום מרגש", באתר ynet, 4 באוקטובר 2010
- ^ דוד זוהר, מוסלמית מהגליל ילדה תינוקת מבחנה, מעריב, 14 ביוני 1985
- ^ איה אדר ממעגן מיכאל ילדה בן ושתי בנות מהפריית מבחנה, מעריב, 8 בינואר 1986
- ^ יוסף שנקר, ההיבטים המוסריים בהפריה אחרי מות בן הזוג, באתר "דעת"
יוסי גרין, הולדה לאחר מיתה באמצעות הפריה חוץ-גופית והשלכותיה על דיני יבום וחליצה, מאזני משפט ב, 2002-2001
יוסי גרין, "ואתם פרו ורבו" (בראשית א', כ"ח), גם לאחר מיתה? הרהורים על ההולדה לאחר מיתה בדין העברי, מאזני משפט ג, 2004-2003
אחיה ראב"ד, תקדים: נפטר מסרטן, אשה שלא הכיר תלד מזרעו, באתר ynet, 6 בדצמבר 2009 - ^ תקנות בריאות העם (הפריה חוץ גופית), התשמ``ז-1987, תקנה 8(ב)(1) ותקנה 11.
- ^ גלעד גרוסמן, בית המשפט המחוזי בירושלים קבע כי יש לאפשר לאישה לעבור טיפולי הפריה בזרעו של גבר נשוי מבלי ליידע את אשתו של הגבר, וואלה, 14 ביוני 2011
- ^ שם, תקנה 8(ב)(3).
- ^ שם, תקנה 9
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.
