מוליך עצבי
 | |
| שחרור של מוליך עצבי בסינפסה | |
| שיוך |
chemical messenger |
|---|---|
מוליך עצבי או מַסְרָן עֲצַבִּי (neurotransmitter - נֵירוֹטְרַנְסְמִיטוֹר) הוא מולקולה המשתחררת מתא עצב (נוירון) אל רווח צר שלפני תא המטרה. הרווח הצר בין שני התאים מכונה בשם סינפסה. תא המטרה יכול להיות תא עצב אחר, תא שריר או תא בלוטה המפריש חומרים.
תפקיד[עריכת קוד מקור | עריכה]
המוליכים העצביים הם האחראים העיקריים על הקשר שבין תאי העצב במערכות עצביות של בעלי חיים באמצעות התהליך של העברה סינפטית. אין תפקוד מוחי ללא מוליכים עצביים המקיימים את פעילות הרשת העצבית במוח, העוסקת בקליטה החושית, בתכנון תנועה, וכן במערכות מפתח מוחיות העומדות בבסיס הקוגניציה, הרגש והמוטיבציה[1]. לפי השפעתם על תא המטרה, ניתן לחלק את המוליכים העצביים לבעלי השפעה מעוררת, מעכבת או מווסתת (מודולטורית) בהתאם לקולטנים על תא המטרה. המספר הכולל של המוליכים העצביים במוח של היונקים אינו ידוע, והוא מוערך במספר עשרות. לכל מוליך עצבי מוכרים מספר סוגים של קולטנים.
מנגנונים של ייצור ופינוי[עריכת קוד מקור | עריכה]
הייצור של סוגי מוליכים עצביים[עריכת קוד מקור | עריכה]
מוליכים עצביים מיוצרים בדרך כלל בתוך תאי העצב ממולקולות אחרות הנמצאות בשפע בתוך התא. בין סוגי המוליכים העצביים נכללים חומצות אמינו, מונואמינים ופפטידים. מונואמינים מיוצרים על ידי שינוי בחומצה אמינית אחת. לדוגמה, המוליך העצבי סרוטונין מיוצר מחומצת האמינו טריפטופן. פפטידים כמוליכים עצביים הם תרכובות של מספר חומצות אמינו, הם מופרשים לעיתים קרובות עם מוליך עצבי אחר מאותו טרמינל, ויש להם השפעה מווסתת. מוליכים עצביים אחרים, הפורינים כמו ATP, נגזרים מחומצות הגרעין. מוליכים עצביים אחרים הם מולקולות גזים קטנות ותוצרים מטבוליים כמו חנקן חד-חמצני (NO)[2]
| קבוצה | דוגמאות |
|---|---|
| חומצות אמינו | GABA, Glutamate, Glycin |
| אמינים | Acetylcholine, Dopamine, Histamine, Epinephrine, Serotonin |
| פפטידים | Somatostatin, Neuropeptide Y, Cholecystokinin, Enkephaline |
| גזים | NO, CO |
איחסון[עריכת קוד מקור | עריכה]
רוב המוליכים העצביים נאספים ומרוכזים בתוך שלפוחיות סינפטיות בסמוך לקרום התא בטרמינלים של האקסונים בתא העצב הקדם סינפטי. מספר מצומצם של מוליכים עצביים כמו הגזים מיוצרים ומשוחררים מייד עם פוטנציאל הפעולה למרווח הסינפטי.[2]
שחרור[עריכת קוד מקור | עריכה]
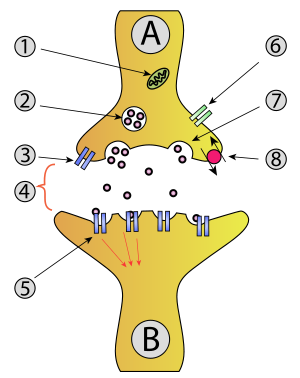
B - תא עצב קולט (בתר-סינפטי)
1. מיטוכונדריון
2. שלפוחית סינפטית המכילה מוליכים עצביים
3. קולטן עצמי
4. מרווח סינפטי דרכו מפעפע מוליך עצבי
5. קולטנים בתר-סינפטיים המופעלים על ידי המוליך העצבי
6. תעלת סידן
7. מוליכים עצביים נפלטים למרווח הסינפטי באקסוציטוזה
8. משאבה לספיגה חוזרת של מוליך עצבי
דחף עצבי המועבר דרך האקסון של תא העצב הפרֶה-סינפטי גורם לשחרור של המוליך העצבי אל המרווח הסינפטי[3]. שלפוחיות האיכסון נעות אל קרום התא, וחלקן מתחברות את הקרום ונפתחות אל המרווח הסינפטי ותוכנן מתרוקן אליו. זהו הליך אקראי. בחלק מהסינפסות של המערכת העצבים המרכזית יש סיכוי לשחרור של שלפוחית בודדת עם כל פוטנציאל פעולה המגיע לטרמינל. לעומת זאת, בסינפסות שבין העצבים המוטוריים ובין השריר משתחררות כ מאה עד 200 שלפוחיות בכל פעילות של העצב. בשני המקרים זהו הליך המפוקח ומווסת על ידי גורמים רבים, והראשי שבהם הוא ריכוז הסידן בטרמינל (ראה העברה סינפטית להרחבה). באופן זה האות החשמלי מתורגם לאות כימי[3]. בסוגי סינפסות רבות קיימת רמה נמוכה "בסיסית" של שחרור מוליכים עצביים ללא דחף עצבי, הנקראת "שחרור ספונטני" וניתנת לרישום ומדידה באמצעות טכניקות אלקטרופיזיולוגיות. המוליכים משוחררים למרווח הסינפטי ועוברים את המרחק הקצר הזה בדיפוסיה. מצידו השני של המרווח הם נקשרים לקולטנים ספציפיים על הקרום של תא המטרה.
ההשפעה על תא המטרה[עריכת קוד מקור | עריכה]
ההשפעה של המוליך העצבי על תא המטרה תלויה בסוג הקולטן שהוא מפעיל בסינפסה המסוימת, ויכולה להיות מעוררת (אקסיטטורית), מעכבת (אינהיביטורית) או מווסתת (מודולטורית).
- השפעה מעוררת נגרמת כאשר הקולטן הוא עצמו תעלה יונית המעבירה יונים כגון נתרן או סידן. פתיחה של התעלה תגרום לשטף של יונים אלה לתוך התא, ובכך לדפולריזציה (צמצום הפרש המתחים בין חוץ התא לצד הפנימי של הקרום), והתקרבות של מתח זה לסף בו יוכל התא לייצר פוצנציאל פעולה בעצמו. המוליך העצבי המעורר השכיח במערכת העצבים של יונים הוא חומצת האמינו גלוטמט, ויש לו 3 סוגים של קולטנים יונוטרופיים (תעלות יונים) היכולים לגרום לפוטנציאל פוסט-סינפטי מעורר.
- השפעה מעכבת השכיחה נגרמת כאשר הקולטן הוא תעלה יונית המעבירה יוני כלור, והמוליך העצבי המעכב השכיח במוח של היונקים הוא GABA.
- השפעה מווסתת נגרמת כאשר הקולטן הוא חלבון מסוג G. הפעלה של קולטן כזה ע"י קשירה של המוליך העצבי גורמת לשרשרת ביוכימית בתוך התא המשפיעה בסוף התהליך לפתיחה או סגירה של תעלות יונים, ובכך משנה קלות ולאורך זמן את הפרש המתחים על פני קרום התא. דוגמאות למוליכים עצביים כאלה הם דופמין או סרוטונין, אשר כל הקולטנים שלהם הם חלבוני G.
פינוי[עריכת קוד מקור | עריכה]
כדי לשמור על תזמון מדוייק של פעולת המוליך העצבי והימנעות מהפעלה ממושכת של הקולטנים, המוליך העצבי חייב להיות מפונה במהירות מהמרווח הסינפטי. קיימים שלושה מנגנונים בהם מפונים המוליכים השונים.
- דיפוסיה וספיגה על ידי תאי גליה, בעיקר אסטרוציטים, המקיפים את אזור הסינפסה.
- פירוק על ידי אנזימים. הדוגמה הבולטת הוא אצטיל-כולין, שהעודפים שלו עוברים בסינפסה פירוק מהיר על ידי האנזים אצטלכולין אסתרזה.
- ספיגה חזרה לתוך תא העצב הקדם-סינפטי כדי להיארז בשלפוחיות לשימוש חוזר.
ראו גם[עריכת קוד מקור | עריכה]
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- מוליך עצבי, באתר אנציקלופדיה בריטניקה (באנגלית)
- The Chemical Mind - סרטון הסבר על הכימיה של המוח והמוליכים העצביים

 נוירוטרנסמיטורים, דף שער בספרייה הלאומית
נוירוטרנסמיטורים, דף שער בספרייה הלאומית
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ Li, S. C. (2012). Neuromodulation of behavioral and cognitive development across the life span. Developmental psychology, 48(3), 810.
- ^ 1 2 Mark F. Bear, Barry W. Connors, Michael A. Paradiso, Neuroscience: exploring the brain, 4. ed, Philadelphia: Wolters Kluwer, 2016, עמ' 119-122, ISBN 978-0-7817-7817-6
- ^ 1 2 רמי רחמימוב (2004). מהפכת המוח: תקשורת, מחלות נפש וסמים. רעננה: מכון ון ליר בירושלים הקיבוץ המאוחד.
| תפקוד מערכת העצבים והמוח | ||
|---|---|---|
| תקשורת במערכת העצבים | תא עצב • דחף עצבי • סינפסה • מוליך עצבי • העברה סינפטית • רשת עצבית • הפלסטיות של מערכת העצבים • אפנון עצבי | |
| מערכות תפקודיות | מערכות חישה • המערכת המוטורית • המערכת הלימבית • מערכת החיזוק • המערכת הנוירואנדוקרינית | |
| תפקודים קוגניטיביים | תפיסה • זיכרון • קשב • תפקודים ניהוליים | |
| בדיקות למדידת תפקודים עצביים | EEG - אלקטרואנצפלוגרם • NCT - בדיקת מוליכות עצבית • fMRI - דימות תהודה מגנטית תפקודי • MEG - מגנטואנצפלוגרפיה • PET - טומוגרפיית פליטת פוזיטרונים | |
