איזומר
בכימיה, איזוֹמֵרים הם תרכובות בעלות אותה נוסחה מולקולרית - כלומר אותו מספר אטומים מכל יסוד, אך סדר האטומים, או סידורם המרחבי שונה.
תופעת האיזומריה שכיחה במיוחד בתרכובות אורגניות, זאת לאור מספר האפשרויות הגדול בהן אטומי פחמן יכולים להיקשר אחד לשני ולאטומים אחרים.
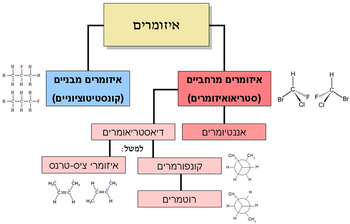
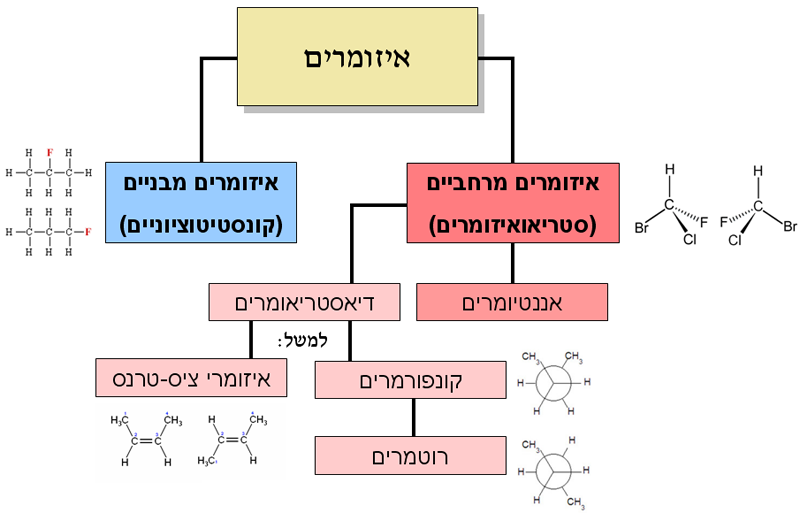
האיזומרים מתחלקים לשני סוגים ראשיים:
- איזומרים מבניים או קונסטיטוציוניים: שני חומרים בהם הסידור המרחבי זהה, אך סדר האטומים שונה. לדוגמה שרשרת פחמימנית המכילה אטום פלואור אחד: אטום הפלואור יכול להופיע בקצה המולקולה או באמצעה, כשאז מתקבלים שני חומרים שונים בעלי נוסחה מולקולרית זהה (בתמונה: הנוסחה C3H7F זהה לשני החומרים). איזומרים מבניים הם תמיד חומרים שונים, בעלי תכונות פיזיקליות (צבע, נקודת רתיחה וכדומה) וכימיות (יכולת להגיב עם חומרים אחרים) שונות.
- איזומרים מרחביים או סטריאואיזומרים: שני חומרים בהם סדר האטומים זהה, אך הסידור המרחבי שונה (למשל כתמונת ראי).
איזומרים מבניים[עריכת קוד מקור | עריכה]
טאוטומרים[עריכת קוד מקור | עריכה]

טאוטומרים (Tautomers) הם איזומרים מבניים הנבדלים זה מזה במיקומו של אטום מימן בודד. טאוטומרים נמצאים בדרך-כלל בשיווי משקל כימי בין שתי צורות מרחביות; המעבר בין שתי הצורות המרחביות נקרא טאוטומריה או טאוטומריזם.
אנולים נמצאים בטאוטומריה עם קטונים, תופעה הקרויה טאוטומריית קטו-אנול.
סטריאואיזומרים[עריכת קוד מקור | עריכה]

סטריאוכימיה היא הענף החוקר את הסטריאואיזומרים. לכיוון, לזווית ולמיקום שבהם נפגשות שתי מולקולות בעת תגובה כימית השפעה מכרעת על הסבירות לקיומה של תגובה בין המולקולות, וכן על התוצרים שיתקבלו. הסטריאוכימיה מנסה להתחקות אחר גורמים אלו. לסטריאוכימיה חשיבות רבה בביולוגיה. תגובה כימית נקראת סטריאוסלקטיבית אם נוצר במהלכה עודף משמעותי של אחד הסטריאואיזומרים.
כאשר בוחנים את האיזומרים המרחביים השונים, לסימטריה שלהם תפקיד חשוב. אטום הפחמן, המוכל בכל תרכובת אורגנית, מסוגל ליצור ארבעה קשרים קוולנטיים עם אטומים אחרים, וקשרים אלה אינם בהכרח סימטריים. אם לאטום פחמן מסוים במולקולה קשורים ארבעה אטומים שונים או קבוצות שונות, הרי שהמולקולה אינה סימטרית סביב אטום זה, וייתכנו איזומרים מרחביים שונים.
לעומת זאת, למולקולות סימטריות, בעלות סימטריית שיקוף (כלומר, ניתן לחצות אותן לשני חלקים זהים המשקפים זה את זה כבמראה), לעולם לא יהיו איזומרים מרחביים. דוגמה לכך היא אטום הפחמן של דיכלורומתאן, בתמונה משמאל, שהוא סימטרי; ניתן להעביר מישור (בין שני אטומי הכלור, למשל) ולחצות את המולקולה לשני חלקים זהים לחלוטין. לדיכלורומתאן, לפיכך, לא יכולים להיות איזומרים מרחביים; אם ננסה לשנות את סדר האטומים (למשל: להחליף בין המיקום של אטום כלור ואטום מימן), תמיד נקבל מולקולות זהות, אותן ניתן להניח האחת על השנייה כך שהן יחפפו לגמרי.
מולקולה שיש לה בבואת ראי שאינה חופפת לה (בדומה לזוג ידיים), מכונה כיראלית (Chiral); מולקולה סימטרית, שבבואת הראי שלה זהה לה (ניתן לחפוף ביניהן, בדומה לסיפרה 8), מכונה אכיראלית. בהתאם לכך נחלקים כל האיזומרים המרחביים לשני סוגים:
- אֵנַנְטיוֹמרים (Enantiomers, או איזומרים אופטיים): שני איזומרים המהווים תמונת ראי זה של זה, ושלא ניתן לחפוף ביניהם. כך, לדוגמה, מולקולות של שני האיזומרים עשויות להכיל אטום מרכזי זהה כאשר סידורי הקשרים של אטום זה (כיראליות) הם בצדדים מנוגדים.
- דִיאַסְטֵרֵיאוֹמרים (Diastereomers): שני איזומרים שאינם מהווים תמונת ראי האחד של השני, והם שונים במרכז כירלי אחד לפחות זה מזה. לדוגמה, במולקולה בעלת שני אטומי פחמן מרכזיים עם קשרים אסימטריים לקבוצות אחרות, שלושת הקשרים הנותרים סביב כל אטום יכולים להיות באותו סדר, או בסדר הפוך בין שני האטומים, כך שיש שני דיאסטראומרים שונים.
אננטיומרים[עריכת קוד מקור | עריכה]
 ערך מורחב – אננטיומר
ערך מורחב – אננטיומר


מקור המושג אננטיומר ביוונית: Enantios פירושו "הפוך". לאננטיומרים, בניגוד לאיזומרים אחרים, תכונות פיזיקליות זהות: הם רותחים וניתכים באותה הטמפרטורה, יש להם צפיפות זהה, וכן הלאה. מצב זה נובע מכך שהקריטריונים הקובעים את התכונות הפיזיקליות כמו הקשרים הכימיים בין אטומי האננטיומרים, מיקום האטומים, אורכי הקשרים, הזוויות וכן הלאה זהים לגמרי.
למרות זאת האננטיומרים אינם זהים מכיוון שניתן להבדיל בין שני אננטיומרים שונים באמצעות הפעילות האופטית שלהם. כשמקרינים גבישים של אננטיומר באור מקוטב מישורית (אור שעובר דרך מסנן אופטי מיוחד המאפשר רק לקרניים במישור מסוים לעבור), הגבישים מסיטים את האור לכיוון מסוים. פעילות אופטית קיימת רק במולקולות כיראליות. שני אננטיומרים שונים מסיטים את האור באותה הזווית בדיוק, אך בכיוון ההפוך. האננטיומר המסיט את האור עם כיוון השעון מסומן בכימיה בסימן פלוס (+), ואילו האננטיומר המסיט את האור כנגד כיוון השעון מסומן בסימן מינוס (−).
אננטיומטרים נפוצים גם בסוכרים למיניהם, חומצות אמינו, ועוד. בביוכימיה הם מסומנים באותיות D ו־L – קיצור של dextrorotary ו־levorotary. אננטיומר D הוא "ברירת המחדל" של הטבע ביצור סוכרים. הבדל הבא לידי ביטוי בסוכרים הוא ביכולת הגוף לפרק אותם – בגוף האדם יש אנזים מיוחד המיועד לפירוק סוכרוז D (הלא הוא הסוכר הרגיל בו אנו משתמשים ביום יום) אך אין אנזים לפירוק סוכרוז L. משמעות הדבר היא שסוכרוז L הוא ממתיק לא משמין שכן יש לו טעם של סוכר, אך הגוף אינו מסוגל לפרקו ולכן אינו נכנס למחזור הדם ואף אינו מסוכן לחולי סוכרת.
איזומרים בביולוגיה[עריכת קוד מקור | עריכה]
מערכות ביולוגיות מדגימות היטב כיצד אננטיומרים הם חומרים שונים. להלן כמה דוגמאות:
- התרופה תלידומיד. אחד האננטיומרים מקל על בחילות שחשות נשים בהריון; האננטיומר השני גורם לפגמים מולדים חמורים בתינוקות.
- החומר קארבון (Carvone). אחד האננטיומרים מקנה ריח לפטרוזיליה ושמיר; האננטיומר השני מקנה ריח לסוג של מנטה (Spearmint).
- החומר לימונן (Limonene). אחד האננטיומרים מקנה ריח ללימון; האננטיומר השני מקנה ריח לתפוז.
להרחבה ראו: סטריאוכימיה.
הסיבה לפעילות השונה של האננטיומרים במערכות הביולוגיות היא שגם האנזימים עצמם, האחראיים, למשל, על הקניית תחושת הריח, הם כיראליים, ובגוף הם מופיעים בדרך-כלל בצורת אחד האננטיומרים בלבד. כך, למשל, אנזים המסיט אור מקוטב עם כיוון השעון מתאים בצורה מושלמת לסובסטרט המסיט אף הוא את האור עם כיוון השעון; התאמתו לאננטיומר השני של הסובסטרט פחותה, והדבר מתבטא בתופעה פיזיולוגית כלשהי, למשל: ההבחנה בין ריח הלימון וריח התפוז.

חומרים כיראליים רבים בטבע מופיעים תמיד בצורת אחד האננטיומרים, ואילו חומרים אחרים מופיעים בשתי הצורות. רוב חומצות האמינו והסוכרים, למשל, מופיעים בצורת אחד האננטיומרים בלבד. הופעתם של חומרים אלו, אבני הבניין של היצורים החיים, כאננטיומר מסוים משפיעה גם ברמת המקרו (הייצור השלם). לקונכיית החלזונות, למשל, מבנה סלילי כיראלי. מסתבר שקונכיות המורכבות מסליל הזורם עם כיוון השעון שכיחות פי 20,000 יותר מקונכיות בהן הסליל זורם כנגד כיוון השעון. זהו אינו צירוף מקרים, אלא תוצאה של סוג האננטיומרים של המולקולות המרכיבות את הקונכיות.
הסיבה לכך שקיימת דומיננטיות בטבע לאננטיומר אחד ולא לשני איננה ידועה, וייתכן שגילויה יאפשר תובנות נוספות בנוגע לאבולוציה ולהיווצרות החיים על-פני כדור הארץ.
בתא קיימים אנזימים רבים הממירים תרכובות מאיזומר אחד שלהן למשנהו. איזומראז הוא שמם הכולל של אנזימים אלו, ודוגמה לכך ניתן למצוא בתהליך הגליקוליזה, בה מומר גלוקוז 6-פוספט לאיזומר שלו - פרוקטוז 6-פוספט - על ידי האנזים פוספוהקסוז איזומראז. במקרה זה משתנה גם הקבוצה הפונקציונלית, והתרכובת הופכת מאלדהיד (או אלדוזה, במקרה של הסוכר גלוקוז) לקטון (פרוקטוז, קטוזה). מאוחר יותר בתהליך הגליקוליזה מומר הקטון דיהידרוקסיאציטון פוספט לאלדהיד גליצראלדהיד 3-פוספט. כל האיזומרים המוזכרים כאן הם איזומרים מבניים ולא מרחביים.
קונפיגורציה מוחלטת[עריכת קוד מקור | עריכה]
לא ידועה שיטה לחיזוי כיוון הסטת האור של אננטיומרים שונים לפי סדר הופעת האטומים בהם[דרוש מקור]. נבחן, לדוגמה, את האננטיומר הימני של ברומוכלורופלואורומתאן (בתמונה). נניח שאננטיומר זה מסיט את האור עם כיוון השעון; אם משנים אחד ממתמיריו (למשל, נחליף את אטום המימן בקבוצת הידרוקסיל, OH), ייתכן שעתה תסיט המולקולה את האור כנגד כיוון השעון - זאת אף על פי שקונפיגורציית האטומים נותרה ללא שינוי.
לאור זאת נקבעה שיטה להגדרת הקונפיגורציה המוחלטת של אננטיומרים. הקונפיגורציה מגדירה את סדר המתמירים סביב אטום הפחמן האסימטרי, ואינה קשורה, כאמור, לכיוון הסטת האור המקוטב. אם המתמירים מסודרים סביב אטום הפחמן עם כיוון השעון (בהמשך תוסבר משמעות העניין), המולקולה מסומנת באות R (קיצור של Rectus, "ימין" בלטינית); אם המתמירים מסודרים כנגד כיוון השעון, המולקולה מסומנת באות S (קיצור של Sinister, "שמאל" בלטינית). אם במולקולה קיימים יותר מאטום פחמן אסימטרי אחד, מצוין S או R עבור כל אחד מהם, בתוספת ספרה המציינת את הפחמן הרלוונטי. לצד סימון הקונפיגורציה המוחלטת ניתן לציין גם את כיוון הסטת האור, זאת כזכור בעזרת מינוס או פלוס. לדוגמה: (2R,3S)-(+)ברומוכלורובוטאן. במולקולה זו 2 פחמנים אסימטריים – לאחד קונפיגורציה מוחלטת R (הפחמן השני בשרשרת) ולשני – S (הפחמן השלישי). המולקולה מסיטה את האור עם כיוון השעון.
היטלי פישר[עריכת קוד מקור | עריכה]
 ערך מורחב – היטל פישר
ערך מורחב – היטל פישר
היטלי פישר, על-שם הכימאי הגרמני הרמן אמיל פישר, זוכה פרס נובל לכימיה בשנת 1902, הם דרך מופשטת להצגה גרפית של המבנה התלת-ממדי של מולקולות. היטלי פישר מאפשרים לקבוע במהירות את הקונפיגורציה המוחלטת של המולקולה.
דיאסטריאומרים[עריכת קוד מקור | עריכה]
 ערך מורחב – דיאסטריאומר
ערך מורחב – דיאסטריאומר
- איזומרי ציס-טרנס (Cis-trans, איזומרים גאומטריים): איזומרים אלו מופיעים בתרכובת בהן קיים קשר קוולנטי כפול בין שני אטומי פחמן, אשר לאף אחד מהם לא קשורים שני מתמירים זהים, ומתמיר מסוג מסוים קשור לשניהם (באלקנים, למשל). האיזומר בו המתמירים המשותפים קשורים לאטומי הפחמן מאותו צד של הקשר הכפול נקרא איזומר הציס, ואילו האיזומר בו המתמירים המשותפים קשורים לאטומי הפחמן מצדדים נגדיים של הקשר הכפול נקרא איזומר הטרנס. קשר כפול, בניגוד לקשר בודד, הוא קשיח, ואינו מאפשר סיבוב. לפיכך, לא ניתן לעבור בין איזומר ציס לאיזומר טרנס ללא שבירת קשרים.
ראו גם[עריכת קוד מקור | עריכה]
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- איזומר, באתר אנציקלופדיה בריטניקה (באנגלית)