מחלת נגיף הזיקה
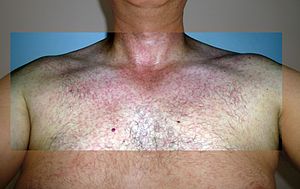 | |
| פריחה על חזה של חולה במחלת נגיף הזיקה | |
| תחום |
מחלות זיהומיות |
|---|---|
| גורם |
נגיף זיקה |
| תסמינים |
חום, פריחה מקולופפולרית, כאבי מפרקים, דלקת הלחמית, כאב ראש |
| קישורים ומאגרי מידע | |
| DiseasesDB | 36480 |
| MeSH | D000071243 |
| סיווגים | |
| ICD-10 | A92.8, U06 |
| ICD-11 |
1D48 |
מחלת נגיף הזיקה (באנגלית: zika fever, נקראת גם: קדחת הזיקה או זיקה) היא מחלה נגיפית הנגרמת בגלל נגיף הזיקה ומועברת בדרך כלל על ידי עקיצות יתושים מסוג אדס[1], אך יכולה לעבור גם באמצעות קיום יחסי מין, עירוי דם ומעבר בין אם לעובר[2]. ברוב המקרים, המחלה היא א-סימפטומטית, וגם כאשר מתגלים תסמינים הם יחסית מתונים, ועלולים להזכיר מחלות אחרות, כדוגמת קדחת דנגי[3]. תינוקות שנדבקו במחלה על ידי אימם במהלך ההיריון עלולים לסבול ממיקרוצפליה או ממומים מוחיים אחרים[4]. בקרב מבוגרים שנדבקו בנגיף, נראה כי המחלה עלולה לגרום לתסמונת גייאן-בארה[3].
תסמינים[עריכת קוד מקור | עריכה]
כ-80% ממי שנדבק בנגיף הזיקה לא ייפתח תסמינים למחלה כלל[5]. במקרים בהם כן מתפתחים תסמינים, הם עלולים לכלול בין היתר: חום, פריחה, דלקת הלחמית, כאבי פרקים (אנ') וכאבי שרירים[6][2][1]. תקופת הדגירה של המחלה היא כ-3 עד 12 ימים[5]. לרוב, תסמיני המחלה אינם חמורים וניתן להחלים מהמחלה גם ללא התערבות רפואית[2][3].
הריון[עריכת קוד מקור | עריכה]

הסכנה העיקרית של מחלת נגיף הזיקה היא לעוברים של נשים הרות שנדבקות בנגיף הזיקה[5][7]. במקרים כאלו, ההדבקות במחלה עלולה לגרום להפלת העובר או לבעיות התפתחות, כאשר המרכזית שבהן היא מיקרוצפליה. לפי ההערכות כ-42% מהתינוקות שנולדים לאימהות שנדבקו במחלה סובלים מרמה מסוימת של מומים, כאשר הנפוצים ביותר הם מומים בהתפתחות המוח והעין כגון מיקרוצפליה ורקמת צלקת בשכבה הדמית של העין[8][8]. במקרים חריגים, נצפו גם מומים רב-מערכתיים כדוגמת הידרופס פטאליס[9][10]. מומים אלו עלולים לגרום לבעיות התפתחותיות של העובר ולגרום להפרעות נוירולוגיות כמו: אפילפסיה, לקויות בשמיעה ובראייה והפרעות פסיכומוטוריות. הסכנה להתפתחות מיקרוצפליה גדלה ככל שההדבקות של האם במחלה היא בשלב מוקדם יותר של ההריון[7]. קיימים נתונים סותרים בנוגע לאחוז ההריונות של נשים החולות במחלה שהובילו למיקרוצפליה, אך נמצא כי גם תינוקות שנולדו עם היקף ראש תקין וללא מומים הנראים לעין, עלולים לפתח מומים מוחיים או נזק מוחי בשלב מאוחר יותר.
תסמונת גייאן-בארה[עריכת קוד מקור | עריכה]
בקרב מבוגרים, נמצא קשר בין מחלת נגיף הזיקה לבין תסמונת גייאן-בארה. תסמונת זו גורמת להחלשות שרירים בעקבות פגיעה של מערכת החיסון במערכת העצבים ההיקפית, פגיעה שעלולה לגרום אף לשיתוק[11]. על אף שלא ניתן לבודד את מחלת נגיף הזיקה כגורם וודאי לתסמונת גייאן-בארה, במספר מדינות שבהן פרצה מגפת הזיקה נרשמה עלייה בשיעור היארעות התסמונת. למשל, בהתפרצות המגפה בפולינזיה הצרפתית בשנים 2013–2014 נרשמו 42 מקרים של תסמונת גייאן-בארה בתקופה של 3 חודשים בלבד. לצורך השוואה, לפני ההתפרצות נרשמו בין 3 ל-10 מקרים בשנה[12].
הדבקות בנגיף[עריכת קוד מקור | עריכה]

נגיף הזיקה הוא וירוס ממשפחת פלאוויווירידה (Flaviviridae) שמועבר על ידי יתושים מסוג אדס. משפחת וירוסים זאת, מקושרת למחלות נוספות כמו קדחת צהובה וקדחת דנגי. על אף שיתושים הם הנשאים של המחלה, המקור העיקרי להפצתה טרם נמצא. אף על פי כן, נמצאו עדויות סרולוגיות לכך שהמחלה עשויה להתפתח מקופים מערב-אפריקאיים וממכרסמים[13][14].
העברה[עריכת קוד מקור | עריכה]
דרך ההדבקות העיקרית היא על ידי עקיצת יתושים מסוג אדס, כאשר המין הנפוץ מביניהם הוא אדס מצרי (אנ') (aedes aegypti). הנגיף גם מופץ על ידי מינים נוספים של יתושי אדס: אדס אפריקאי (אנ') (aedes africanus), אדס אפיקוארגנטוס (אנ') (aedes apicoargenteus), אדס לוטאוספלוס (אנ') (aedes luteocephalus), יתוש הטיגריס האסייתי (aedes albopictus), אדס ויטאטוס (אנ') (aedes vittatus) ואדס פורסיפר (אנ') (aedes furcifer). בנוסף למינים אלו, קיים המין אדס הנסילי (אנ') (aedes hensilli) שהוביל להתפרצות מחלת נגיף הזיקה באי יאפ שבמיקרונזיה בשנת 2007, והמין אדס פולינסיס (אנ') (aedes polynesiensis) שהיה אחראי להתפרצות בפולינזיה הצרפתית בשנת 2013[15][16][17][18].
נגיף הזיקה עשוי להיות מועבר בעת קיום יחסי מין[19][20][21]. בדגימת זרע שנלקחה מגבר שבועיים לאחר ההדבקות בנגיף, נמצאו פי 100,000 יותר נגיפים מאשר בדגימת דם או שתן שנלקחו ממנו[22]. לא ברור מדוע המצאות הנגיף בזרע גבוהה יותר מאשר בנוזלי גוף אחרים, וגם לא ידוע כמה זמן יכול הנגיף להישאר בנוזלי הזרע. היו גם מקרים של גברים שהיו ללא תסמינים למחלת הזיקה, ובכל זאת העבירו את המחלה. המרכז לבקרת מחלות ומניעתן (CDC), ממליץ לגברים שביקרו באזורים נגועי זיקה, להימנע מלקיים יחסי מין במטרה לגרום להריון במשך כחצי שנה, גם אם הם אינם מגלים סימני מחלה[23]. אף על פי שקיימים מקרים רבים יותר של גברים שהעבירו את המחלה, דווחו גם מקרים שנשים הן אלו שהעבירו את המחלה לבני זוגם[24]. יחסי מין ואגינאליים, אנאליים ואוראליים, עשויים להביא להדבקה בנגיף.
קיימים דיווחים על מקרים של העברת הנגיף מהאם לעובר במהלך ההריון[25]. המרכז לבקרת מחלות ומניעתן (CDC) ממליץ לנשים החולות במחלת נגיף הזיקה להמתין לפחות 8 שבועות לאחר היחשפות למחלה, בטרם ינסו להיכנס להריון. לא דווחו על מקרים של העברת הנגיף מהאם דרך הנקה, אך הנגיף אותר בחלב אם[26].
כמו וירוסים אחרים מסוג פלאוויווירוס (אנ'), גם נגיף הזיקה עשוי לעבור בעירויי דם ובהשתלת איברים. כמה מדינות הנגועות בנגיף הזיקה, פיתחו שיטות לבדיקת הימצאות הנגיף בתרומות דם. למשל, בפולינזיה הצרפתית, הנגיף אותר ב-3% מקרב תורמי הדם שלא גילו תסמינים למחלה.
מנגנון המחלה[עריכת קוד מקור | עריכה]
מחקר רב בוצע, ועדיין מבוצע, כדי להבין את מנגנון הפגיעה של נגיף הזיקה, וכיצד הוא גורם למיקרוצפליה ולמומים נוירולוגיים. אחת ההנחות היא שהנגיף גורם לזיהומים בתאי הגזע של מערכת העצבים המרכזית של העובר[27][10]. תפקידם העיקרי של תאי גזע אלו הוא להשתכפל ולהתרבות עד לייצור כמות מספקת של תאי עצב. החלבונים של נגיף הזיקה, NS4A ו-NS4B, נמצאו כגורמים המדכאים את תהליך ייצור תאי העצב[10]. זיהום בתאי הגזע במוח עלול לגרום למוות של תאים, מה שמוביל לפגיעה בייצור עתידי של תאי עצב ולבסוף למומים במבנה המוח. כמו כן, הווירוס עלול לגרום לטרופיזם של תאים בעין, ובכך לגרום לשיעור גבוה של מומים במבנה העין[10].
מספר רב של מקרי מיקרוצפליה קושרו להורשה של מוטציות בגנים, במיוחד מוטציות שקשורות לפגיעה בכישור החלוקה - שלב חשוב בתהליך החלוקה של התא. ישנן ראיות לכך שנגיף הזיקה גורם באופן ישיר או עקיף לפגיעה בתהליך המיטוזה של התא[28]. כיוון מחקרי נוסף בוחן את האפשרות שנגיף הזיקה, בשונה מנגיפים אחרים ממשפחת פלאוויווירידה, תוקף תאי מוח המתפתחים בעובר לאחר שהוא עובר את השלייה וגורם לפגיעה בהם. בעקבות פגיעה זו המערכת החיסונית מנסה לפגוע בתאים המזוהמים וכתוצאה מכך, נגרמת הפגיעה במוח התינוק כנזק אגבי של פעילות המערכת החיסונית[29].
אבחון[עריכת קוד מקור | עריכה]
קשה לאבחן את המחלה באמצעות תסמינים קליניים ואנמנזה בלבד, זאת משום שקיימת חפיפה בין תסמינים של מחלת הזיקה עם תסמינים של מחלות אחרות שמועברות באופן דומה. כמו כן, באזורים הנגועים במחלת הזיקה, נפוצות אותן מחלות דומות בדרך כלל[30][31]. המרכז לבקרת מחלות ולמניעתן (CDC) מוסיף כי "בהתבסס על התסמינים ההקליניים האופייניים, האבחנה המבדלת למחלת נגיף הזיקה היא רחבה. המאבחן צריך לקחת בחשבון בנוסף לקדחת דנגי, גם מחלות וחיידקים נוספים כגון: עכברת, מלריה, ריקציה, סטרפטוקוקוס מסוג A, אדמת, חצבת ומחלות הנגרמות מהנגיפים: adenoviridae, פרבו-וירוס (אנ') (parvovirus), אנטרו-וירוס (Enterovirus) ואלפא-וירוס (אנ') (alphavirus), (כדוגמת המחלות: צ'יקונגוניה, מחלת נגיף המיירו (אנ'), קדחת נהר רוס (אנ'), מחלת נגיף יער ברמה (אנ'), מחלת נגיף O'nyong-nyong ומחלת נגיף הסינדביס (אנ')).
קיימת בדיקת דם לזיהוי מחלת הזיקה אך היא אינה חד משמעית[5]. ברוב המקרים, בדיקות דם שבוצעו לחולים שהמחלה אצלם הייתה מתונה, הראו תוצאות תקינות. למרות זאת, עבור מעט חולים, נצפה מיעוט כדוריות דם לבנות, מיעוט טסיות דם ועלייה בתפקודי כבד[32]. ניתן לאבחן את המחלה בחולים במצב קשה באמצעות טכניקת RT-PCR. הזמן שלוקח לנגיף להיכנס לזרם הדם ולהתפשט בכל הגוף הוא קצר יחסית[3], לכן ארגון הבריאות העולמי מציע לבצע את בדיקת RT-PCR על דגימות דם שנלקחו תוך 1–3 ימים מהופעת התסמינים, או על דגימת רוק שנאספה תוך 3–5 מהופעת התסמינים. כאשר השוו את הימצאות הנגיף בדגימות המדוברות, נמצא כי הנגיף אותר יותר בקרב דגימות הרוק[32]. בבדיקת שתן, ניתן לאתר את הנגיף עד 14 ימים מהופעת התסמינים. הזמן הארוך ביותר בו אותר נגיף הזיקה לאחר תחילת הופעת הסימפטומים היה 11 ימים. לאחר זמן זה, ניתן לבדוק בדם שאריות של נוגדנים ספציפיים של נגיף הזיקה, נוגדנים המעידים שבגוף הייתה המחלה.
משום שהבדיקה איננה חד משמעית, משרד הבריאות ממליץ לבדוק רק חולים שפיתחו סימפטומים למחלה בתקופה של עד שבועיים מרגע החשיפה לנגיף, תינוקות שנולדו לנשים שנחשפו לנגיף הזיקה, ואנשים שנחשפו למחלה והם מתלוננים על בעיות נוירולוגיות שאינן מוסברות.
בדיקת נשים הרות[עריכת קוד מקור | עריכה]
המרכז האמריקאי לבקרת מחלות ולמניעתן ממליץ לבדוק נשים הרות שנמצאות בסיכון להידבק בנגיף, גם אם הן אינן מגלות תסמינים למחלה. נשים הרות שביקרו באזורים נגועי זיקה, צריכות להיבדק תוך שבועיים ועד 12 שבועות מרגע חזרתן לארצן[33]. במקרה שהאישה מפתחת תסמינים שעלולים לנבוע ממחלת הזיקה, עליה לפנות לרופא המטפל[33]. אם התגלה כי האישה אכן חולה במחלת הזיקה, משרד הבריאות ממליץ לבצע מעקב הריון במרפאה להריון בסיכון גבוה[5].
בדיקת תינוקות[עריכת קוד מקור | עריכה]
כאמור, משרד הבריאות הישראלי ממליץ לבדוק כל תינוק שנולד לאישה שנחשפה לנגיף במהלך ההריון. המרכז לבקרת מחלות ממליץ לבצע בדיקת דם, בדיקת שתן ובדיקות ביולוגיות (כדוגמת RT-PCR) לכל עובר שנולד לאם חשופה[34]. במקרה בו האם אובחנה כחולה במחלת נגיף הזיקה, יש לבצע בדיקות נוספות ומעקב אחר התפתחות המוח ומבנה ראש התינוק (מיקרוצפליה), בדיקות לאיתור מומים נוירולוגיים ומעקב אחר פריחות ומחלות עור[34]. בדיקות מומלצות נוספות הן אולטראסאונד תוך-גולגולתי (אנ') ובדיקות שמיעה[35] וראייה. בנוסף לכך, יש לבצע בדיקות לזיהומים מולדים כדוגמת: עגבת, טוקסופלזמוזיס, CMV, הרפס סימפלקס, דלקת קרום המוח ואדמת[34]. על חלק מהבדיקות יש לחזור כמה פעמים, עד גיל חצי שנה של התינוק, משום שחלק מהבעיות עשויות להתגלות מאוחר יותר, במיוחד בעיות שמיעה[34].
מניעה[עריכת קוד מקור | עריכה]

הנגיף מופץ על ידי עקיצות יתוש, לכן הימנעות מיתושים היא צעד משמעותי בהגנה מפני הנגיף. משרד הבריאות והמרכז האמריקאי לבקרת מחלות ולמניעתן ממליצים למי שמגיע לאזורים הנגועים בזיקה לנקוט באמצעים הבאים[36][5]: מריחה של חומר דוחה יתושים; לבוש ארוך: חולצה עם שרוולים ארוכים, מכנסיים ארוכים, כובע וגרביים; לינה בחדרים המוגנים מפני יתושים על ידי רשתות תקינות בחלונות ובדלתות, חדר סגור וממוזג, או שינה תחת כילה. משום שמחלת נגיף הזיקה עלולה לעבור בעת קיום יחסי מין, גברים שביקרו באזורים הנגועים בזיקה צריכים להשתדל להימנע מקיום יחסי מין, או להשתמש בקונדומים לתקופה של עד 6 חודשים מרגע חזרתם. הנקה עדיין מומלצת על ידי ארגון הבריאות העולמי (WHO), גם בקרב נשים שאובחנו כחולות במחלה. לא תועד אף מקרה של הדבקה בנגיף על ידי הנקה, זאת אף על פי שהנגיף אותר בחלב אם. לאחר החזרה לארץ המוצא, מומלץ להמשיך להימנע מעקיצות יתושים למשך תקופה של שלושה שבועות כדי למנוע מיתושים נוספים להפוך להיות נשאים של המחלה.
אזהרת מסע של ה-CDC[עריכת קוד מקור | עריכה]
בעקבות "התחזקות הראיות לקשר בין מחלת הזיקה לבין מיקרוצפליה", הפיץ המרכז האמריקאי לבקרת מחלות (ינואר 2016) אזהרת מסע המייעצת לנשים הרות להימנע מביקור במדינות או באזורים בהם קיימת העברה פעילה של הנגיף[37]. עבור גברים הנמצאים בזוגיות עם אישה הרה, או זוגות השוקלים להיכנס להריון, וחייבים להגיע לאזורים המדוברים, מומלץ להשתמש בקונדומים, או להימנע מיחסי מין (מכל סוג - אוראלי, אנאלי או וגינאלי) לחלוטין[38].
רשימת אזורים ומדינות עם סיכון להעברה מקומית של נגיף הזיקה, האגף לאפידמיולוגיה, משרד הבריאות (18.03.2018)[39]:
- דרום אמריקה: אקוודור, ארגנטינה, בוליביה, ברזיל, גויאנה, גיאנה הצרפתית, וונצואלה, סורינאם, פרגוואי, פרו וקולומביה.
- מרכז אמריקה והאיים הקריביים: איי הבתולה של ארצות הברית, איי הבתולה הבריטיים, איי טרקס וקייקוס, אל-סלבדור, אנגווילה, אנטיגואה וברבודה, ארובה, בונר, בליז, ברבדוס, ג'מייקה, גואטמלה, גרנדרה, דומיניקה, האיטי, הונדורס, הרפובליקה הדומיניקנית, טרינידד/טובגו, מונטסראט, ניקרגואה, סינט אוסטטיוס וסאבה, סינט מארטן, סנט לוציה, סנט מרטין, סנט וינסנט/גרנדין, סנט קיטס ונוויס, פוארטו ריקו, פנמה, קובה, קוסטה ריקה, קוראסאו.
- צפון אמריקה: ארצות הברית (טקסס) ומקסיקו.
- אפריקה: אוגנדה, אנגולה, אקווטוריאל גינאה, בורונדי, בורקינה פאסו, בנין, גאנה, גבון, גינאה, גמביה, ג'נאה ביסו, דרום סודאן, טוגו, טנזניה, ליבריה, מאלי, ניגר, ניגריה, סודאן, סיארה לאון, סנגאל קייפ, צ'אד, קונגו, קוט דלויאור, קייפ ורדה, קמרון, קניה, רואנדה, קונגו, רפובליקה מרכז אפריקה.
- אסיה: איים מלדיביים, אינדונזיה, בנגלדש, בורמה, הודו, וייטנאם, טימור לסטה, לאוס, מלזיה, סינגפור, פקיסטן, פיליפינים, קמבודיה ותאילנד.
- מערב האוקיינוס השקט: איי סלומון, טונגה, סמואה, פיג'י, פפואה ניו גינאה.
תגובת ארגון הבריאות העולמי (WHO)[עריכת קוד מקור | עריכה]
הן ארגון הבריאות האמריקאי (PAHO) והן ארגון הבריאות העולמי הביעו את חששם מההתפשטות הרחבה של נגיף הזיקה והקשר שנמצא בינו לבין המיקרוצפליה ולתסמונת גייאן-בארה[40]. ראש ארגון הבריאות העולמית מרגרט צ'אן הודיעה בפברואר 2016 "העלייה במקרי המיקרוצפליה ובהפרעות נוירולוגיות אחרות שדווחו בברזיל, ובאו לאחר עלייה דומה בפולינזיה הצרפתית בשנת 2014, מייצרות מצב חירום בנושא בריאות הציבור שהוא בעל חשיבות בין-לאומית". הכרזה זו אפשרה לארגון הבריאות העולמי לייצר תגובה בין-לאומית משותפת לעצירת ההתפרצות, ובנוסף, אפשרה לארגון לפעול תחת חוקים בין-לאומיים במסגרת תקנות בריאות עולמיות[41]. בנובמבר של אותה שנה, הסתיימה הכרזת חירום זו[42].
חיסון[עריכת קוד מקור | עריכה]
נכון להיום אין חיסון מניעתי כנגד המחלה[5]. ייצור חיסון שכזה עלול לקחת שנים[3], ועל אף ההתפרצויות הגדולות של השנים 2014 ו-2016, ארגוני הבריאות לא הצליחו לייצר חיסון מונע למחלה.
בקרת יתושים[עריכת קוד מקור | עריכה]

מאמציהם העיקריים של ארגוני מניעת ובקרת המחלות באזורים הנגועים, סובבים סביב בקרת יתושים. קיימים כמה אופני פעולה למיגור ולשליטה בהפצת הווירוס על ידי היתוש אדס מצרי (aedes aegypti). ביניהם הרס של אזורי רבייה של היתוש, כמו גם קטילה אקטיבית של יתושים צעירים ובוגרים[43]. בנוסף, טכנולוגיות חדשניות למיגור יתושים נמצאות בשלבי פיתוח, וארגון הבריאות אישר שימוש בשיטות מודרניות לבקרה על יתושים כדוגמת השימוש בבקטריה בשם וולבחיה (אנ') (wolbachia) שמחלישה את עמידות היתוש לנגיף. כמו כן, מופצים יתושים עקרים שמטרתם להזדווג עם יתושות ובכך להביא לצמצום אוכלוסיית היתושים הללו[43].
טיפול[עריכת קוד מקור | עריכה]
כיום, אין טיפול ספציפי נגד מחלת הזיקה. טיפול נלווה למחלה כולל טיפול בתסמינים ובתופעות הלוואי שלה, כמו הורדת חום, משככי כאבים וטיפול בגירודים[18]. חלק מהרשויות, וביניהן איגוד רופאי המשפחה בישראל[7], ממליצים להימנע מטיפול באספירין ובתרופות נוגדות דלקת שאינן סטרואידים (NSAIDs) משום שתרופות אלו עלולות לגרום לדימום, כאשר הן מטופלות נגד מחלות דומות למחלת הזיקה שנגרמות בעקבות נגיפים אחרים ממשפחת פלאוויווירידה, כדומת קדחת דנגי[44][45]. מחלת נגיף הזיקה נחקרה מעט מאוד על להתפרצות הגדולה בשנת 2015, ולכן אין טיפול יעיל נגד נגיף הזיקה עד היום[45]. לפיכך ההמלצה לנשים הרות להימנע ככל הניתן מאפשרות להידבקות במחלה כה חשובה שכן אין טיפול אפקטיבי למחלה[46].
אפידמיולוגיה[עריכת קוד מקור | עריכה]
היסטוריה[עריכת קוד מקור | עריכה]

באפריל 1947, כחלק ממחקר של מחלת הקדחת הצהובה, 6 קופים מסוג מקוק רזוס שוחררו ביער "זיקה" שבאוגנדה (מכאן קיבל הנגיף את שמו)[47]. ב-18 באפריל, אחד הקופים (קוף מספר 776) פיתח חום. בדיקות דם שנלקחו מהקוף גילו את המקרה הידוע הראשון של מחלת נגיף הזיקה[13][47]. בהמשך לכך, בוצע בתקופה זו מדגם אוכלוסייה באוגנדה שגילה כי בדמם של 6.1% ממשתתפי המדגם נמצא נגיף הזיקה[25]. בשנת 1954, דווחו המקרים הראשונים של מחלת נגיף הזיקה בבני אדם, בניגריה[48]. מאז, כבר דווחו מספר התפרצויות באזורים הטרופיים של אפריקה ובכמה אזורים בדרום מזרח אסיה[49]. באותה תקופה לא דווח על אף מקרה של נגיף הזיקה בתת היבשת ההודית, אך נמצאו נוגדנים לנגיף הזיקה בקרב אנשים בריאים בהודו. ממצא זה עשוי להעיד שהם נחשפו בעבר לנגיף, אך הוא גם עשוי להיות בעקבות חשיפה למחלה דומה הנגרמת מנגיף אחר מאותה משפחה של נגיף הזיקה[50].
על ידי שימוש באנליזה פילוגנטית על מוצאים אסייתים, מעריכים כי נגיף הזיקה הופץ לדרום מערב אסיה בשנת 1945. בשנים 1977–1978, מחלת נגיף הזיקה תוארה כגורמת לחום באינדונזיה[51]. למרות כל זאת, עד שנת 2007 דווחו רק 13 מקרים של הידבקות טבעית במחלת נגיף הזיקה, כולם בעלי תסמינים מעטים וחלשים[52][13].
התפרצות באיי יאפ[עריכת קוד מקור | עריכה]
בשנת 2007 התרחשה ההתפרצות הראשונה של מחלת הזיקה באיי יאפ שתחת שליטת מדינת מיקרונזיה. בהתפרצות זו חלו 185 חולים. הסימפטומים העיקריים בהתפרצות היו: פריחה, חום, כאבי פרקים ודלקת הלחמית. במהלך ההתפרצות, לא נרשם אף מקרה מוות כתוצאה מהמחלה[53][25].
ההתפרצות באוקיאניה[עריכת קוד מקור | עריכה]
בין השנים 2013–2014 קרו מספר התפרצויות בפולינזיה הצרפתית, בקלדוניה החדשה, באי הפסחא ובאיי קוק[25]. ההתפרצות הגדולה ביותר מבין ההתפרצויות הללו הייתה בפולינזיה הצרפתית בה דווחו על 8,723 מקרים מאומתים של המחלה[54]. בהתפרצות זו טופלו 29,000 אנשים בעלי תסמינים המזכירים את מחלת הזיקה, מחשש שלקו במחלה. מספר זה מהווה כ-11.5% מאוכלוסיית פולינזיה הצרפתית[55]. לפי ההערכות, במחלה חלו כ-30 אלף בני אדם, אשר רק חלקם פנו לקבלת טיפול רפואי. בשאר האיים באזור ההתפרצויות היו קטנות יותר. בקלדוניה החדשה כ-1,400 חולים[54]; באיי קוק כ-1,000 חולים[54]; ובאי הפסחא כ-200 חולים[56].
ההתפרצות ביבשת אמריקה[עריכת קוד מקור | עריכה]
לפי ניתוח גנטי, מוערך כי נגיף הזיקה הגיע לראשונה ליבשת אמריקה בין מאי לדצמבר 2013[57]. הנגיף אותר לראשונה בצפון אמריקה בפברואר 2014 ובמהרה התפשט לדרום ולמרכז אמריקה, והגיע למקסיקו בנובמבר 2015[58][25]. מקרה המוות הראשון בארצות הברית בעקבות נגיף הזיקה קרה בפברואר 2016[59]. ההתפרצות הגדולה החלה בברזיל וממנה התפשטה לשאר היבשת. במאי 2015 ברזיל דיווחה לראשונה על 16 מקרי מחלה של זיקה[60]. זאת על אף שתייר שעזב את המדינה כבר במרץ של אותה שנה, נמצא חולה בזיקה[61]. עד סוף שנת 2015 ברזיל לא ידעה לתת מספר מדויק של מקרי מחלת הזיקה מכיוון שלא בוצע מעקב אחר התחלואה במחלה. אף על פי כן, מוערך כי בשנת 2015, מחלת נגיף הזיקה הייתה הגורם לכ-2,400 מקרי מיקרוצפליה ולמותם של 29 ילודים[62][63][64]. עד לאותה התפרצות, דווח בברזיל על ממוצע של בין 150–200 מקרים של מיקרוצפליה[65]. במדינה פרנמבוקו שבברזיל, גדל שיעור המיקרוצפליה בשנת 2015 פי 77 בהשוואה לחמש השנים שלפני כן[65]. מודל סטטיסטי שבוצע על נתונים מפולינזיה הצרפתית, מצא כי הסיכוי למיקרוצפיה לילדים שנולדו לאם שנדבקה במחלה בשליש הראשון של ההריון הוא 1%[66]. בשנת 2016 הכריז ארגון הבריאות העולמי על מקרה חירום בין-לאומי בעניין בריאות הציבור. במהלך התפרצות זו, שהייתה הגדולה מכולן, נרשמו כ-700,000 חולים במחלת הזיקה ועוד כ-15 מקרי מוות (מספרים אלו אינם כוללים מיתות של תינוקות או הפלות)[67].
בשנת 2016 התקיימו בברזיל המשחקים האולימפיים. לאור התפרצות המחלה בתקופה זו, החלו קריאות של מומחים ורופאים רבים הקוראים לדחיית האולימפיאדה, או להעברתה למקום אחר. מדינות רבות הוציאו אזהרות מסע להגעה לברזיל. צעד זה גרם לירידה בתיירות הספורט למרות קיומה של האולימפיאדה. יתר על כן, חשש רב צף בקרב אתלטים וספורטאים רבים בנוגע להגעה לברזיל. הרוכב האמריקאי טג'יי ואן גרדרן (Tejay Van Garderen) אף הודיע על פרישה מהמשחקים האולימפיים[68]. למרות כל זאת, ארגון הבריאות העולמי הודיע כי אין סיבה לדחות או להעביר את האולימפיאדה[69].
ההתפרצות באסיה[עריכת קוד מקור | עריכה]
בשנת 2016 אותר נגיף הזיקה בכל מדינות אסיה למעט: ברוניי, הונג קונג, מיאנמר ונפאל[70]. אף על פי שהייתה עלייה במספר מקרי המחלה לאחר אולימפיאדת ריו, ניתוח גנטי מראה כי הנגיף הגיע ככל הנראה מתאילנד ולא מדרום אמריקה[71][72][73].
ראו גם[עריכת קוד מקור | עריכה]
קישורים חיצוניים[עריכת קוד מקור | עריכה]
- מחלת נגיף הזיקה באתר משרד הבריאות
- הערך "התפרצות מחלת נגיף הזיקה", באתר ויקירפואה
- הערך "נגיף הזיקה - נייר עמדה", באתר ויקירפואה
- אתר של ארגון הבריאות העולמי בנושא מחלת נגיף הזיקה (באנגלית)
- דף בנושא מחלת נגיף הזיקה באתר של המרכז האמריקאי לבקרת מחלות ומניעתן (CDC) (באנגלית)
- אתר של ארגון הבריאות הפאן-אמריקאי (PAHO) בנושא מחלת נגיף הזיקה (באנגלית)
- רותם אליזרע, 30 חולי זיקה ישראלים בשנה וחצי; חצי מהנדבקים - מהמזרח, חדשות הבריאות - ynet, 9 ביולי 2017
- רן לוצקי, הזמזום שמאיים על האולימפיאדה, ידיעות אחרונות, 2 בפברואר 2016
 אמיר ענבר, הנגיף זיקה מאיים להדביק גם את אולימפיאדת ריו, באתר הארץ, 31 בינואר 2016
אמיר ענבר, הנגיף זיקה מאיים להדביק גם את אולימפיאדת ריו, באתר הארץ, 31 בינואר 2016
הערות שוליים[עריכת קוד מקור | עריכה]
- ^ 1 2 American College of Physicians, Annals of internal medicine., Annals of internal medicine., 0000 u
- ^ 1 2 3 Zika virus, www.who.int (באנגלית)
- ^ 1 2 3 4 5 Zika virus infection, European Centre for Disease Prevention and Control (באנגלית)
- ^ Sonja A. Rasmussen, Denise J. Jamieson, Margaret A. Honein, Lyle R. Petersen, Zika Virus and Birth Defects — Reviewing the Evidence for Causality, https://doi.org/10.1056/NEJMsr1604338, 2016-04-13 (באנגלית)
- ^ 1 2 3 4 5 6 7 תחלואה בזיהום הנגרם על ידי נגיף זיקה, באתר משרד הבריאות
- ^ D. Musso, E.J. Nilles, V.-M. Cao-Lormeau, Rapid spread of emerging Zika virus in the Pacific area, Clinical Microbiology and Infection 20, 2014-10-01, עמ' O595–O596 doi: 10.1111/1469-0691.12707
- ^ 1 2 3 נגיף הזיקה - נייר עמדה – ויקירפואה, באתר www.wikirefua.org.il
- ^ 1 2 P. Brasil, J.P. Pereira, M.E. Moreira, R.M. Ribeiro Nogueira, Zika Virus Infection in Pregnant Women in Rio de Janeiro, The New England journal of medicine 375, 2016-12-15, עמ' 2321–2334 doi: 10.1056/NEJMoa1602412
- ^ Antonio R. P. de Almeida, Albert I. Ko, Nikos Vasilakis, Nivison Nery Jr, Zika Virus Infection and Stillbirths: A Case of Hydrops Fetalis, Hydranencephaly and Fetal Demise, PLOS Neglected Tropical Diseases 10, 2016-02-25, עמ' e0004517 doi: 10.1371/journal.pntd.0004517
- ^ 1 2 3 4 Hongda Li, Laura Saucedo-Cuevas, Sujan Shresta, Joseph G.Gleeson, The Neurobiology of Zika Virus, Neuron 92, 2016-12-07, עמ' 949–958 doi: 10.1016/j.neuron.2016.11.031
- ^ Jennifer A. Frontera, Ivan R. F. da Silva, Zika Getting on Your Nerves? The Association with the Guillain–Barré Syndrome, https://doi.org/10.1056/NEJMe1611840, 2016-10-05 (באנגלית)
- ^ Van-Mai Cao-Lormeau, Alexandre Blake, Sandrine Mons, Stéphane Lastère Phar, Claudine Roche, Jessica Vanhomwegen, Timothée Dub, Laure Baudouin, Anita Teissier, Philippe Larre, Anne-Laure Vial, Christophe Decam, Valérie Choumet, Susan K Halstead, Hugh J Willison, Lucile Musset, Jean-Claude Manuguerra, Philippe Despres, Emmanuel Fournier, Henri-Pierre Mallet, Didier Musso, Arnaud Fontanet, Jean Neil, Frédéric Ghawché, Guillain-Barré Syndrome outbreak associated with Zika virus infection in French Polynesia: a case-control study, The Lancet 387, 2016-04-09, עמ' 1531–1539 doi: 10.1016/S0140-6736(16)00562-6
- ^ 1 2 3 E. B. Hayes, Zika Virus Outside Africa - Volume 15, Number 9—September 2009 - Emerging Infectious Diseases journal - CDC, Emerging Infectious Diseases journal doi: 10.3201/eid1509.090442
- ^ Manfred Brack, Agents Transmissible from Simians to Man, Springer Science & Business Media, 2012-12-06. (באנגלית)
- ^ WRBU: Aedes luteocephala, web.archive.org, 2016-01-28
- ^ Eric Maurice Leroy, Christophe Paupy, Didier Fontenille, Davy Jiolle, Zika Virus in Gabon (Central Africa) – 2007: A New Threat from Aedes albopictus?, PLOS Neglected Tropical Diseases 8, 2014-02-06, עמ' e2681 doi: 10.1371/journal.pntd.0002681
- ^ Cheong-Huat Tan, Lee-Ching Ng, Chee-Seng Chong, Mei-zhi Irene Li, Aedes (Stegomyia) albopictus (Skuse): A Potential Vector of Zika Virus in Singapore, PLOS Neglected Tropical Diseases 7, 2013-08-01, עמ' e2348 doi: 10.1371/journal.pntd.0002348
- ^ 1 2 WHO Western Pacific | World Health Organization, www.who.int (באנגלית)
- ^ Alexandra M. Oster, Interim Guidelines for Prevention of Sexual Transmission of Zika Virus — United States, 2016, MMWR. Morbidity and Mortality Weekly Report 65, 2016 doi: 10.15585/mmwr.mm6505e1er
- ^ CDC Press Releases, CDC, 2016-01-01 (באנגלית)
- ^ Susan L. Hills, Transmission of Zika Virus Through Sexual Contact with Travelers to Areas of Ongoing Transmission — Continental United States, 2016, MMWR. Morbidity and Mortality Weekly Report 65, 2016 doi: 10.15585/mmwr.mm6508e2er
- ^ Jean Michel Mansuy, Marine Dutertre, Catherine Mengelle, Camille Fourcade, Bruno Marchou, Pierre Delobel, Jacques Izopet, Guillaume Martin-Blondel, Zika virus: high infectious viral load in semen, a new sexually transmitted pathogen?, The Lancet Infectious Diseases 16, 2016-04-01, עמ' 405 doi: 10.1016/S1473-3099(16)00138-9
- ^ Emily E. Petersen, Update: Interim Guidance for Health Care Providers Caring for Women of Reproductive Age with Possible Zika Virus Exposure — United States, 2016, MMWR. Morbidity and Mortality Weekly Report 65, 2016 doi: 10.15585/mmwr.mm6512e2er
- ^ התפרצות מחלת נגיף הזיקה - חוזר משרד הבריאות – ויקירפואה, באתר www.wikirefua.org.il
- ^ 1 2 3 4 5 Derek Gatherer, Alain Kohl, Zika virus: a previously slow pandemic spreads rapidly through the Americas, Journal of General Virology 97, 2016, עמ' 269–273 doi: 10.1099/jgv.0.000381
- ^ Myrielle Dupont-Rouzeyrol, Antoine Biron, Olivia O'Connor, Emilie Huguon, Elodie Descloux, Infectious Zika viral particles in breastmilk, The Lancet 387, 2016-03-12, עמ' 1051 doi: 10.1016/S0140-6736(16)00624-3
- ^ Irina Burd, Sabra Klein, Andrew Pekosz, Jun Lei, Pathogenesis and Molecular Mechanisms of Zika Virus, Seminars in Reproductive Medicine 34, 2016/09, עמ' 266–272 doi: 10.1055/s-0036-1592071
- ^ Joern Bullerdiek, Andreas Dotzauer, Ingrid Bauer, The mitotic spindle: linking teratogenic effects of Zika virus with human genetics?, Molecular Cytogenetics 9, 2016-04-19 doi: 10.1186/s13039-016-0240-1
- ^ Rong Hai, Kingyung Hui, Leonel Islas, Stephanie Thurmond, Zika virus genome biology and molecular pathogenesis, Emerging Microbes & Infections 6, 2017-03, עמ' e13 doi: 10.1038/emi.2016.141
- ^ Veronica Sikka, Vijay Kumar Chattu, Raaj K Popli, Sagar C Galwankar, The Emergence of Zika Virus as a Global Health Security Threat: A Review and a Consensus Statement of the INDUSEM Joint working Group (JWG), Journal of Global Infectious Diseases 8, 2016, עמ' 3–15 doi: 10.4103/0974-777X.176140
- ^ Anthony S. Fauci, David M. Morens, Zika Virus in the Americas — Yet Another Arbovirus Threat, https://doi.org/10.1056/NEJMp1600297, 2016-02-17 (באנגלית)
- ^ 1 2 Benjamin A. Pinsky, Jesse J. Waggoner, Zika Virus: Diagnostics for an Emerging Pandemic Threat, Journal of Clinical Microbiology 54, 2016-04-01, עמ' 860–867 doi: 10.1128/JCM.00279-16
- ^ 1 2 Titilope Oduyebo, Update: Interim Guidelines for Health Care Providers Caring for Pregnant Women and Women of Reproductive Age with Possible Zika Virus Exposure — United States, 2016, MMWR. Morbidity and Mortality Weekly Report 65, 2016 doi: 10.15585/mmwr.mm6505e2er
- ^ 1 2 3 4 Kate Russell, Update: Interim Guidance for the Evaluation and Management of Infants with Possible Congenital Zika Virus Infection — United States, August 2016, MMWR. Morbidity and Mortality Weekly Report 65, 2016 doi: 10.15585/mmwr.mm6533e2
- ^ Mariana C. Leal, Hearing Loss in Infants with Microcephaly and Evidence of Congenital Zika Virus Infection — Brazil, November 2015–May 2016, MMWR. Morbidity and Mortality Weekly Report 65, 2016 doi: 10.15585/mmwr.mm6534e3
- ^ Avoid bug bites | Travelers' Health | CDC, wwwnc.cdc.gov
- ^ CDC Issues Zika Travel Alert, Medscape
- ^ CDC, Pregnant Women and Zika Virus | CDC, Centers for Disease Control and Prevention, 2018-11-16 (באנגלית)
- ^ טבלה 1: אזורים ומדינות עם סיכון להעברה מקומית של נגיף הזיקה, באתר משרד הבריאות
- ^ WHO Declares Zika a Public Health Emergency, NBC News (באנגלית)
- ^ Tavernise, Sabrina; Jr, Donald G. McNeil (2016-02-01). "Zika Virus a Global Health Emergency, W.H.O. Says". The New York Times (באנגלית אמריקאית). ISSN 0362-4331. נבדק ב-2018-12-29.
- ^ CNN, Debra Goldschmidt,. "WHO ends Zika public health emergency". CNN. נבדק ב-2018-12-29.
{{cite news}}: תחזוקה - ציטוט: extra punctuation (link) - ^ 1 2 ClinicalKey, www.clinicalkey.com
- ^ Zika virus infection, European Centre for Disease Prevention and Control (באנגלית)
- ^ 1 2 Veronica Sikka, Vijay Kumar Chattu, Raaj K Popli, Sagar C Galwankar, The Emergence of Zika Virus as a Global Health Security Threat: A Review and a Consensus Statement of the INDUSEM Joint working Group (JWG), Journal of Global Infectious Diseases 8, 2016, עמ' 3–15 doi: 10.4103/0974-777X.176140
- ^ Emily E. Petersen, Interim Guidelines for Pregnant Women During a Zika Virus Outbreak — United States, 2016, MMWR. Morbidity and Mortality Weekly Report 65, 2016 doi: 10.15585/mmwr.mm6502e1
- ^ 1 2 Duane J. Gubler, Didier Musso, Zika Virus, Clinical Microbiology Reviews 29, 2016-07-01, עמ' 487–524 doi: 10.1128/CMR.00072-15
- ^ F. N. MacNamara, Zika virus : A report on three cases of human infection during an epidemic of jaundice in Nigeria, Transactions of The Royal Society of Tropical Medicine and Hygiene 48, 1954-03-01, עמ' 139–145 doi: 10.1016/0035-9203(54)90006-1
- ^ D. I. H. Simpson, Zika virus infection in man, Transactions of The Royal Society of Tropical Medicine and Hygiene 58, 1964-07-01, עמ' 335–337 doi: 10.1016/0035-9203(64)90201-9
- ^ K. C. Smithburn, J. A. Kerr, P. B. Gatne, Neutralizing antibodies against certain viruses in the sera of residents of India, Journal of Immunology (Baltimore, Md.: 1950) 72, 1954-4, עמ' 248–257
- ^ Triwibowo, Suhandiman, T. G. Ksiazek, J. G. Olson, Zika virus, a cause of fever in Central Java, Indonesia, Transactions of The Royal Society of Tropical Medicine and Hygiene 75, 1981-01-01, עמ' 389–393 doi: 10.1016/0035-9203(81)90100-0
- ^ Lyle R. Petersen, Denise J. Jamieson, Ann M. Powers, Margaret A. Honein, Zika Virus, https://doi.org/10.1056/NEJMra1602113, 2016-03-30 (באנגלית)
- ^ Mark R. Duffy, Tai-Ho Chen, W. Thane Hancock, Ann M. Powers, Zika Virus Outbreak on Yap Island, Federated States of Micronesia, New England Journal of Medicine 360, 2009-06-11, עמ' 2536–2543 doi: 10.1056/NEJMoa0805715
- ^ 1 2 3 Y. Souarès, L. Guillaumot, E. Benyon, S. Duituturaga, Concurrent outbreaks of dengue, chikungunya and Zika virus infections – an unprecedented epidemic wave of mosquito-borne viruses in the Pacific 2012–2014, Eurosurveillance 19, 2014-10-16, עמ' 20929 doi: 10.2807/1560-7917.ES2014.19.41.20929
- ^ J. Broult, V. M. Cao-Lormeau, A. Shan Yan, K. Zisou, Potential for Zika virus transmission through blood transfusion demonstrated during an outbreak in French Polynesia, November 2013 to February 2014, Eurosurveillance 19, 2014-04-10, עמ' 20761 doi: 10.2807/1560-7917.ES2014.19.14.20761
- ^ "Mainland Chile confirms first three cases of Zika virus". Reuters (באנגלית). 2016-02-03. נבדק ב-2018-12-29.
- ^ Nuno Rodrigues Faria, Raimunda do Socorro da Silva Azevedo, Moritz U.G. Kraemer, Renato Souza, Zika virus in the Americas: Early epidemiological and genetic findings, Science (New York, N.Y.) 352, 2016-04-15, עמ' 345–349 doi: 10.1126/science.aaf5036
- ^ Owen Dyer, Zika virus spreads across Americas as concerns mount over birth defects, BMJ 351, 2015-12-23, עמ' h6983 doi: 10.1136/bmj.h6983
- ^ Lena H. Sun, First Zika virus-related death reported in U.S. in Puerto Rico, The Washington Post, April 29, 2016
- ^ Luciana AmaralDo G1, em Brasília, Ministério da Saúde confirma 8 casos de zika vírus no RN e 8 na BA, Bem Estar, 2015-05-14 (בפורטוגזית)
- ^ J. Schmidt-Chanasit, A. Bartoloni, G. Venturi, S. Günther, Zika virus infection in a traveller returning to Europe from Brazil, March 2015, Eurosurveillance 20, 2015-06-11, עמ' 21153 doi: 10.2807/1560-7917.ES2015.20.23.21153
- ^ Governo confirma relação entre zika vírus e epidemia de microcefalia, BBC News Brasil (בפורטוגזית)
- ^ "Brazil confirms zica virus link to fetal brain-damage outbreak". Reuters (באנגלית). 2015-11-28. נבדק ב-2018-12-29.
- ^ País registra 1.248 casos de microcefalia e sete mortes; maioria em PE, noticias.uol.com.br (בפורטוגזית)
- ^ 1 2 Zika virus epidemic in the Americas: potential association with microcephaly and Guillain-Barré syndrome, ecdc.europa.eu
- ^ Simon Cauchemez, Marianne Besnard, Priscillia Bompard, Timothée Dub, Association between Zika virus and microcephaly in French Polynesia, 2013–2015: a retrospective study, Lancet (London, England) 387, 2016-05-21, עמ' 2125–2132 doi: 10.1016/S0140-6736(16)00651-6
- ^ Zika cases and congenital syndrome associated with Zika virus (קובץ אקסל להורדה), באתר www.paho.org
- ^ Reuters (2016-06-02). "USA cyclist Tejay van Garderen withdraws from Olympics over Zika virus". The Guardian (באנגלית בריטית). ISSN 0261-3077. נבדק ב-2018-12-28.
- ^ World Health Organization: Athletes should not fear Zika virus at Rio Olympics, USA TODAY (באנגלית)
- ^ ClinicalKey, www.clinicalkey.com
- ^ Adriano de Bernardi Schneider, Robert W. Malone, Jun-Tao Guo, Jane Homan, Molecular evolution of Zika virus as it crossed the Pacific to the Americas, Cladistics 33, 2017, עמ' 1–20 doi: 10.1111/cla.12178
- ^ Raymond TP Lin, Lin Cui, Raphael TC Lee, Daniel A. Holdbrook, South-east Asian Zika virus strain linked to cluster of cases in Singapore, August 2016, Eurosurveillance 21, 2016-09-22, עמ' 30347 doi: 10.2807/1560-7917.ES.2016.21.38.30347
- ^ Dale Fisher, Jeffery Cutter, The inevitable colonisation of Singapore by Zika virus, BMC Medicine 14, 2016-11-21 doi: 10.1186/s12916-016-0737-9
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.
