תרופה – הבדלי גרסאות
מ ←פיתוח וייצור תרופות: הגהה, replaced: שינוים ← שינויים באמצעות AWB |
Matanyabot (שיחה | תרומות) מ בוט החלפות: לעיתים |
||
| שורה 92: | שורה 92: | ||
לדוגמה, מתן [[אנטיביוטיקה]] בצורה של טיפות או משחה (כגון [[כלוראמפניקול]]) לדלקת בעיניים. |
לדוגמה, מתן [[אנטיביוטיקה]] בצורה של טיפות או משחה (כגון [[כלוראמפניקול]]) לדלקת בעיניים. |
||
===== מתן לאוזניים ===== |
===== מתן לאוזניים ===== |
||
בצורה של טיפות לאוזניים |
בצורה של טיפות לאוזניים ולעיתים גם בצורה של תרסיס או אבקה לאוזניים. |
||
===== מתן לאף ===== |
===== מתן לאף ===== |
||
| שורה 247: | שורה 247: | ||
מרבית ה[[תרכובת אורגנית|תרכובות האורגניות]] המשמשות כתרופות, יוצרו '''באופן סינתטי''' (מלאכותי) במעבדה הכימית. אולם, חלק מהתרופות עשויות להתקבל בתהליכים '''חצי-סינתטיים''' (מלאכותיים למחצה), כלומר ביצוע של עיבוד כימי לחומרי טבע שהתקבלו בתהליכי [[מיצוי]], [[זיקוק]] והפרדה. |
מרבית ה[[תרכובת אורגנית|תרכובות האורגניות]] המשמשות כתרופות, יוצרו '''באופן סינתטי''' (מלאכותי) במעבדה הכימית. אולם, חלק מהתרופות עשויות להתקבל בתהליכים '''חצי-סינתטיים''' (מלאכותיים למחצה), כלומר ביצוע של עיבוד כימי לחומרי טבע שהתקבלו בתהליכי [[מיצוי]], [[זיקוק]] והפרדה. |
||
לעיתים קרובות, הייצור של ה[[תרכובת אורגנית|תרכובות האורגניות]] נעשה בשיטות [[ביוטכנולוגיה|ביוטכנולוגיות]], כלומר במקום ייצור כימי ישיר של התרופה על ידי [[סינתזה אורגנית]] קלאסית, נעשה שימוש ביצרנים ביולוגים כגון [[פטריות]] או [[חיידקים]] לייצור של התרכובות הרצויות (ראו [[ביוסינתזה]], [[ביוטכנולוגיה]]). |
|||
דוגמאות לתרופות המבוססות על [[תרכובת אורגנית|תרכובות אורגניות]]: |
דוגמאות לתרופות המבוססות על [[תרכובת אורגנית|תרכובות אורגניות]]: |
||
| שורה 303: | שורה 303: | ||
# [[ניסוי קליני|ניסויים קליניים]] - ווידוא האפקט הפרמקולוגי בבני אדם ובדיקה שהתרופה אינה מסוכנת למשתמשים בה. ניסויים קליניים חייבים להיעשות על ידי רופא ובפיקוח ועדה ממשלתית ([[ועדת הלסינקי]]). הניסוי הקליני נעשה בדרך כלל בשלושה שלבים. |
# [[ניסוי קליני|ניסויים קליניים]] - ווידוא האפקט הפרמקולוגי בבני אדם ובדיקה שהתרופה אינה מסוכנת למשתמשים בה. ניסויים קליניים חייבים להיעשות על ידי רופא ובפיקוח ועדה ממשלתית ([[ועדת הלסינקי]]). הניסוי הקליני נעשה בדרך כלל בשלושה שלבים. |
||
# בדיקה לאחר מתן האישור לתרופה - גם תרופות שכבר אושרו מתגלות כמסוכנות לפעמים היות שאוכלוסיית המחקר מוגבלת בכמותה. |
# בדיקה לאחר מתן האישור לתרופה - גם תרופות שכבר אושרו מתגלות כמסוכנות לפעמים היות שאוכלוסיית המחקר מוגבלת בכמותה. |
||
בתעשיית התרופות ידועות מולקולות [[כיראליות (כימיה)|כיראליות]] שונות, שרק גרסה אחת שלהן מבצעת את פעולת הריפוי, ואילו הגרסה השנייה אינה מועילה, |
בתעשיית התרופות ידועות מולקולות [[כיראליות (כימיה)|כיראליות]] שונות, שרק גרסה אחת שלהן מבצעת את פעולת הריפוי, ואילו הגרסה השנייה אינה מועילה, ולעיתים אפילו מזיקה. כדוגמה ניתן לציין את ה[[תלידומיד]] ש[[אננטיומר]] אחד שלו מקל על בחילות בוקר של נשים בהריון, ואילו לאננטיומר השני יש אפקט [[טרטוגן|טרטוגני]], כלומר פוגע בהתפתחות העובר. תרופה זו שניתנה לנשים בהריון ב[[שנות השישים]] של [[המאה ה-20]] הביאה ללידת תינוקות חסרי גפיים. בארצות-הברית, הטרגדיה נמנעה משום שהתרופה לא אושרה לשימוש. הידע שהצטבר בתחום ה[[סטריאוכימיה]] מאפשר כיום לייצר תרופות בתגובות [[סטריאוסלקטיביות]], כלומר כאלו שנוצר בהן עודף משמעותי של אחד ה[[איזומר|סטריאואיזומרים]]. |
||
בעולם שני גופים מרכזיים העוסקים באישור תרופות - ה[[FDA]] האמריקאי וה-[[EDMA]] האירופי. בנוסף נערכים מבחנים קליניים לשם אישור תרופות ב[[יפן]] ובהיקף קטן יותר ב[[קוריאה הדרומית]]. לגבי אירופה יש הסדר מיוחד המאפשר לעקוף את ה-EDMA לאישור תרופה על ידי משרדי הבריאות הלאומיים (הרבה חברות תרופות נוטות לרשום תרופות ב[[דנמרק]] בזכות חוקיה הפשוטים יחסית). |
בעולם שני גופים מרכזיים העוסקים באישור תרופות - ה[[FDA]] האמריקאי וה-[[EDMA]] האירופי. בנוסף נערכים מבחנים קליניים לשם אישור תרופות ב[[יפן]] ובהיקף קטן יותר ב[[קוריאה הדרומית]]. לגבי אירופה יש הסדר מיוחד המאפשר לעקוף את ה-EDMA לאישור תרופה על ידי משרדי הבריאות הלאומיים (הרבה חברות תרופות נוטות לרשום תרופות ב[[דנמרק]] בזכות חוקיה הפשוטים יחסית). |
||
גרסה מ־02:16, 2 בינואר 2018


תרופה (באנגלית: Pharmaceutical Drug או בקיצור Drug או Medication; שמות נרדפים בעברית: תכשיר רפואי, מיושנים: רפואה, סם מרפא) היא חומר כימי או ביולוגי פעיל, בודד או כחלק מתערובת של חומרים, המשמש לטיפול, ריפוי, מניעה של מחלות.
בעבר הרחוק, התרופות היו ממקור טבעי בלבד, אבל התקדמות התעשייה הכימית ומדעי הכימיה, הביאו לעולם חומרים פעילים כימיים בעלי פעילות פרמקולוגית ניכרת. לקראת סוף המאה ה-20, בשל התקדמות מדעי הביוטכנולוגיה, נוספו לשוק גם תרופות ביולוגיות, שהם חלבונים בעלי מבנים גדולים ומסובכים ומשמשים כתרופה. מאחר שבמקרים רבים, התרופה מכילה כמות מינון מזערית, בתהליך הייצור שלה מוסיפים לה רכיבים שאינם פעילים וזאת בהתאם לצורה שבה היא נרקחת (לדוגמה, סירופים יכילו חומר ממתיק או משפר טעם כלשהו, טבליות יכילו חומר נותן נפח כגון לקטוז ומרכיבים נוספים שיעזרו לייצר את הכדור בתנאי מפעל וכיוצא בזה).
מדעי הפרמקולוגיה הם תחום במדעי הטבע והכימיה שעוסקים בתחום התרופות, איך תרופות פועלות בגוף, על אילו איברי מטרה הן פועלות, אילו תופעות לוואי צפויות מהתרופה ואיך הגוף מתייחס לתרופה (במונחים של כיצד התרופה נספגת ומהם המנגנונים הקיימים בגוף שקשורים בפירוק התרופה והפרשתה מהגוף).
היסטוריה
משחר האנושות האדם חיפש מזור למכאוביו ומחלותיו, ובתחילה הוא עשה זאת תוך הסתכלות על סביבתו וחיפוש אחר גורמים בסביבה (כגון צמחים ובעלי חיים) שיתרמו לבריאותו. לפיכך בתחילת דרכה של הרפואה, תרופות הורכבו בעיקר מצמחים או מבעלי חיים. כאשר קוראים כתבי רפואה עתיקים, ניתן לראות התייחסות שונה לרפואה ולריפוי, כאשר בחלק מהמקרים נקשרו גורמים מיסטיים לעולם הצמחים המשמשים ברפואה. בעבר הייתה גם חפיפה בין אלכימיה לרפואה ולרוקחות.
לאורך ההיסטוריה, התרופות עברו גלגולים שונים ויוצרו בשיטות שונות לחלוטין ובצורות רקיחה שונות. לעולם העתיק היו ידועות רק מספר בודד של צורות רקיחה, כגון תרופות הניתנות בזריקה, בנוזל לבליעה, בנוזל חיצוני והיה גם נפוץ שימוש באבקות. במאה השנים האחרונות, תחום הפרמקולוגיה והרוקחות עבר שינוי משמעותי עם הופעת תרופות בייצור מסחרי, ובעקבותיו נוצרו צורות רקיחה שלא היו מוכרות לעולם העתיק (כגון טבליות, משאפים, מדבקות וכיוצא בזה).
עם התקדמות המדעים, חל מפנה גם בהתייחסות לתרופות ובחיפוש אחר רפואה מבוססת ראיות, שבה השפעות של תרופות נבדקות במחקרים קליניים המאפשרים איכות טיפולית ותרופות שמוכחות כיעילות, נטולות אפקט פלצבו ואפקטים אחרים שמשפיעים פסיכולוגית על מטופלים בנטילת תרופות.
הגדרות
על פי משרד הבריאות בישראל[1], הגדרת המונח "סמי מרפא" על פי פקודת הרוקחים (נוסח חדש 1981) היא:
- "מוצר כימי, תכשיר רוקחות, תרופה, תרכיב, נסיוב וכל מצרך או חומר אחרים לשימוש ברפואה".
באירופה[2], ההגדרה של התרופה היא:
- כל חומר או שילוב של חומרים שיש להם תכונות לטיפול או מניעת מחלות בבני אדם
- כל חומר או שילוב חומרים שניתן להשתמש בו או בם וניתן לתת אותם לבני אדם כדי לתקן או לשנות תפקוד פיזיולוגי בגוף באמצעות פעילות פרמקולוגית, אימונולוגית או מטאבולית או כדי לאבחן מחלות.
בארצות הברית[3], ההגדרה של תרופה היא:
- חומר שמוכר על ידי פרמקופיאה רשמית
- חומר המיועד לאבחון, ריפוי, הקלה, טיפול או מניעת מחלה
- חומר (שאיננו מזון) שמכוון להשפיע על המבנה או התפקוד של הגוף
- חומר שמשמש כמרכיב ברפואה אך הוא איננו התקן או איננו חלק מהתקן
- חומרים ביולוגיים כלולים בהגדרה זאת והם בדרך כלל נמצאים תחת אותו פיקוח חוקי, אבל יש שינויים בייצור שלהם בהשוואה לתרופות המיוצרות בתהליכים כימיים.
מאפיינים
לחומר הפעיל של התרופה יש מאפיינים ייחודיים המבדילים אותו מחומרים אחרים בגוף החי.
ראשית, תרופה מכילה חומר שנוצר מחוץ לגוף (exogenous). לכן חומרים הנוצרים בתוך הגוף (כמו הורמונים או מוליכים עצביים) אינם נחשבים במרבית המקרים לתרופה (להוציא מקרים ספציפיים כגון מתן הורמון בלוטת התריס במטופלים שסובלים מתת פעילות בלוטת התריס ומתן אינסולין למטופלים עם סוכרת). עם זאת, חומרים סינתטיים המחקים את הפעולה של חומרים הנוצרים בגוף כן נחשבים לתרופה.
להבדיל מרעלים שיכולים לגרום לנזק ולמוות למי שנוטל אותם, תרופה איננה נחשבת מסוכנת כל עוד היא ניטלת במינונים מתאימים. נטילה תרופה מעל המינון המומלץ שלה עלול לגרום להשפעה טוקסית ובכך לגרום לתופעות לוואי קשות ובמקרים קיצוניים אף למוות.
ניתן למיין תרופות במספר דרכים, ובין היתר ניתן למיינן על פי המבנה הכימי (או הביולוגי) שלהן, על פי השתייכותן למשפחה פרמקולוגית כלשהי, על פי אזור פעולתה בגוף, על פי ההתוויה שלשמה היא ניתנת וכו'. לדוגמה: מתילפנידאט היא תרופה שהמבנה הכימי שלה הוא פנתילאמין, היא שייכת לקבוצת התרופות המכונות מגרות (סטימולנטיות) מערכת העצבים המרכזית, היא פועלת על מערכת העצבים המרכזית וניתנת לטיפול בהפרעות קשב ובנרקולפסיה.
פעילות
פרמקודינמיקה היא מונח המתייחס לפעילות של תרופה בגוף. המושג פעילות התרופה מתייחס לשינויים הפזיולוגיים שחלים בעקבות השימוש בתרופה. לתרופה ישנה פעילות פרמקולוגית מוכחת, אשר אמורה להיטיב עם המטופל כל עוד היא ניתנת במינונים המומלצים שלה. פעילות לא רצויה של תרופה מוגדרת כתופעת לוואי.
מרבית התרופות יוצרות את הפעילות שלהן על ידי אינטראקציה עם קולטן/ים שנמצאים או על קרום התא או בתוך התא. יצירת הקומפלקס שבו תרופה נצמדת לקולטן גורמת לשינויים ביוכימיים או מולקולריים בתוך התא וגורמת לשינויים פיזיולוגיים[4].
אזור או איבר המטרה הוא האיבר שבו התרופה אמורה לפעול, ויש תרופות שיש להן יותר מאיבר מטרה אחד. לדוגמה משתנים מסוג תיאזידים פועלים על הכליה וגורמים לפעולה משתנת (איבר המטרה הוא האבובית המפותלת המרוחקת של הנפרון, שהוא היחידה הפועלת של הכליה) אבל הם גם מורידים לחץ דם על ידי הפחתת תנגודת היקפית ולפיכן הם גם פועלים על כלי הדם.
תרופות יכולות לחקות פעילות פיזיולוגית בגוף (לדוגמה מתן אינסולין עוזר לטיפול במחלת הסוכרת) או לנגוד או לבטל או לשנות פעילות פיזיולוגית בגוף (לדוגמה חוסמי תעלות סידן חוסמים תעלות סידן ומונעים מסידן להיצמד לתעלות ולהוציא את פעולתו הפיזיולוגית).
במרבית המקרים, החומר הפעיל של התרופה לא נשאר בגוף באופן קבוע. עם הזמן הוא מופרש מהגוף (בשתן, במרה או בצואה) או הופך לחלקים פעילים ולא פעילים שמופרשים גם מהגוף. האופן בו הגוף מתמודד עם התרופה מכונה פרמקוקינטיקה.
שימוש בטוח בתרופות
לתרופות יש פעילות פרמקולוגית תקינה כל עוד הן ניטלות במינונים המומלצים המקובלים ואינן ניטלות בעודף. במינונים גבוהים מהמותר, מופיעות תופעות טוקסיות של התרופה ועלול להיגרם נזק למטופל או מוות.
תופעות לוואי עלולות להתרחש גם כאשר התרופה ניתנת במינונים הרגילים שלה ולאו דווקא במינונים רעילים שלה. יש חשיבות במעקב אחרי תופעות לוואי של תרופות והדרכת מטופלים להכרת תופעות הלוואי של הטיפול התרופתי שלהם.
חשוב גם לעקוב אחרי פרמטרים נוספים שיכולים לגרום לרעילות כתוצאה מתרופות, כגון מצבי מחלה שונים (למשל הפרעות בתפקוד הכלייתי או הכבדי עלולות לגרום להצטברות תרופות בגוף), מאפיינים של המטופלים (כגון גיל, מין, מצב תזונתי, שייכות אתנית ומאפיינים גנטיים) ותגובות בין תרופתיות.
דרכי מתן תרופות
כדי שהתרופה תהיה יעילה עליה להגיע לאזור שעליו היא נועדה להשפיע. תרופות ניתנות בדרכים רבות, אשר ניתן לסווג לשני סוגים עיקריים - מתן מקומי ומתן סיסטמי (מערכתי).
מתן מקומי
זהו מתן התרופה ישירות לאזור המטרה של התרופה. מתן זה מתאפיין בפחות תופעות לוואי בהשוואה למתן סיסטמי של התרופה וזאת בזכות הפיזור המוגבל של התרופה בגוף והבאת התרופה לאיבר המטרה שלה מבלי הצורך לעבור במדורים אחרים ולהתפזר באיברים שונים.
מתן טופיקלי
מתן טופיקלי הוא מתן הכרוך בשימוש חיצוני של התרופה, כלומר על העור ועל ממברנות חיצוניות (כולל העיניים, רקמות האף, האוזניים וחלל הפה, הלשון והחניכיים).
מתן טופיקלי: מריחה על העור

מרבית התרופות שניתנות במתן טופיקלי הן תרופות המיועדות למריחה על העור. תרופות אלו מגיעות בצורות שונות, כולל:
- משחה
- קרם
- ג'ל
- תמיסות לשימוש חיצוני (Solution)
- תרחיפים ותחליבים לשימוש חיצוני (Emulsion)
- תרחיצים לשימוש חיצוני (Lotion)
- שמפו
- מדבקות
- אבקות (כגון אבקת אונדציל לטיפול בשפשפת ופטרת כף הרגל
- תרסיסים לשימוש חיצוני
- קצף לשימוש חיצוני
מתן זה מאפשר את הגעת התרופה ישר לאבר המטרה (העור) ולכן הוא מתאים במצבים דרמטולוגיים, מחלות בעור, אבחון של מחלות בעור (בדיקות אלרגיה) וטיפולים קוסמטיים.
חשוב לציין שקיימות מדבקות המכילות חומרים פעילים לשימוש על העור. כל עוד שהמדבקות הללו מיועדות לשימוש על העור ולטיפול או אבחון של בעיה בעור הן נחשבות למתן טופיקלי. יחד עם זאת, קיימות מדבקות הניתנות באופן טרנסדרמלי והן מכילות תרופות שמגיעות למחזור הדם דרך העור. מתן זה איננו נחשב לטופיקלי כי אם סיסטמי בשל השפעה סיסטמית של התרופה על ידי הגעתה למחזור הדם.
מתן לעיניים


מתן לעיניים יכול להיות בצורה של טיפות, ג'ל או משחה למתן תוך עיני או באזור העיניים והעפעפיים.
לדוגמה, מתן אנטיביוטיקה בצורה של טיפות או משחה (כגון כלוראמפניקול) לדלקת בעיניים.
מתן לאוזניים
בצורה של טיפות לאוזניים ולעיתים גם בצורה של תרסיס או אבקה לאוזניים.
מתן לאף

מתן לאף מאפשר טיפול במצבים הקשורים למערכת הנשימה והאף, כגון נזלת, גוש באף או יובש באף.
דרך הממברנה של האף, קיימות גם תרופות שיכולות להיספג למערכת הדם ולכן קיימים גם תכשירים המיועדים לשימוש באף, אך אלו הם תכשירים סיסטמיים. דוגמאות: אינסולין הניתן בתרסיס לאף, חיסון נגד שפעת והתרופה מינירין, שמשמשת לטיפול בסוכרת תפלה.
מתן לחלל הפה

מתן לחלל הפה מיועד לטפל במחלות ומצבים רפואיים בחלל הפה, הלשון, החניכיים והגרון.
דוגמאות לתרופות הניתנות במתן זה כוללות:
- שטיפות פה
- ג'ל למריחה על הלשון או החניכיים
- פסטה למריחה על השיניים או החניכיים
- משחה לטיפול בדלקת חניכיים
- משחת שיניים המכילה חומרים פעילים ו
- כדורים וסוכריות למציצה להקלה על כאבי גרון
מתן רקטאלי

מתן רקטאלי נעשה באמצעות החדרת:
התכשירים הללו נועדו לשימוש מקומי בפי הטבעת או בחלחולת. במצבים הקשורים למחלה באזורים אלו, כגון טחורים, עצירות, פיסורה, מחלת מעי דלקתית.
דוגמאות: מתן פתילות וחוקני רפאסל לטיפול במחלת מעי דלקתית, מתן של חוקנים לפני לידה או לפני תהליכים רפואיים, מתן ג'ל ניפדיפין לטיפול בפיסורה בחלחולת.
מתן רקטאלי יכול להיות גם מתן סיסטמי, משום שיש תרופות שנספגות דרך החלחולת, לדוגמה פתילות המכילות פאראצרטאמול או איבופרופן לטיפול בחום ובכאבים. התרופות הללו ניתנות דרך הרקטום אבל ההשפעה ואזור המטרה הוא סיסטמי ואיננו קשור לרקטום.
מתן וגינלי
מתן וגינלי נעשה באמצעות החדרת פתילות, משחות וטבליות לנרתיק ומיועד לטפל במחלות ומצבים רפואיים הקשורים בנרתיק.
דוגמאות מתן טבליות וגינליות של אגיסטן לטיפול בפטרת הנרתיק, מתן של קרם דלאצין לטיפול בזיהום חיידקי בנרתיק, מתן של ג'ל או קרם לטיפול ביובש בנרתיק וכו'.
מתן בשאיפה



מתן בשאיפה (אינהלציה) לריאות, נועד להביא את התרופה לאיבר המטרה שהוא הריאות, במצבים של מחלות ריאה (כגון אסתמה, מחלת ריאות חסימתית כרונית וסיסטיק פיברוזיס) או מצבים רפואיים הקשורים בקוצר נשימה.
דוגמאות: מתן משאף בצורה של תרסיסים, משאף המכילים אבקה יבשה ותמיסות לאינהלציה לשימוש במכשיר אינהלציה.
תרופות הניתנות במתן זה כוללות תרופות ממשפחת מרחיבי הסימפונות כגון ונטולין או אנטיביוטיקות שניתנות בשאיפה לטיפול בזיהומים ריאתיים על רקע סיסטיק פיברוזיס.
תרופות הניתנות לריאות עוברות גם דרך חלל הפה, ולכן הן גם עלולות להיספג (באחוזים נמוכים עד מזעריים) ולגרום להשפעות סיסטמיות. כמו כן הן גם נשארות בחלל הפה ועלולות לגרום לתופעות לוואי בחלל הפה (כגון יובש, צרידות ופטרת) ולכן מומלץ לשטוף את הפה לאחר השימוש במשאפים ובתכשירי אינהלציה.
מתן סיסטמי
באמצעות מתן תרופה סיסטמי החומר הפעיל מגיע אל מחזור הדם ודרכה מתפזר בגוף. קיימות מספר דרכים למתן סיסטמי, כאשר הנפוצות בהן הן הדרך האנטרלית (מתן פומי, דרך מערכת העיכול) והדרך הפראנטרלית (ישירות למחזור הדם). דרכים נוספות כוללות שימוש בתרסיסי אף, מדבקות טרנסדרמליות וג'ל או קרם שמורחים על העור אבל התרופה נספגת דרך העור אל מחזור הדם.
מתן פומי
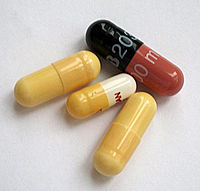


ישנן מספר דרכים אנטרליות למתן תרופה דרך המעיים מערכת העיכול:
- מתן פומי (אוראלי, כלומר דרך הפה בבליעה) כולל מתן של טבליות, קפליות, קפסולות, סירופים, תרחיפים, טנקטורות, סוכריות מציצה ועוד. מתן פומי היא הדרך הנוחה, הקלה והנפוצה ביותר. מחקרים רבים נעשים כדי למצוא דרך למתן פומי עבור תרופות שכיום ניתן לתת רק בהזרקה (ראו כלל החמישה של ליפינסקי).
- צינור האכלה קיבתי או תריסריוני, או גסטרוטומיה (פתיחת הבטן). דרך מתן זו מיועדת בעיקר להאכלה במקרים שהאדם אינו מסוגל לאכול בעצמו לאורך זמן. מבחינה פרמקולוגית היא דומה למתן פומי.
- רקטלית (דרך החלחולת), של פתילה הנספגת על ידי המעי הגס למתן סיסטמי של תרופה. משתמשים במתן רקטאלי במקום במתן פומי בעיקר בשני מקרים, כאשר האדם אינו מסוגל לבלוע או כדי לעקוף את הפירוק הראשוני של התרופה על ידי הכבד: תרופות הנספגות למחזור הדם מהמעי הגס אינן עוברות פרוק ראשוני בכבד לעומת שאר מערכת העיכול למעט הפה.
דרך פראנטרלית


ישנם מספר דרכים פראנטרליות למתן תרופה שלא דרך המעיים. חלקן מחדירות את התרופה באופן ישיר למערכת הדם וחלקן מחדירות את התרופה באופן עקיף שאינו מערב את מערכת העיכול.
שלושת השיטות הפראנטרליות הנפוצות ביותר הן:
- תוך ורידית (IV, intravenous), מתן רוב התרופות בהזרקה או באינפוזיה. בהזרקה תוך ורידית החומר הפעיל מוחדר למחזור הדם באופן מיידי ומופץ ברחבי הגוף בתוך שניות מעטות בלבד. באופן זה המינון המלא מגיע למחזור הדם בבת-אחת והזמינות הביולוגית היא 100%.
- תוך שרירית (IM, intramuscular), לדוגמה מתן חיסונים ותרופות דרך השריר. דרך מתן זאת היא בדרך כלל כואבת ולא נעימה. ניתן לצמצם את הכאב על ידי הזרקה של נפח תמיסה נמוך. ניתן לתת בדרך זאת גם זריקות המכונות "Depot" שבהן החומר המוזרק לשריר משתחרר בריכוזים קבועים נמוכים ולאורך זמן (שבועיים ועד ארבעה שבועות) ומאפשר הענות לטיפול רפואי, במיוחד במקרים של תרופות נוגדות פסיכוזה לטיפול בסכיזופרניה.
- תת-עורית (SC, subcutaneous) למשל מתן אינסולין ומתן של נגזרות בעלות משקל מולקולרי של הפרין לטיפול ומניעת קרישי דם.
שיטות פראנטרליות נוספות כוללות:
- בזריקות:
- תוך עורית (intradermal), לבדיקות עור על ידי אלרגנים מסוימים.
- תוך עורקית, לדוגמה מתן מרחיבי כלי דם לטיפול בהתכווצות כלי דם.
- תוך לבבית (אל תוך הלב), לדוגמה מתן אדרנלין כחלק מהחייאה (לא נפוץ בשימוש כיום)
- אל מח העצם.
- אל תעלת השדרה (אפידורלית), בשימוש להרדמת עמוד השדרה ומתן כימותרפיה.
- תוך צפקית (אל תוך הצפק, או קרום הבטן).
- תוך מפרקית (intra-articular) מתן המאפשר מתן תרופה לתוך מפרק "חולה" ומאפשר הגעת התרופה לאיבר המטרה וצמצום פיזור סיסטמי. אפשר לראות בדרך מתן זאת גם סוג של מתן טופיקלי.
- בדרכים אחרות:

מדבקות המכילות פנטניל תרופה אופיואידית לשיכוך כאבים חזקים
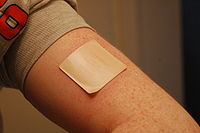
מדבקות אלו מודבקות על העור ומאפשרות את חדירת החומר הפעיל של התרופה אל תוך מחזור הדם דרך העור. דוגמאות: מדבקות אופיואידים לטיפול בכאב, או מדבקות ניקוטין לטיפול בהתמכרות לעישון טבק. להבדיל ממתן טופקלי העור כאן אינו איבר המטרה אלא רק דרך לעקוף את מערכת העיכול או ליצור מתן סיסטמי של התרופה.
- טרנסמוקוסלית (דרך ריריות), דרך מתן לא נפוצה של ספיגה סיסטמית של תרופה דרך ריריות האף. לדוגמה מתן מינירין (הורמון סינתטי המשמש כתרופה לטיפול בהרטבות לילה).
- מתן שאיפתי, לשימוש סיסטמי, לדוגמה שאיפת מרדימים נדיפים.
סוגי תרופות
ניתן לחלק את התרופות למספר סוגים על פי קריטריונים שונים. תרופה מסוימת יכולה להתאים ליותר מסוג אחד.
חלוקה משפטית, בישראל
תרופות מרשם
תרופות מרשם רופא מחולקות ל 4 קטגוריות:
- תרופות מרשם רגילות מכונות גם Separanda (משום שהן מופרדות מהקהל) מוקסיפן (amoxycillin) – תרופות אלו דורשות כתיבת מרשם על ידי רופא, רופא שיניים או וטרינר טרם רכישתם.
- תרופות המסווגות כטוקסיקה – מסומנות באות T, מסודרות בבית מרקחת במקום נפרד וייעודי ולא בסמוך לתרופות separanda. אלו הן עם חלון תירפויטי צר במיוחד, שמנה עודפת קטנה שלהן עלולה להיות עם סיכון משמעותי לבריאות המטופלים. דוגמאות קולכיצין ו-דיגוקסין.
- תרופות פסיכוטרופיות – סמי שינה והרגעה למשל בונדורמין (brotizolam) - אלו הן תרופות בעלי פוטנציאל התמכרות או שהן מרדימות ולכן נמצאות תחת הגדרה נפרדת.
- תרופות המכונות בפקודות "סמים מסוכנים" – המונח "סם מסוכן" הוא מונח ארכאי ואיננו מתאים כיום, שכן הוא התרופות האלו אינן מסוכנות יותר מתרופות אחרות אך יש למרביתן פוטנציאל התמכרות גבוה. ההגדרה המתאימה יותר לתרופות אלו היא בדומה לשמן בארצות הברית ובבריטניה, "תרופות תחת פיקוח" (באנגלית: controlled drugs)
תרופות המוגדרות בישראל כ"סם מסוכן" או "תרופה תחת פיקוח" הן תרופות המכילות חומרים פעילים נרקוטיים כגון מורפין ופנטניל. כמו כן הרשימה כוללות תרופות נוספות בעלי פוטנציאל התמכרות כגון מתילפנידאט (ריטלין) ודקסמתילפנידאט. לתרופות אלו נדרש מתן מרשם מיוחד וכמו כן גם על הרופא וגם על הרוקח חלים פקודות ותקנות נוספות הנוגעים לרישום, שיווק, ייצור וטיפול בתרופות אלו.
תרופות ללא מרשם
תרופות ללא מרשם רכישת מרבית התרופות מצריכה מרשם של רופא, תרופות הנמכרות גם ללא מרשם רופא מחולקות בישראל לשתי קטגוריות:
תרופות לשיווק כללי

תרופות לשיווק כללי (נקראות גם תל"ם – תרופות ללא מרשם; באנגלית: GSL – General Sales List).
אלו הן תרופות ללא מרשם המותרות למכירה מחוץ לביתי המרקחת, בחנויות אחרות שקיבלו היתר לכך ממשרד הבריאות.
זוהי קטגוריה חדשה יחסית (משנת 2005) של תרופות ומכילה כ 200 תכשירים בלבד. חלק מהתרופות האלו כוללות גם הגבלת כמות (כגון הגבלה על כמות הכדורים באריזה למכירה).
תרופות לשיווק על ידי רוקח
תרופות ללא מרשם לשיווק על ידי רוקח – (באנגליה תרופות אלו נקראות P medicine). מכירתן מותרת רק על ידי רוקח בבתי מרקחת. דוגמאות בישראל כוללות את אופטלגין. תרופות אלו יכולות לכלול גם תרופות שמוגדרות כתל"ם אולם אריזתם תכיל כמות גדולה יותר של התרופה.
קיימים מצבים שבהן תרופות מרשם הופכות להיות תרופות ללא מרשם וגם אז הן מוגבלות מבחינת כמות כדורים באריזה.
קיימים מצבים שבהם תרופות ללא מרשם הופכות להיות תרופות מרשם.
חלוקה פרמקולוגית על פי איברי המטרה
חלוקה לפי השפעה על מערכת מסוימת בגוף. לדוגמה:
- תרופות אוטונומיות, משפיעות על מערכת העצבים האוטונומית.
- תרופות קרדיוסקולריות, משפיעות על הלב וכלי הדם.
- תרופות אנטידלקתיות, כוללות משככי כאבים וסטרואידים.
- תרופות נוגדות פרכוסים פועלות על המוח ומפחיתות פעילות אפילפטית במוח.
- תרופות כימותרפיות הם ציטוטקסיות ומשמשות להרס תאים הומניים, בעיקר לטיפול בסרטן אך גם במחלות אוטואימוניות. כימותרפיה כוללת גם את התרופות ה אנטיביטיות לטיפול בזיהומים הנגרמים על ידי חיידקים, תרופות אנטיווירליות לטיפול בזיהומים נגיפיים ותרופות אנטימיקוטיות לטיפול בפטרת.
חלוקה פרמקולוגית על פי אופן הפעולה
תרופות יכולות לחקות תהליך פיזיולוגי בגוף אך גם יכולות לנגוד את הפעילות הפיזיולוגית. לפיכך מקובל לחלק את התרופות על פי אופן פעולתן לשני סוגים עיקריים:
- אגוניסט - תרופה שמחקה פעילות פיזיולוגית של חומר פיזיולוגי בגוף. דוגמה לכך היא מתן של תרופות אגוניסטיות לדופמין. תרופות אלו פועלות על קולטנים לדופמין במוח ומחקות את פעילות דופמין במוח ומהוות טיפול במחלת פרקינסון.
- אנטגוניסט - סוג של תרופה שמתנגדת או מעכבת את הפעולה הפיזיולוגית של חומרים פיזיולוגיים בגוף. דוגמאות כוללות חוסמי אלפא אשר נוגדים את פעילותו של אדרנלין ונוראדרנלין ותרופות המעכבות פעילות אנזימים כגון מעכבי ACE.
קיימות חלוקות נוספות על פי אופן הפעולה כגון אגוניסט חלקי, מעכבים הפיכים ומעכבים בלתי הפיכים.
חלוקה לפי משפחות תרופות
תרופות לטיפול במחלות מסוימות או תרופות שפועלות על אזורים מסוימים בגוף האדם מחולקות גם על פי דרך פעולתן למשפחות.
דוגמאות: בטיפול ביתר לחץ דם, קיימות משפחות רבות של תרופות נוגדות יתר לחץ דם כגון חוסמי בטא, חוסמי תעלות סידן, מעכבי ACE ו-חוסמי הקולטן לאנגיוטנסין II. בטיפול בפרקינסון, קיימות תרופות ממשפחת האגוניסטים לדופמין, מעכבי דופה-דקארבוקסילאז, לבודופה ומעכבי MAO.
חלוקה כימית
חלוקה על פי סוג התרכובות המהווה את החומר הפעיל בתרופה:
תרכובות אורגניות

קבוצת התרכובות האורגניות מהווה את החלק הארי והכמעט מוחלט של החומרים התרופתיים. מדובר בתרכובות המבוססות על שלד של אטומי פחמן ומימן ואטומים נוספים כגון: חמצן, חנקן, גופרית, זרחן (כתלות בתרכובות) שביניהן קשרים קוולנטיים.
המולקולה הראשונה שסונתזה כחומר פעיל נקי ושווקה כתרופה מסחרית היא ה"אצטיל סליציליק אסיד" או בשמה המסחרי הראשון אספירין.
מרבית התרכובות האורגניות המשמשות כתרופות, יוצרו באופן סינתטי (מלאכותי) במעבדה הכימית. אולם, חלק מהתרופות עשויות להתקבל בתהליכים חצי-סינתטיים (מלאכותיים למחצה), כלומר ביצוע של עיבוד כימי לחומרי טבע שהתקבלו בתהליכי מיצוי, זיקוק והפרדה.
לעיתים קרובות, הייצור של התרכובות האורגניות נעשה בשיטות ביוטכנולוגיות, כלומר במקום ייצור כימי ישיר של התרופה על ידי סינתזה אורגנית קלאסית, נעשה שימוש ביצרנים ביולוגים כגון פטריות או חיידקים לייצור של התרכובות הרצויות (ראו ביוסינתזה, ביוטכנולוגיה).
דוגמאות לתרופות המבוססות על תרכובות אורגניות:
תרופות טבעיות (המופקות מצמחים) כגון דיגוקסין (תרופה המופקת מצמח האצבעונית ומשמשת לטיפול באי ספיקת לב ובהפרעות קצב), קולכיצין (תרופה המופקת מצמח הסתוונית ומשמשת בטיפול בגאוט ובקדחת ים תיכונית משפחתית, גאלאנטאמין (תרופה לטיפול באלצהיימר המופקת מנרקיסים) ומורפין (תרופה נוגדת כאבים המופקת מפרג האופיום).
תרכובות אי-אורגניות

תרכובות אי-אורגניות קבוצה קטנה יותר הן מבחינה כימית וכן מבחינת כמות התרופות. מדובר בתרכובות המבוססות על מלחים של מתכות. דוגמה לתרופה כזו היא ליתיום פחמתי (lithium carbonate), המשמשת לטיפול בהפרעה דו-קוטבית. תרופה זו עלולה להיות רעילה אם ניטלת במינון עודף וזאת בשל חלון תרפויטי צר.
דוגמה נוספת, היא זו של מגנזיום הידרוקסיד (ידוע גם כ"חלב מגנזיה") זוהי תרופה המשמשת לסתירה של חומציות יתר בקיבה ולהקלה של צרבות.
תרכובות אורגנו-מתכתיות
אלו הן תרכובות המבוססות על שלד אורגני המחובר למרכז מתכתי באמצעות קישור קואורדנטיבי.
פפטידים - מולקולות ביולוגיות קטנות

אלו הן מולקולות ביולוגיות המכילות מספר קטן של חומצות אמינו ומכונות פפטידים. דוגמאות לכך כוללות את ההורמון אינסולין המשמש לטיפול בסוכרת. אינסולין ניתן רק בהזרקה כי הוא לא עמיד במעבר במערכת העיכול, ואינן חדירות במעבר טרנדרמלי (דרך העור). מאמצים רבים נעשים בתחום הרוקחות למציאת פתרון לנטילה יותר נוחה יותר של אינסולין בהם מחקרים באלקטרופרוזיס ומשאפים נאזליים. בשנת 2015 יצא תכשיר אינסולין חדש במתן אפי. דוגמה נוספת לטיפול בפפטידים היא התרופה desmopressin המכילה 9 חומצות אמינו בדומה להורמון נוגד השתנה. תרופה זאת משמשת בטיפול בסוכרת תפלה. היא קיימת בשם המסחרי Minirin ומשווקת בפורמולות של טבליות בליעה, טבליות הנמסות בפה ותרסיס לאף.
מולקולות ביולוגיות מורכבות

 ערך מורחב – תרופה ביולוגית
ערך מורחב – תרופה ביולוגית
זוהי הקבוצה החדשה ביותר של תרופות שיצאה לשוק בסוף המאה ה-20. אלו הן מולקולות ביולוגיות גדולות ומורכבות. תרופות אלו מוגדות כתרופות ביולוגיות, והנציגים שלה הם נוגדנים מסוגים שונים הניתנים בהזרקה. הנוגדנים משמשים היום גם במחקר וכמו כן בטיפול במחלות דלקתיות וממאירויות. דוגמאות כוללות:
- אינפליקסימאב, אדאלימומאב, אטאנרצפט - אלו הן תרופות ביולוגיות המכוונות כנגד ציטוקינים TNF המשמשות לטיפול בסוגים שונים של מחלות חיסון עצמי.
- ריטוקסימאב המכוונת נגד תאי B המשמשת בטיפול של מגוון סוגים של סרטן ומחלת חיסון עצמי.
- אנאקינרה המכוונת כנגד אינטרלאוקין 1 (IL-1) ומשמשת בטיפול בדלקת פרקים שגרונית ובקדחת ים תיכונית משפחתית.
- אפליברספט המכוונת נגד חלבון VEGF – חלבון המהווה "פקטור צמיחה" (vascular endothelial growth factor) ומעודד צמיחה פתולוגית של כלי הדם הלא תקינים במחלות רשתית.
תרופות באוכלוסיות מיוחדות
למספר אוכלוסיות ההתאמה של הטיפול התרופתי חייבת להיעשות בהשגחה יתרה של הרופא או הרוקח (לתרופות ללא מרשם):
- נשים הרות - נטילת תרופות במהלך הריון עלולה לגרום לנזק לעובר. מאז מקרה התלידומיד, מקובל להגביל באופן משמעותי מתן תרופות לנשים בהריון וקיימות תרופות שאסור ליטול אותן בהריון. הענף העוסק במומים מולדים נקרא טרטולוגיה.
- נשים מניקות - תרופות עלולות להיות מופרשות בחלב האם ולהגיע לתינוק שיונק מהאם. לפיכך קיימות תרופות שאפשר להניק איתן וקיימות תרופות שאין להשתמש בהן בהנקה.
- יילודים ותינוקות - תינוקות שונים מילדים ואנשים מבוגרים ממספר סיבות, וביניהם מערכת לא מפותחת של אנזימים בכבד ובמערכת העיכול ומערכת חיסון חלשה יותר. לפיכך תינוקות מפרקים תרופות בצורה שונה ממבוגרים וילדים. לא כל התרופות שמתאימות לילדים מתאימות גם לתינוקות.
- ילדים - ילדים רגישים יותר לתופעות לוואי של תרופות, הם בעלי משקל גוף קטן יותר שדורש התאמות מינון וכמו כן מערכות הגוף שלהן אינן מתפקדות כמו אצל מבוגרים.
- מטופלים הסובלים ממחלות בכבד או בכליות - מטופלים אלו ידרשו התאמות מינונים בתרופות, משום שהאיברים הפגועים שלהם מתקשים בתפקוד הפיזיולוגי הקשור לפירוק והפרשת תרופות מהגוף.
- טיפול תרופתי במצב של ריבוי תרופות - בכל מקרה של נטילת מספר תרופות במקביל עלול להיוצר אינטראקציות על רקע תחרות בפינוי התרופה: אם רמות התרופה בדם עולות יש להפחית את המינון. אם עקב אינדוקציה של האנזים המפרק את התרופות הרמות של התרופות נמוכות מהמתוכנן, יש להגדיל את המינון.
- קשישים – אוכלוסיית הקשישים רגישה יותר לתופעות לוואי של תרופות מאחר שהקשישים עוברים שינויים פיזיולוגיים בתהליך הזקנה המתאפיין בירידה בתפקוד הכלייתי והכבדי וכמו כן ירידה בתפקוד מערכות הגוף.
פיתוח וייצור תרופות
בתקופה המודרנית תרופה מיוצרת על ידי חברת תרופות או תכשיר גלני שנרקח בבית מרקחת על ידי רוקח מוסמך. שיווק תכשיר כתרופה מחייב אישור רשויות הבריאות של המדינה (בישראל אגף הרוקחות של משרד הבריאות ובארצות הברית המנהל המזון והתרופות האמריקאי, ה-FDA).
תהליך פיתוחה ואישורה של תרופה חדשה הוא תהליך יקר וממושך מאוד. ההערכות הן שפיתוח תרופה חדשה כיום לוקח לפחות 5 שנים ועולה בין כמה מאות מיליוני דולרים לכמה מיליארדים. התהליך כולל כמה שלבים:
- מודל - מעבדת מחקר מציעה מודל לחומר חדש, תהליך זה נעשה כיום רבות על ידי מודלים ממוחשבים - In Silico.
- סינון - סקרינינג, מאות או אלפים של מולקולות המבוססות על המודל נבדקות ברמת המבחנה - אין ויטרו.
- פרמקולוגיה - בדיקת האפקט הפרמקולוגי של מספר מועמדים נבחרים במודלים של בעלי חיים - אין ויוו.
- ניסויים קליניים - ווידוא האפקט הפרמקולוגי בבני אדם ובדיקה שהתרופה אינה מסוכנת למשתמשים בה. ניסויים קליניים חייבים להיעשות על ידי רופא ובפיקוח ועדה ממשלתית (ועדת הלסינקי). הניסוי הקליני נעשה בדרך כלל בשלושה שלבים.
- בדיקה לאחר מתן האישור לתרופה - גם תרופות שכבר אושרו מתגלות כמסוכנות לפעמים היות שאוכלוסיית המחקר מוגבלת בכמותה.
בתעשיית התרופות ידועות מולקולות כיראליות שונות, שרק גרסה אחת שלהן מבצעת את פעולת הריפוי, ואילו הגרסה השנייה אינה מועילה, ולעיתים אפילו מזיקה. כדוגמה ניתן לציין את התלידומיד שאננטיומר אחד שלו מקל על בחילות בוקר של נשים בהריון, ואילו לאננטיומר השני יש אפקט טרטוגני, כלומר פוגע בהתפתחות העובר. תרופה זו שניתנה לנשים בהריון בשנות השישים של המאה ה-20 הביאה ללידת תינוקות חסרי גפיים. בארצות-הברית, הטרגדיה נמנעה משום שהתרופה לא אושרה לשימוש. הידע שהצטבר בתחום הסטריאוכימיה מאפשר כיום לייצר תרופות בתגובות סטריאוסלקטיביות, כלומר כאלו שנוצר בהן עודף משמעותי של אחד הסטריאואיזומרים.
בעולם שני גופים מרכזיים העוסקים באישור תרופות - הFDA האמריקאי וה-EDMA האירופי. בנוסף נערכים מבחנים קליניים לשם אישור תרופות ביפן ובהיקף קטן יותר בקוריאה הדרומית. לגבי אירופה יש הסדר מיוחד המאפשר לעקוף את ה-EDMA לאישור תרופה על ידי משרדי הבריאות הלאומיים (הרבה חברות תרופות נוטות לרשום תרופות בדנמרק בזכות חוקיה הפשוטים יחסית). ה-FDA אינו מחויב להחלטות אירופיות, לכן נוטים יצרני התרופות לענות על הקריטריונים הן של הרשויות האירופיות והן של ה-FDA.
מאחר שבישראל לא מנוהלים ניסויים קליניים גדולים, תרופה מאושרת לשימוש בישראל רק אם היא אושרה על ידי ה-FDA, האיחוד האירופי או יפן (לפעמים מחייבת ישראל את החברה המייצרת לשינויים מסוימים כמו שינוי שם התרופה או בעלון לצרכן). ייצורן של תרופות נעשה בתעשייה הפרמצבטית, שמבחינתה נחלקות התרופות לשני סוגים:
- תרופות אתיות, שהן תרופות מוגנות פטנט, שרק מי שפיתח אותן רשאי ליצרן. הגנת פטנט על תרופה נמשכת עשרים שנה מיום רישום הפטנט, שבהן מספקת ההגנה למפתח התרופה את היכולת להחזיר לעצמו את ההשקעה בפיתוח התרופה (למעשה, כתריסר שנים חולפות מיום רישום הפטנט ועד תחילת השיווק הסדיר של התרופה, כך שליצרן התרופה נותרות רק כשמונה שנים של בלעדיות).
- תרופות גנריות, שהן תרופות שהגנת הפטנט עליהן הסתיימה, ולכן כל חברת תרופות רשאית לייצר אותן.
בישראל תעשיית תרופות מפותחת למדי, ומרבית תפוקתה כוללת תרופות גנריות. יצרני התרופות הבולטים בישראל הם:
ראו גם
- פרמקולוגיה – חקר התרופות והשפעתן
- רפואה
- אפקט הפלצבו
- ניסוי קליני
- שיכוך כאב
- תרופת סבתא
- היענות תרופתית
- תופעת לוואי
קישורים חיצוניים
- איתי גל, סוד רפואי: כך ממציאים שמות לתרופות, באתר ynet, 4 בינואר 2013
- מאגר תרופות מקצועי של ארגון רוקחות בישראל
- תקנות הרוקחים (מכירה של תכשיר בלא מרשם שלא בבית מרקחת או שלא בידי רוקח), התשס"ז–2006, באתר משרד הבריאות
- סל שרותי הבריאות הכולל את סל התרופות, באתר משרד הבריאות
- תרופות בסל הבריאות, באתר כל זכות
- מדריך תרופות באתר "הכללית"
- איתי להט, החיים כפטנט, באתר כלכליסט, 8 בדצמבר 2011
- Ben Goldacre: What doctors don't know about the drugs they prescribe – הרצאה מאתר TED על הסכנה בהימנעות מפרסום תוצאות שלליות של מחקרים על תרופות.

- בן גולדייקר: להילחם במדע גרוע – הרצאה על מחקרים אודות תרופות באנגלית מאתר TED עם כתוביות בעברית

 רוני לינדר-גנץ, החיים שלך, תמורת מיליון שקל: התרופות לסרטן שיכלו להציל את אבא שלי, באתר TheMarker, 19 בפברואר 2016
רוני לינדר-גנץ, החיים שלך, תמורת מיליון שקל: התרופות לסרטן שיכלו להציל את אבא שלי, באתר TheMarker, 19 בפברואר 2016 רוני לינדר-גנץ, מה באמת עומד מאחורי המחיר המטורף של התרופות שמצילות חיים?, באתר TheMarker, 26 בפברואר 2016
רוני לינדר-גנץ, מה באמת עומד מאחורי המחיר המטורף של התרופות שמצילות חיים?, באתר TheMarker, 26 בפברואר 2016
הערות שוליים
- ^ http://www.health.gov.il/LegislationLibrary/Rokhut23.pdf פקודת הרוקחים - נוסח חדש 1981
- ^ (a) Any substance or combination of substances presented as having properties for treating or preventing disease in human beings; or (b) Any substance or combination of substances which may be used in or administered to human beings either with a view to restoring, correcting or modifying physiological functions by exerting a pharmacological, immunological or metabolic action, or to making a medical diagnosis.
- ^ מילון מונחים של ה-FDA באתר: http://www.fda.gov/Drugs/InformationOnDrugs/ucm079436.htm
- ^ Lippincott’s Illustrated Reviews: Pharmacology 5th edition. Lippincott Williams & Wilkins, a Wolters Kluwer business. 2012
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.

