פורטל:כימיה/תמונה נבחרת/גלריה
אוסף תמונות נבחרות בנושא כימיה
לעריכת סדרות התמונות לחצו על המספר בכותרת ואחר כך "עריכה".
1
 |
| נוזל מגנטי משנה צורתו תחת השפעתו של שדה מגנטי. |
2
 |
| גביש נחושת גופרתית, אחת התרכובות המוכרות ביותר של הנחושת. |
3

גבישי כרום טהור שנוצרו מתגובה כימית, ליד קובייה של היסוד. כרום היא מתכת אפורה, מבריקה וחזקה, המשמשת בעיקר בפלדת אל חלד.
4

גביש של גליום. גליום הוא אחד מהיסודות הכימיים שאת קיומם ותכונותיהם ניבא דימיטרי מנדלייב על סמך הטבלה המחזורית שיצר. יסוד זה התגלה רק ב-1875 ותאם לתחזית במרבית תכונותיו. הגליום הוא מתכת בעלת טמפרטורת התכה של 29.9°C, מהמתכות היחידות בעלות טמפרטורת התכה הקרובה לטמפרטורת החדר. היישום העיקרי של גליום הוא כחלק ממוליכים למחצה מורכבים, ובמיוחד גליום ארסניד (GaAs) וגליום ניטריד (GaN).
5

|
| אב טיפוס של מנוע יוני קסנון בזמן ניסוי במעבדת מנועי הסילון של נאס"א. |
6
 |
| הסמלים בהם השתמש ג'ון דלטון לתיאור האטומים של היסודות שהיו ידועים בתקופתו. |
7
 |
| גרף המציג באופן חזותי את השפעת שינוי הטמפרטורה על מצב הצבירה, ואת התהליך שהחומר עובר על מנת לשנות מצב צבירה. |
8
 |
| ספקטרום הפליטה של ברזל בתחום האור הנראה. אלקטרון באטום מסוים יפלוט פוטון (קרינה אלקטרומגנטית) כאשר הוא יורד ברמת האנרגיה שלו. באנליזה ספקטרוגרפית ובספקטרוסקופיה בכללותה, מודדים הכימאים את ספקטרום פליטת הקרינה האלקטרומגנטית באמצעות מכשיר הנקרא ספקטרוסקופ. על ידי השוואה בין ספקטרומי פליטה ידועים מראש ניתן לגלות את הרכב החומר, שיטה מועילה כאשר גוף הבדיקה רחוק מהבודק, כמו למשל בבדיקת ספקטרום הפליטה של כוכבים. |
9
 |
| הפרדה של דיו למרכיביו באמצעות כרומטוגרפיית שכבה דקה. |
10
 |
| הצגת הצורות המרחביות של האורביטלים אטומיים (בשורה העליונה) ואורביטלים מולקולריים (שורה תחתונה). אורביטל הוא הסתברות למציאת אלקטרון במקום מסוים ברמת אנרגיה באטום. האורביטל היא פונקציית הגל המתקבלת כתוצאה ממשוואת שרדינגר. אורביטל, הן מולקולרי והן אטומי, יכול לאכלס עד 2 אלקטרונים בעלי ספין הפוך. אורביטל מולקולרי מתקבל מחיבור או חיסור פונקציות הגל. כתוצאה מחיבור הפונקציות אנו מקבלים אורביטל קושר, בעל אנרגיה נמוכה מזו של שני האורביטלים האטומים היוצרים אותה, ואורביטל אנטי-קושר המתקבל מחיסור פונקציות הגל, הגבוה באנרגיה מזו של שני האורביטלים האטומים היוצרים אותו. באיור ניתן לראות את הסימטריה בין האורביטל האטומי 1S לבין האורביטל המולקולרי σ1S, הנראה כשני 1S שחיברו את מרכזן. כך נראים גם 2P ו-σ2P (ישנם 3 2P, אחד לכל ציר במרחב: X, Y ו-Z). |
11
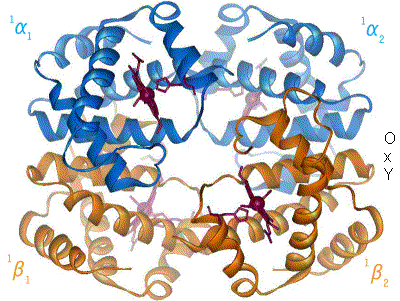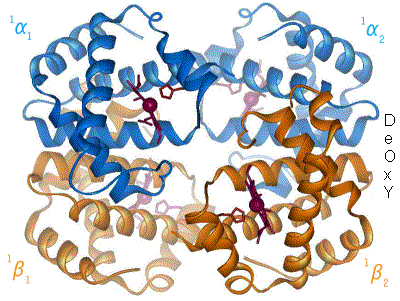
12

13

14

15

16

17

העלאת הטמפרטורה באוויר שבתוך הכדור הפורח גורמת לו להפוך לקל מן האוויר שמחוץ לבלון ולהתרומם מן הקרקע
18

גביש ביסמוט. ביסמוט היא מתכת בצבע לבן עם גוון ורוד. גביש הביסמוט בתמונה מצופה בשכבה דקה של תחמוצת הגורמת למגוון הצבעים, תופעה המכונה התאבכות משכבות דקות.

קוביית ביסמוט טהור ולידה גביש ביסמוט ששכבתו החיצונית עברה חמצון, תגובה כימית הגורמת להחלפת צבעו. ביסמוט הוא יסוד כימי מתכתי שסמלו הכימי Bi ומספרו האטומי 83. הביסמוט כבד, שביר, צבעו בתצורתו הטהורה לבן הנוטה לוורוד, והוא דומה מבחינה כימית לארסן ולאנטימון.
19

התפרצות כתוצאה מהתגרענות הנוצרת לאחר הכנסת חמש סוכריות מנטוס למשקאות מוגזים, משמאל לימין: מי סודה, קוקה קולה, ספרייט ודיאט קולה.
התפרצות כתוצאה מהתגרענות (בלשון עממית: "התפרצות מנטוס") היא תופעה, המתרחשת כשמכניסים סוכריות מנטוס לתוך בקבוק משקה מוגז. לאחר זמן קצר ניתז מאליו המשקה המוגז, מפתח הבקבוק, בסילון חזק שגובהו עשוי להגיע למספר מטרים. תוצאות דומות מתקבלות אם מבצעים את הניסוי בהכנסת מוצק מסיס אחר, כמו מלח או סוכר, במשקה מוגז כלשהו.
20

21

22
23

רתך בעת עבודת ריתוך. ריתוך הינו פעולה פיזיקלית של חיבור מתכות באמצעות יצירת קשרים בין-אטומיים בין פניהן. עבודת הריתוך כרוכה בקרבה למקור של חום גבוה, ובתהליכה נפלטים קרינה על סגולה וגזים המסוכנים לנשימה. מסיבה זו קיים צורך מובהק בשימוש באמצעי בטיחות מתאימים, כגון כפפות עור ומשקפי מגן מיוחדים.
24

גוש ספסרטין מסין. ספרסטין הוא מינרל נזוסיליקטי השייך לקבוצת הגארנט. השימוש המסחרי הנפוץ ביותר של המינרל הוא כאבן חן. הקשיות הגבוהה יחסית, והגוונים האדומים שלו, הפכו אותו לאבן חן פופולרית, אם כי ספסרטין באיכות של אבן חן הוא נדיר למדי. המקורות העיקריים לספסרטין באיכות של אבן חן הם סרי לנקה ומדינת מינאס ז'ראיס ברזיל.
25

חקלאים אוספים מלח בשדות מלח בתאילנד. המלח משמש הן לתיבול מזון והן בתהליכי ההכנה והשימור שלו. ברומא העתיקה היו ניתנים שקי מלח כמענק לחיילים, מענק שנקרא בלטינית salarium, מלשון Sal (מלח), ומכך נגזרה המילה משכורת במספר שפות אירופיות.
26

גלגל שיניים הוא גלגל אשר בהיקפו מסודרות שיניים במרחקים שווים אחת מן השנייה, אשר נועד להעביר מומנט (שילוב של כוח ותנועה) לגלגל שיניים נוסף או לכל רכיב משונן אחר. בצמד גלגלי שיניים, כאשר גלגל אחד מסתובב לכיוון מסוים, הגלגל השני מסתובב בכיוון ההפוך. בתמונה - גלגל שיניים חלוד, במפעל נטוש בספרד.
27

מכבי אש הם שירות חירום שתפקידו העיקרי הוא להילחם בשריפות ובהתפשטות אש בלתי מבוקרת. בנוסף לכך, כוחות מכבי האש עוסקים גם בפעולות חילוץ והצלת לכודים.
28

גפרור הוא מקל עץ המצופה בזרחן ומחמצן כלשהו ומשמש להצתת אש. בשנת 1680 גילה רוברט בויל האנגלי, כי אם ישופשפו זה בזה זרחן וגופרית, הם יתפרצו בלהבה מיידית, דבר שהוביל להמצאת הגפרור.
29

מדורה היא הדלקת אש מבוקרת בשטח חיצוני מצומצם, למטרות שונות. המדורה משמשת בעיקר לחימום הגוף ליושבים בחוץ בלילות קרים, לבישול מזון, לאיתות ולציון חגים שונים, כגון ל"ג בעומר בישראל או ליל גאי פוקס הנחוג ב-5 בנובמבר בבריטניה. חלק מהווי הפלמ"ח היה הקומזיץ, מפגש חברתי הנערך סביב מדורה, שכלל שירה בציבור, צ'יזבאטים ואכילת קרטושקעס - תפוחי אדמה שנאפים במדורה עצמה. אחר קום מדינת ישראל הפך הקומזיץ לפעילות נפוצה בתנועות הנוער.
30

תרגיל כיבוי אש של חיל הנחתים האמריקני. מכבי אש הם שירות חירום שתפקידו העיקרי הוא להילחם בשריפות ובהתפשטות אש בלתי מבוקרת. בנוסף לכך, כוחות מכבי האש עוסקים גם בפעולות חילוץ והצלת לכודים.
31

"שער הגיהנום" - בור בכפר דרווזה שבטורקמניסטן, שבתוכו אש הבוערת ברצף מאז שנת 1971 בשל הגז הטבעי המצוי באדמה. הבור נוצר בטעות, כשגאולוגים סובייטים קדחו אל תוך חלל תת-קרקעי. כדי להיפטר מהגז שבבור, הם החליטו לכלות אותו על ידי הדלקתו. לפי הערכתם, הגז היה אמור להיגמר תוך כמה ימים, אולם בפועל, הבור בוער מאז עד עתה.
32

שבבי ברזל טהור שזוקקו באלקטרוליזה. ברזל הוא היסוד הכימי הנפוץ ביותר (מבחינת מסה) בכדור הארץ (כולל פנימו). הברזל הוא יסוד מתכתי המשמש רבות בביולוגיה ובתעשייה.
33

גארנט - קבוצת מינרלים נזוסיליקטיים (כלומר, סיליקטים במבנה של איים) המונה שישה סוגי מינרלים. היסודות הכימיים המשתתפים בבניית סוגי הגארנט השונים כוללים: סידן, מגנזיום, אלומיניום, ברזל דו-ערכי, ברזל תלת-ערכי, כרום, מנגן וטיטניום. הגארנטים נפוצים מאוד בחלקו התחתון של קרום כדור הארץ ובמעטפת כדור הארץ ומשחקים תפקיד חשוב בהבנת הגאוכימיה של כדור הארץ.
34

ליזה מייטנר ואוטו האן במעבדה ב-1913. ליזה מייטנר, הפיזיקאית שעל שמה קרוי היסוד הכימי מייטנריום, נמלטה מגרמניה עקב מוצאה היהודי. ב-1944 זכה אוטו האן בפרס נובל לכימיה על גילוי תהליך הביקוע הגרעיני, תגלית שאותה הוא חלק עם מייטנר. יש הסבורים שמייטנר לא קיבלה פרס נובל בעקבות כך שהשופט בוועדה, מאנה סיגבאן, שנא נשים מדעניות.
35

ארנסט רתרפורד היה פיזיקאי ניו זילנדי, חתן פרס נובל לכימיה לשנת 1908. בעקבות תוצאה של ניסוי רתרפורד, פיתח את המודל הפלנטרי המתאר את מבנה האטום. מודל זה סתר את מודל עוגת הצימוקים שהיה מקובל בזמנו. היה לראשון שביצע ניסוי בו יסוד כימי אחד הופך לאחר. הגדיר את קרינת אלפא וקרינת בטא.
36

נשיא מדינת ישראל פרופ' חיים ויצמן בשנת 1949. ויצמן היה נשיאה הראשון של מדינת ישראל, כימאי, מראשי הציונות ומנהיג גישת הציונות הסינתטית וכן נשיאה הרביעי של ההסתדרות הציונית. עבודתו במעבדות המחקר הכימיות של הצי הבריטי, שבעקבותיה פיתח קשרים במסדרונות השלטון הבריטי, נחשבת כבעלת תרומה מכרעת לפרסום הצהרת בלפור ב-1917. לאחר פרסומה ויצמן עזב את עבודתו המדעית כמעט לחלוטין, והתמסר לפעילות המדינית הציונית. בשנת 1931 החל לעבוד במעבדה ב"מכון דניאל זיו", ששמה שונה ב-1949 למכון ויצמן למדע. אחיינו, עזר ויצמן, היה לנשיא השביעי של מדינת ישראל.
37

האריסטוקרט הצרפתי אנטואן לָבוּאַזיֶה יחד עם שותפתו לעבודה המדעית ואשתו, מארי-אן פִּירֶט פּוֹלז, בציור מעשה ידיו של הצייר ז'אק-לואי דויד משנת 1788. לבואזיה היה כימאי חשוב שניסח את חוק שימור החומר ונחשב לאבי הכימיה האנליטית. בהיותו גם גובה מס לאוצר המלך, הוכרז בימי המהפכה הצרפתית כ"אויב האומה" והוצא להורג בשנת 1794.
38

סר ג'ון הרשל, 1867, צילום מעשה ידי ג'וליה מרגרט קמרון, הצלמת המפורסמת ביותר בתקופה הוויקטוריאנית. ג'ון הרשל היה איש אשכולות אנגלי: מתמטיקאי, אסטרונום, כימאי ומחלוצי הצילום. הרשל היה בנו היחיד של האסטרונום ויליאם הרשל. הוא נתן שם לשבעה מהירחים של כוכב הלכת שבתאי ולארבעה מהירחים של אורנוס, הרים תרומות חשובות להתפתחות הצילום, וחקר את תופעת עיוורון הצבעים ואת ההשפעה הכימית של קרינת על-סגול.
39

ג'יימס ווטסון ומאחוריו פסל בצורת מבנה הדי-אן-איי. ווטסון הוא גנטיקאי אמריקאי שגילה בשנת 1953 יחד עם פרנסיס קריק את מבנה מולקולת הדי-אן-איי במעבדת קוונדיש שבאוניברסיטת קיימברידג', בריטניה. על הישג זה הוענק לו פרס נובל לפיזיולוגיה או לרפואה לשנת 1962 יחד עם קריק ומוריס וילקינס. בשנת 1968 ראה אור ספרו "הסליל הכפול", בו תיאר את גילוי מבנה ה-DNA במשפט: "מבנה כל כך יפה פשוט חייב היה להתקיים."
